Системний червоний вовчак (СЧВ) — хронічне автоімунне захворювання невизначеної етіології, що розвивається під впливом численних ендогенних і екзогенних факторів на основі генетичної схильності, характеризується гіперпродукцією широкого спектра автоантитіл та імунних комплексів, що викликають імунозапальні ураження внутрішніх органів [1, 13].
На СЧВ хворіють переважно дівчата або особи жіночої статі; хлопчики і чоловіки становлять лише 5–10 % від загальної кількості хворих. Підвищення захворюваності у дітей починається з 9-річного віку, пік її припадає на 12–15 років, тобто на вік максимального напруження фізіологічних процесів в організмі у пубертатному періоді [2, 15].
У дебюті СЧВ клінічна картина хвороби може бути поліморфною та включати різноманітні симптоми — від незначних до тяжких проявів, захворювання може мати хвилеподібний або безперервно прогресуючий перебіг. З урахуванням широкого спектра клінічних проявів СЧВ у дитячому та підлітковому віці проблема ранньої діагностики захворювання і призначення своєчасної адекватної терапії залишається актуальною, потребує постійної уваги педіатрів і дитячих ревматологів [3, 14].
Найчастішими клінічними проявами СЧВ у дітей є лихоманка, ураження шкіри, суглобовий, м’язовий, судинний, церебральний, гематологічний синдроми, серозити, полівісцерити (кардит, пульмоніт, нефрит, гепато- і спленомегалія) на тлі патологічного загальнотрофічного симптомокомплексу: різке схуднення у поєднанні з розладами трофіки (підвищене випадіння та ламкість волосся, алопеція, дистрофічні зміни нігтів і шкіри) [5, 16].
Класичні прояви СЧВ — так звана вовчакова тріада (дерматит на обличчі у формі метелика, неерозивні артрити, полісерозити) спостерігається далеко не в усіх пацієнтів. У низці випадків висип на шкірі має настільки неспецифічний характер, що його природа може бути остаточно визначена лише завдяки результатам морфологічних досліджень.
До числа ранніх симптомів СЧВ відносять лихоманку, загальне нездужання (37–100 % пацієнтів), втрату маси тіла (21–32 %), лімфаденопатію (13–45 %). Від 60 до 90 % пацієнтів з ювенільний дебютом СЧВ мають ураження шкірних покривів і слизових оболонок. «Візитною карткою» СЧВ є еритематозна висипка без свербежу, що злегка піднімається над рівнем шкіри, поширюється на перенісся і нагадує за формою крила метелика, спостерігається у 60–85 % дітей [4, 10]; висипка може захоплювати підборіддя, вушні раковини, але не поширюється на носогубні складки і не призводить до рубцювання. У більше ніж третини хворих подібна висипка фоточутлива і в разі загострення хвороби є передвісником системних проявів. Крім типової еритеми на обличчі, при ювенільному дебюті, на відміну від дорослих пацієнтів, у дітей можуть спостерігатися різноманітні шкірні прояви захворювання. Для дітей і підлітків більш характерне гостре ураження шкіри. Хронічні, дискоїдні ураження в дітей, за даними великого проспективного дослідження, проведеного L. Hiraki та співавт., становлять не більше 10 %, але, на відміну від дорослих, вони дуже часто супроводжуються системними проявами хвороби. Ризик прогресування за наявності дискоїдного вовчака значно вище у дітей, ніж у дорослих (23,5–26 проти 5–10 %).
У дитячому віці також частіше фіксуються зміни, специфічні для СЧВ, тоді як у дорослих частіше спостерігаються неспецифічні прояви хвороби (феномен Рейно — 45 % у дорослих і 12 % у дітей, livedo reticularis — 35 і 12 % відповідно) [6, 12].
Досить часто маніфестація захворювання на СЧВ починається з ураження одного органа чи однієї системи та/або залучення до патологічного процесу одразу декількох органів і систем без певної послідовності, незалежно один від одного та в різні терміни від дебюту. В окремих хворих типові для СЧВ симптоми швидко зникають, а в клінічній картині домінують синдроми, позбавлені нозологічної специфічності. Тривалий час пацієнти з СЧВ можуть мати окремі прояви захворювання, зокрема дискоїдного вовчака, синдрому Рейно, автоімунних гематологічних порушень або епілептиформного, суглобового чи суглобово-м’язового синдромів [2, 7].
Поліморфізм клінічних проявів, нетиповість окремих симптомів у дебюті або наявність спільних клінічних ознак з іншими ревматичними хворобами обумовлюють труднощі та тривалість встановлення діагнозу СЧВ, з огляду на це в світі продовжуються дослідження зі стандартизації підходів до ранньої діагностики захворювання у дітей, що є невід’ємною умовою своєчасного призначення патогенетичної терапії, яка визначає перебіг і прогноз хвороби.
Проблема класифікаційного аналізу СЧВ зі спробою виділити групи хворих, подібних за клінічними проявами, перебігом і наслідками захворювання, завжди залишалась в центрі уваги дитячих ревматологів. Упродовж останніх років діагноз СЧВ встановлювали на підставі даних клінічних, лабораторних та інструментальних досліджень відповідно до класифікаційних критеріїв Американської колегії ревматологів (АCR, 1997), за якою для верифікації вірогідного діагнозу СЧВ враховуються 4 і більше з 11 критеріїв [8]. Однак слід визнати, що застосування цих діагностичних критеріїв не завжди дозволяє діагностувати СЧВ у дебюті захворювання в дитячому віці.
Суворе дотримання кількісної відповідності критеріям ACR призводить до «випадання» хворих із ранніми, ще не повністю сформованими синдромами та/або нетиповою формою хвороби. Різноманітність клінічних проявів і різні ступені їх вираженості, а відповідно, і вибір терапевтичної тактики можуть визначатися проявами, які не увійшли в критерії, що особливо актуально для дитячого віку. У низці випадків хвилеподібність перебігу СЧВ для підтвердження вірогідного діагнозу вимагає спостереження пацієнтів у динаміці. Згідно з дослідженням, проведеним S.M. Benseler та E.D. Silverman, терміни верифікації діагнозу можуть становити від 1 місяця до 3,3 року [3]. На терміни встановлення діагнозу впливає також можливість моноорганного дебюту СЧВ, який спостерігається в більше ніж 20 % випадків. Такі пацієнти протягом тривалого часу спостерігаються у гематологів, нефрологів, неврологів та інших фахівців залежно від ураження тих чи інших органів і систем. На етапі встановлення діагнозу недостатньо вивченою, але прогностично значущою залишається проблема «неповного» вовчака (pre-SLE, preclinical lupus, incomplete lupus erythematosus, latent lupus, lupus-like, probable lupus, undifferentiated connective tissue disease) з наявністю у хворих діагностичних титрів автоантитіл і клінічних ознак, характерних для СЧВ, але недостатніх за кількістю для встановлення діагнозу (менше чотирьох за АCR, 1997), а також у осіб із підвищеним генетичним ризиком розвитку СЧВ, але без будь-яких критеріїв для верифікації діагнозу [3, 9]. У дослідженні G.S. Alarcon та співавт. продемонстровано, що від 15 до 80 % пацієнтів дитячого віку з «неповним» вовчаком у подальшому мають вірогідно встановлений діагноз ще до переходу у дорослий стан [4]. Найчастішими проявами при «неповному» вовчаку є артрити, фотосенсибілізація, висип на вилицях, феномен Рейно, лейкопенія, позитивний антинуклеарний фактор (АNA). Такі пацієнти потребують ретельного клініко-лабораторного моніторингу, виключення дії можливих провокуючих чинників у вигляді інсоляції, стресових ситуацій, вакцинації і, при високих титрах АNA, призначення амінохінолінових препаратів. При розвитку в подальші періоди життя вірогідних ознак СЧВ такі пацієнти мають більш тяжкі необоротні зміни з боку життєво важливих органів і систем та більш тяжкий прогноз захворювання [10, 15].
Водночас у клінічній практиці актуальною залишається проблема гіпердіагностики СЧВ, обумовлена недостатніми знаннями щодо специфічних клінічних проявів захворювання, механічним підходом до набору симптомів, часто розрізнених за часом, — гіперемія шкіри обличчя, поліартралгії, субфебрилітет, втрата маси тіла, кардіалгії, лейкопенія, лейкоцитурія, білок у сечі, наявності у пацієнтів АNA в низьких титрах. Істотним недоліком критеріїв ACR є відсутність стандартизованих вимог до певного набору діагностичних параметрів; наприклад, всі чотири критерії можуть бути тільки клінічними, а імунологічні — відсутні.
Діагностичні критерії СЧВ SLICC (2012) [9, 11] передбачають наявність у хворого клінічних та імунологічних критеріїв (будь-який з наступних лабораторних показників: антитіла до нативної ДНК, АNA, анти-Sm антитіла, антифосфоліпідні антитіла: кардіоліпінові антитіла, вовчаковий антикоагулянт, антитіла проти глікопротеїну-β2, та зниження вмісту в сироватці крові C3, C4 — білків комплементу), але вони не знайшли широкого впровадження в практичній діяльності дитячих ревматологів.
Запропоновані ACR та EULAR (2017) нові критерії для діагностики СЧВ остаточно не затверджені та потребують подальшої валідації.
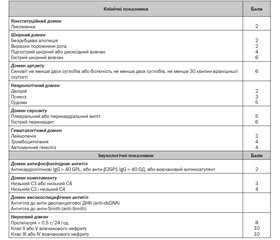
За цими критеріями пацієнти, класифіковані як такі, що мають системний червоний вовчак, повинні мати сироватковий титр антинуклеарних антитіл щонайменше 1 : 80 на людських епітеліальних-2-позитивних (Hep-2) клітинах або еквівалентний позитивний тест. Крім того, пацієнт із підозрою на СЧВ для верифікації діагнозу повинен мати щонайменше 10 балів за клініко-імунологічними критеріями (табл. 1). Критерії не враховуються, якщо вони можуть мати більш вірогідне інше пояснення, ніж захворювання СЧВ. Наявність окремого критерію лише один раз в анамнезі достатньо для того, щоб підрахувати відповідні бали, а час, коли пацієнт позитивний за одним із критерієм, не повинен перетинатися з часом, коли пацієнт позитивний за іншими критеріями. Зазначена класифікація СЧВ вимагає врахування балів щонайменше за одним клінічним показником. Якщо пацієнт позитивний за більше ніж одним показником з домену, то підрахунок проводиться за тим, який має найбільше значення (табл. 1).
/68.jpg)
За останні 10 років у дитячий клініці інституту перебували 22 пацієнти з СЧВ, більшість з них були дівчата (81,8 %). Тривалість спостереження становила від 2 до 6 років, кратність госпіталізації в клініку — від 1 до 3 разів на рік. Дебют захворювання відзначався у віці 11–17 років, тобто у період вікового піка, характерного для розвитку СЧВ. Остаточний діагноз СЧВ встановлено 13 хворим через 1–3,5 року після дебюту захворювання при першому зверненні в клініку інституту, а 7 (28,0 %) пацієнтам — при повторних госпіталізаціях в клініку інституту або в медичні заклади за місцем проживання, у двох дітей термін від дебюту до моменту встановлення діагнозу становив 6 років. У 12 (54,4 %) хворих протягом декількох тижнів (2–4) з моменту появи перших симптомів формувалася полісиндромна клінічна картина із залученням уражень шкіри, суглобів, серозних оболонок, периферичної нервової системи, у 2 хворих — нирок, у 1 — печінки та кишечника.
В дебюті СЧВ у цих дітей переважали підгострий або гострий початок хвороби з високою частотою лихоманки, ураження шкіри, суглобів, у багатьох випадках у патологічний процес залучались серозні оболонки, серце, нирки, судинна і периферична нервова системи. Спостерігались поодинокі випадки ураження печінки, шлунково-кишкового тракту, розвиток антифосфоліпідного синдрому.
У 8 (36,4 %) дітей в початковому періоді та протягом досить тривалого часу в подальшому (1–2,5 року) домінували ознаки тільки одного з синдромів: шкірного (2 дітей), представленого у формі метелика на обличчі, який посилювався у весняно-літній період на тлі інсоляції, та/або судинного синдрому (Рейно), суглобового синдрому (6 дітей) з ураженням периферичних суглобів із наявністю больових і стійких ексудативних проявів. У 3 (13,6 %) дівчат в дебюті хвороби спостерігались здебільшого шкірно-суглобово-м’язові симптоми, короткочасна лейкопенія, незначно виражені ознаки залучення в патологічний процес периферичної нервової системи. При такому дебюті хвороби досить часто встановлюються помилкові діагнози (алергічний дерматит, синдром Рейно, ювенільний ревматоїдний артрит, реактивний артрит) або недиференційованого захворювання сполучної тканини, що відтерміновує початок патогенетичного лікування.
Наводимо клінічні спостереження пацієнтів, які мали особливості дебюту і труднощі встановлення діагнозу з СЧВ.
Клінічний випадок 1. Хворий хлопчик К., 15 років, спостерігався в інституті протягом 5 років. Анамнез життя без особливостей. Ріс та розвивався відповідно до віку. Профілактичні щеплення згідно з календарем щеплень. Медикаментозну та харчову алергію у дитини батьки заперечують. Переніс вітряну віспу у 3 роки. Із сімейного анамнезу: у бабусі ревматоїдний артрит. З анамнезу захворювання відомо, що протягом 6 місяців хлопчик скаржився на біль у ліктьових суглобах, набряк та локальне підвищення температури, що було розцінено як післятравматичне ураження. Після підвищеної інсоляції з’явилися вперше гіперемовані плями, що виступали над поверхнею шкіри на обличчі, повіках, плечах, спині та зникали на короткий час після застосування гормонального крему. У дитини також періодично відзначались підйоми температури до субфебрильних цифр. При стаціонарному обстеженні за місцем проживання встановлено діагноз: «системний васкуліт, ANA позитивний». Отримував дексаметазон, розпочато терапію плаквенілом, після чого стан дитини покращився. Через 3 місяці після самостійної відміни призначеного лікування у дитини була помічена виражена слабкість, посилились артралгії, больові контрактури ліктьових суглобів, міалгії, з’явився висип на обличчі, еритематозні плями на кінцівках. Хворий схуднув на 2 кг. Для уточнення діагнозу хлопчик був направлений в інститут із діагнозом «системне захворювання сполучної тканини (дерматоміозит?)».
При надходженні загальний стан середньотяжкий. Відзначались скарги на артралгії, міалгії, артрит і згинальні контрактури ліктьових суглобів. На верхніх і нижніх повіках, на правому плечі візуалізувались еритематозні плями округлої форми, підвищені над поверхнею шкіри, з лущенням, долонний капілярит, ознаки хейліту, збільшені шийні регіональні лімфатичні вузли. Тони серця звучні, ритмічні, ясні, вислуховувався м’який систолічний шум. Проводилась диференціальна діагностика між ювенільним ідіопатичним артритом, дерматоміозитом, СЧВ.
При обстеженні: Hb — 128 г/л, ер. — 5,0 × 1012/л, лейк. — 5,6 × 109/л, тромб. — 310 × 109/л, ШОЕ — 10 мм/год, е. — 4 %, п. — 3 %, с. — 50 %, л. — 37 %, м. — 6 %. Біохімічне дослідження крові: білок — 64,4 г/л, альбумін — 52,4 г/л, α1-глобулін — 9,3 %, α2-глобулін — 9,3 %, β-глобулін — 12,6 %, γ-глобулін — 18,6 %, А/Г коеф. — 1,12, СРБ — 14 мг/л, білірубін — 8,2 мкмоль/л, тимолова проба — 2,6 Од., ЛФ — 200,0 Од/л, АЛТ — 15 Од/л, АСТ — 18 Од/л, сечовина — 4,38 мкмоль/л, креатинін — 66 мкмоль/л, креатинфосфокіназа — 82 Од/л (норма), фібриноген загальний — 4,42 г/л, фібриноген В (+), глюкоза — 4,06 ммоль/л, вітамін D — 52,6 нг/мл. Імунологічне дослідження крові: IgG — 17,2 г/л (норма 7,7–15,1 г/л), ІgА — 1,47 г/л (норма 1,0–3,3 г/л), ІgМ — 0,45 г/л (норма 0,7–2,0 г/л), ЦІК — 0,013 г/л (норма < 0,025 г/л), AНA — (3+), титр — 1 : 320, тип — гомогенний, Sm-антитіла IgG > 8 (позитивний результат), Sm/RNP, антитіла IgG-7 (позитивний результат); RNP, антитіла IgG > 8 (позитивний результат), Smith-антиген — 65,5 (норма < 15,0); антитіла до одноланцюгової ДНК — 1,2 (норма < 1,1), антитіла до дволанцюгової ДНК — 0,9 (норма < 1,0); антикардіоліпінові IgM GPL — 12,0 (норма < 10), антифосфатидил-серинові IgM — 22,3 U/ml (норма < 10 U/ml), антифосфатидил-етаноламінові IgM — 14,0 U/ml (норма < 12 U/ml), РФ і АССР негативні. Дитині проведена електроміографія (ЕМГ): швидкість проведення збудливості по нервах верхніх кінцівок, сила скорочення дистальних м’язів у межах норми, ЕМГ-ознаки зниження функції периферичних нервів (поліневропатії, супутні тунельні синдроми) не виявлено. За даними голчастої ЕМГ поточних гострих денерваційних змін не виявлено. У проксимальних м’язах верхніх кінцівок відзначається помірне зниження параметрів потенціалів рухових одиниць у вигляді зменшення середньої тривалості, поліфазія потенціалів (переважно в правому дельтаподібному). Висновок: відсутні ознаки поточного запального процесу в м’язах, зниження середньої ПДЕ в проксимальних м’язах і перебудова потенціалів може бути проявом міогенних змін.
ЕКГ: синусова аритмія, неповна блокада правої ніжки пучка Гіса. ЕхоКГ: ПМК І ст., гемодинамічно незначний. Спірографія: функція зовнішнього дихання не порушена.
УЗД ліктьових суглобів: синовіт ліктьових суглобів справа не визначається; зліва — незначний; висота по передній поверхні 3 мм. Незначна кількість ексудату по латеральних поверхнях обох ліктьових суглобів. По задній поверхні ліктьового суглоба ексудату не визначається. Васкуляризація не посилена. Латеральна та медіальна колатеральні зв’язки без особливостей з обох боків. Суглобові поверхні плечової та ліктьової кісток без особливостей. Товщина хрящового шару — до 1–3 мм, без дефекту. УЗ-ознаки відповідають ексудативному синовіту лівого ліктьового суглоба. МРТ суглобів: ознаки хронічного бурситу підшкірно слизової сумки ліктьового відростку зліва; синовіт лівого ліктьового суглоба; зона набряку в ліктьовому відростку лівої ліктьової кістки.
Проведене патогістологічне дослідження біоптату шкіри: в епідермісі явища вогнищевого гіперкератозу і гіпотрофії, помірного акантозу, що чергуються з ділянками потоншення надсосочкових ділянок мальпігієвого шару; в базальних клітинах вогнищева вакуольна дистрофія. У сосочковому та сітчастому шарах дерми явища дезорганізації сполучної тканини, дрібновогнищеві лімфо-макрофагальні інфільтрати, помірні явища мікроваскуліту. Відзначається вогнищева атрофія придатків шкіри. Висновок: морфологічна картина в наданих препаратах відповідає системному захворюванню сполучної тканини з наявністю васкуліту.
На основі даних анамнезу (суглобовий синдром, фотосенсибілізація), клінічного (фіксована еритема, еритематозний висип, капілярит, хейліт, артрит) і лабораторного обстеження (збільшення рівня анти-ДНК, позитивний тест на АNA, наявність антифосфоліпідних антитіл, Sm-антитіл) та результатів патогістологічних досліджень біоптату шкіри хворому вперше встановлено діагноз: «системний червоний вовчак, хронічний перебіг: синдром дискоїдного вовчака, фотосенсибілізація, артрит ліктьових суглобів, активність 1 (SLEDAI — 29 балів)». Призначено лікування: плаквеніл, моваліс, гормональні мазі на елементи висипу, омепразол; кальцемін. Стан дитини нормалізувався, досягнута клініко-лабораторна ремісія.
Цей приклад демонструє, що діагноз СЧВ був встановлений хворому лише через 9 місяців від початку хвороби, незважаючи на неухильне прогресування суглобового синдрому, приєднання шкірних проявів вовчака та фотосенсибілізаії. Відповідно до нових діагностичних критеріїв у дитини вже під час першої госпіталізації за місцем проживання можна нарахувати до 10 балів, що дозволило б запідозрити СЧВ та призначити специфічне імунологічне дообстеження.
Клінічний випадок 2. Хвора дівчина А., 17 років, спостерігається в інституті протягом останніх двох років. Дебют захворювання у віці 15 років розпочався з висипки на обличчі, тулубі, кінцівках та фотосенсибілізації. За місцем проживання встановлено діагноз алергічного дерматиту, призначено елімінаційну дієту, антигістамінні препарати, ентеросорбенти; позитивного ефекту не було досягнуто. Через 3 місяці влітку після тривалої інсоляції стан прогресивно погіршився, з’явилися лихоманка (до 39 оС), головний біль, підвищення артеріального тиску до 160/120 мм рт.ст., періодична набряклість обличчя, гомілок, прогресування висипки на шкірі, бульозний дерматит шкіри на грудній клітці, випадіння волосся, стоматит, хейліт, артрит колінних і дрібних суглобів кистей, стоп, втрата маси тіла до 10 кг. Через 5 місяців від початку перших симптомів за місцем проживання в крові виявлено: ШОЕ — 77 мм/год,
лейкопенія (2,55 × 109/л), анемія (еритроцити — 2,85 × 1012/л, гемоглобін — 76 г/л), тромбоцитопенія (145 × 109/л), позитивні антинуклеарні антитіла (АНА), антитіла до двоспіральної ДНК, Sm-антитіла та зміни в аналізах сечі (мікроеритроцитурія, мікропротеїнурія). На підставі сукупності результатів клінічного та лабораторного обстеження діагностовано СЧВ, призначено преднізолон 60 мг на добу. Незважаючи на призначену терапію, відзначалось прогресування хвороби, і через 6 місяців від початку захворювання дитина була направлена до інституту.
З анамнезу життя відомо, що дитина народилась від першої нормальної вагітності, фізіологічних пологів, доношена. Щеплення за календарем. Часто хворіла на застудні захворювання. Спадковий анамнез має певні особливості, а саме: бабуся по лінії матері хворіє на гормонозалежну бронхіальну астму, у матері — розсіяний склероз.
Стан при госпіталізації тяжкий. Температура — до 39 оС, ЧСС — 120 уд/хв, ЧД — 26 уд/хв, артеріальний тиск — 160/120 мм рт.ст. Дівчина бліда, млява; виражена слабкість, скаржиться на міалгії, біль в гомілковостопних, променезап’ясткових, ліктьових, плечових, скронево-нижньощелепному суглобах. На шкірі обличчя, грудей, над суглобами — еритематозна висипка з елементами некрозу, виразками, кров’янистими кірками, синдром Рейно, вогнищева алопеція, хейліт. На слизовій оболонці порожнини рота — прояви афтозно-некротичного та ангулярного стоматиту, гінгівіту з елементами кандидозного ураження. Мають місце набряк і дефігурація колінних, дрібних суглобів кистей і стоп, невиражена пастозність гомілок. Полінейропатія. Перкуторно над легенями відзначався легеневий звук із притупленням у задньонижніх відділах, аускультативно — жорстке дихання. Межі відносної серцевої тупості розширені в поперечнику, аускультативно серцеві тони приглушені, аритмічні, вислуховується систолічний шум на верхівці, в V точці. Живіт при пальпації безболісний, пастозність передньої черевної стінки, пупок помітно згладжений. Печінка виступала з-під краю реберної дуги на 3,5 см, селезінка — на 1,5 см. Випорожнення зі схильністю до запорів. Діурез до 1000 мл на добу.
При обстеженні: в загальному аналізі крові — анемія (еритроцити — 2,81 × 1012/л, гемоглобін — 80 г/л), лейкопенія (3,55 × 109/л), тромбоцитопенія (125 × 109/л), ШОЕ — 58 мм/год. Час та тривалість кровотечі: початок — 41´05´´, кінець — 5´40´´, тривалість — 1´35´´. Ретикулоцити — 40,00 % (норма 2,0–12,0 %), феритин — 142,1 нг/мл (норма 20–200 нг/мл), залізо сироваткове — 17,30 мкмоль/л (норма 5,90–18,30 мкмоль/л), загальне залізо — 26,60 мкмоль/л (норма 41,0–77,0 мкмоль/л), коефіцієнт насичення трансферином — 0,05 г/л (норма 0,10–0,40 г/л). Біохімічне дослідження крові: загальний білок — 56,4 г/л, білірубін — 7,0 мкмоль/л, холестерин — 4,98 ммоль/л, тимолова проба — 1,2 Од, АЛТ — 19 Од/л, АСТ — 24 Од/л, сечовина — 8,95 мкмоль/л, креатинін — 0,115 мкмоль/л, глюкоза — 5,44 ммоль/л, креатинінкіназа — 154,0 Од/л (норма 15,0–123,0 Од/л), тропонін Т (високочутливий) < 0,003 нг/мл (норма 0,00–0,03 нг/мл), 25(OH) — 27,13 нг/мл (недостатній рівень). Коагулограма: фібриноген — 4,42 г/л, протромбіновий індекс — 71 %, фібрин — 32 мг, МНО — 0,91 %, фібриноген В (++). Протеїнограма: загальний білок — 57,3 г/л, альбумін — 36,55 г/л, α1-глобулін — 7,49 %, α2-глобулін — 13,42 %, β-глобулін — 15,30 %, γ-глобулін — 27,25 %, А/Г коефіцієнт — 0,6. Тиреоїдні гормони: ТТГ — 3,1 мМО/л (норма 0,17–4,05 мМО/л), Т4 — 98,9 нмоль/л (норма 60–160 нмоль/л), анти-ТПО — 77,2 МО/мл (норма до 20 МО/мл).
При дослідженні загального аналізу сечі в динаміці встановлені коливання питомої ваги (1015–1022), білка (0,5–0,7) г/л, лейкоцитів (12–15 в полі зору), змінених та вилужених еритроцитів (все поле зору), гіалінових циліндрів (2–3 в полі зору). Креатинін у сечі — 2,2 ммоль/л, швидкість клубочкової фільтрації — 109 мл/хв. Аналіз сечі за Зимницьким: коливання денної кількісті — 220–600 мл, нічної — 320–420 мл, питомої ваги — 1010–1020. В добовій сечі: білок — 0,5–0,7 г/л. Аналіз сечі за Нечипоренком: лейкоцити — 12500–8000 в 1 мл, еритроцити — все поле зору, змінені та частково вилужені. Посів сечі на флору — росту немає.
Субпопуляції лімфоцитів: лімфоцити — 29,36 % (норма 35–55 %), 2450 мкл (норма 1100–5900 мкл); Т-лімфоцитів — 81,9 % (норма 55–75 %), 2005/мкл (норма 700–4200/мкл); Т-хелпери (CD3+, CD4+) — 47,18 % (норма 30–55 %), 1156/мкл (норма 300–1800/мкл); Т-цитотоксини (CD3+, CD8+) — 34,42 % (норма 12–30 %), 843/мкл (норма 200–700/мкл); Тх-Тц-співвідношення — 1,37 (норма 1,0–2,5); В-лімфоцити (CD19+) — 15,74 % (норма 10–25 %); NK-лімфоцити — 1,54 % (норма 5–17 %), 38/мкл (норма 90–900/мкл). HCT-тест: спонтанний — 7 % (норма 5–12 %), стимульований — 14 %, функціональний резерв — 7 %. Фагоцитоз: активність — 15 % (норма 50–90 %), інтенсивність — 5,0 (норма 4–15). Імунограма: IgG — 12,4 г/л (норма 7,7–15,1 г/л), ІgА — 2,9 г/л (норма 1,0–3,3 г/л), ІgМ — 1,7 г/л (норма 0,7–1,5 г/л), ЦІК — 0,150 г/л (норма < 0,025 г/л). Комплемент С3 — 0,57 г/л (норма 0,90–1,80 г/л). Антифосфоліпідні антитіла: антикардіоліпінові aCL IgG — 20,8 U/ml (норма < 10 U/ml), антифосфатидил-серинові aPS IgG — 22 U/ml (норма < 10 U/ml), антифосфатидил-етаноламінові aPE IgG — 14,1 U/ml (норма < 12 U/ml). Антинуклеарні антитіла (АНА) — 1 : 1000, антитіла до одноланцюгової ДНК — 2,6 (норма до 1,1), антитіла до дволанцюгової ДНК — 1,9 (норма до 1,1). Вовчаковий антикоагулянт — позитивний.
ЕКГ: синусовий ритм, неповна блокада правої ніжки пучка Гіса, метаболічні зміни міокарда. ЕхоКГ: клапанний апарат без особливостей, розміри порожнин серця не збільшені, гіпертрофії стінок міокарда не виявлено, скоротливість міокарда помірно знижена (ФВ — 51 %), рідина в перикарді. УЗД органів черевної порожнини: дифузні зміни паренхіми печінки, реактивні зміни підшлункової залози, мінімальна кількість вільної рідини в плевральній порожнині, в ділянці малого таза. УЗД суглобів: ексудативний синовіт колінних, гомілковостопних, кульшових, ліктьових суглобів, міжфалангових суглобів кистей та стоп. УЗД щитоподібної залози: дифузне збільшення розмірів щитоподібної залози. Рентгенографія органів грудної порожнини: розширення меж серця в поперечнику, посилення інтерстиціального рисунка легень.
З урахуванням спадкового анамнезу (наявність родичів по материнській лінії з автоімунними захворюваннями), анамнезу захворювання, даних клінічного та лабораторного обстеження у дитини діагностовано: СЧВ, підгострий перебіг, з ураженням шкіри і слизових оболонок («метелик», алопеція, афтозний стоматит, бульозний дерматит, панікуліт); синдром Рейно; ураження суглобів (поліартрит), легень (пульмоніт), серця (кардит), нирок (вовчаковий гломерулонефрит), нервової системи (полінейропатія); полісерозити; лейкопенію; тромбоцитопенію; автоімунний гемоліз та імунологічні порушення (підвищення антитіл до нативної ДНК, позитивні Sm-антитіла, АNА, зниження комплементу С3); високий ступінь активності (SLEDAI — 65 балів).
Була проведена індукційна терапія, що включала високодозну глюкокортикоїдну (солумедрол) і цитостатичну (циклофосфамід) терапію, — пульс-терапія 1 раз на місяць протягом 6 місяців, антикоагулянти, дезагреганти, блокатори АПФ. Після завершення пульс-терапії дівчина продовжувала отримувати ГК-терапію per os з поступовою відміною до підтримуючої дози, ендоксан, лізиноприл, плаквеніл, вітамін D. У стані медикаментозної стабілізації хвороби передана під нагляд дорослих кардіоревматологів.
У цьому випадку підгострий розвиток СЧВ дебютував зі шкірного синдрому, фотосенсибілізації. Однак навіть після прогресуючого погіршення стану дитини (втрата маси тіла, фебрильна лихоманка, головний біль, підвищення артеріального тиску, збільшення вогнищ висипки на шкірі з бульозним дерматитом, випадіння волосся, стоматит, хейліт, артрит колінних і дрібних суглобів кистей, стоп) діагноз не був запідозреним, а лише після залучення до патологічного процесу життєво важливих органів (нирок, серця), появи показників лабораторної активності через 5 місяців від перших симптомів проведено імунологічне дообстеження та діагностовано СЧВ. Відповідно до нових критеріїв діагностики вже через 3 місяці від дебюту захворювання у пацієнтки можна було нарахувати 16 балів тільки за клінічними критеріями та верифікувати СЧВ. Більш рання діагностика та лікування дозволили б запобігти прогресуванню й генералізації хвороби із залученням до патологічного процесу життєво важливих органів (нирок, легенів, серця), що потребувало агресивної терапії, та уникнути тяжкого необоротного органного ушкодження і досягти в більш короткі терміни неактивної фази захворювання.
Висновки
Досвід дитячої клініки ДУ «ІПАГ ім. акад. О.М. Лук’янової НАМН України» і наведені випадки свідчать про те, що системний червоний вовчак у дітей — захворювання з гетерогенною клінічною картиною, особливостями дебюту, прогресування та прогнозу, що потребує всебічного клінічного, лабораторного, інструментального обстеження хворих, кваліфікованого та персоніфікованого підходів до оцінки його результатів з метою більш ранньої діагностики та своєчасного призначення адекватного лікування.
Більш агресивний перебіг СЧВ у дітей і підлітків як у самому дебюті, так і з плином часу призводить до більшої частоти органних ушкоджень. Своєчасна діагностика з визначенням активності й варіанту перебігу хвороби та призначенням адекватної терапії сприяє запобіганню генералізації процесу із залученням життєво важливих органів, мінімізації ускладнень у пацієнтів, їх інвалідизації, збільшенню тривалості та поліпшенню якості життя.
Діагностика СЧВ у дебюті в дітей до цього часу певною мірою є складною як для сімейного лікаря, педіатрів, так і для дитячих ревматологів. Застосування нових діагностичних критеріїв дозволяє встановити діагноз у більш ранні терміни захворювання та розпочати патогенетичну терапію.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.

/68.jpg)