Журнал «Здоровье ребенка» Том 15, №2, 2020
Вернуться к номеру
Экспресс-метод для определения вероятности развития врожденной пневмонии у доношенных новорожденных
Авторы: Горячко А.Н., Сукало А.В.
Белорусский государственный медицинский университет, г. Минск, Беларусь
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
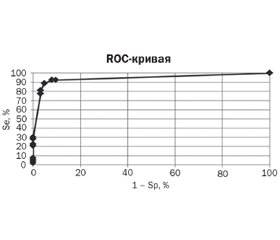
За даними Всесвітньої організації охорони здоров’я, в 2017 році в усьому світі від пневмонії померло 15 % дітей віком молодше п’яти років. Мета дослідження: розробка математичної моделі для визначення ймовірності розвитку вродженої пневмонії у доношених новонароджених експрес-методом. Проведено комплексне обстеження 116 доношених новонароджених, які перебували в педіатричному відділенні для новонароджених дітей та пологовому фізіологічному відділенні Державної установи «Республіканський науково-практичний центр «Мати і дитя» в період з 2017 по 2019 рік. Проведено порівняльний аналіз 174 даних анамнезу життя, результатів попередніх вагітностей, ускладнень справжньої вагітності у матерів, клінічних і рутинних лабораторних методів дослідження у новонароджених на 1-шу — 2-гу добу життя. В подальшому визначено найбільш значущі фактори, асоційовані з розвитком вродженої пневмонії у доношених новонароджених. На підставі бінарної логістичної регресії та ROC-аналізу проведено математичний аналіз 387,4 млн зв’язків змінних. Внаслідок проведеного обстеження встановлено найбільш значущі фактори, асоційовані з розвитком вродженої пневмонії у доношених новонароджених: з акушерсько-гінекологічного та соматичного анамнезу життя матері — мимовільний викидень; з ускладнень вагітності — хронічна внутрішньоматкова гіпоксія плода і хронічна фетоплацентарна недостатність; за результатами клінічних проявів у першу добу життя — наявність дихальної недостатності. На підставі отриманих даних розроблена модель з чутливістю 90,6 %, специфічністю 92,1 % і площею під ROC-кривою AUC = 0,93 ± 0,054, р < 0,001 (95% довірчий інтервал 0,88–0,98). За допомогою прогностичної моделі розраховано порогові значення: для мимовільного викидня — 0,836; хронічної внутрішньоматкової гіпоксії плода — 0,537; хронічної фетоплацентарної недостатності — 0,533; наявності дихальної недостатності — 0,939, що при порогових значеннях ≥ 0,53 ROC-кривої дозволяє виділити групу високого ризику з розвитку вродженої пневмонії серед доношених новонароджених. З діючою математичною моделлю для визначення ймовірності розвитку вродженої пневмонії у доношених новонароджених експрес-методом можна ознайомитися на сайті http://pneu.bsmu.by або https://www.bsmu.by (внизу сторінки меню «Лікар/провізор: діагностика вродженої пневмонії»).
По данным Всемирной организации здравоохранения, в 2017 году во всем мире от пневмонии умерло 15 % детей в возрасте младше пяти лет. Цель исследования: разработка математической модели для определения вероятности развития врожденной пневмонии у доношенных новорожденных экспресс-методом. Проведено комплексное обследование 116 доношенных новорожденных, находившихся в педиатрическом отделении для новорожденных детей и родильном физиологическом отделении Государственного учреждения «Республиканский научно-практический центр «Мать и дитя» в период с 2017 по 2019 год. Произведен сравнительный анализ 174 данных анамнеза жизни, исходов предыдущих беременностей, осложнений настоящей беременности у матерей, клинических и рутинных лабораторных методов исследования у новорожденных на 1–2-е сутки жизни. В последующем определены наиболее значимые факторы, ассоциированные с развитием врожденной пневмонии у доношенных новорожденных. На основании бинарной логистической регрессии и ROC-анализа проведен математический анализ 387,4 млн связей переменных. В результате проведенного обследования установлены наиболее значимые факторы, ассоциированные с развитием врожденной пневмонии у доношенных новорожденных: из акушерско-гинекологического и соматического анамнеза жизни матери — самопроизвольный выкидыш; из осложнений беременности — хроническая внутриматочная гипоксия плода и хроническая фетоплацентарная недостаточность; по результатам клинических проявлений в первые сутки жизни — наличие дыхательной недостаточности. На основании полученных данных разработана модель с чувствительностью, равной 90,6 %, специфичностью — 92,1 % и площадью под ROC-кривой — AUC = 0,93 ± 0,054; р < 0,001 (95% доверительный интервал 0,88–0,98). С помощью прогностической модели рассчитаны пороговые значения: для самопроизвольного ± выкидыша — 0,836; хронической внутриматочной гипоксии плода — 0,537; хронической фетоплацентарной недостаточности — 0,533; наличия дыхательной недостаточности — 0,939, что при пороговых значениях ≥ 0,53 ROC-кривой позволяет выделить группу высокого риска по развитию врожденной пневмонии среди доношенных новорожденных. С действующей математической моделью для определения вероятности развития врожденной пневмонии у доношенных новорожденных экспресс-методом можно ознакомиться на сайте http://pneu.bsmu.by или https://www.bsmu.by (внизу страницы меню «Врач/провизор: диагностика врожденной пневмонии»).
According to the World Health Organization, 15 % of children under the age of five died of pneumonia worldwide in 2017. Objective: to create a mathematical model for determining the probability of developing congenital pneumonia in full-term newborns using the express method. A comprehensive examination was conducted in 116 full-term newborn infants, who were admitted to pediatric ward for newborn children and maternity physiological department of the State Institution “Republican Scientific Practical Center “Mother and Child” during the period from 2017 to 2019. A comparative analysis of 174 life history data, outcomes of previous pregnancies, complications of current pregnancy in mothers, clinical and routine laboratory methods used in newborns on day 1–2 of life was performed. Subsequently, the most significant factors associated with the development of congenital pneumonia in full-term newborns were determined. Based on binary logistic regression and receiver operating characteristic (ROC) analysis, a mathematical analysis of 387.4 million variable relationships was performed. The survey determined the most significant factors associated with the development of congenital pneumonia in full-term newborns: from the past obstetric-gynecologic and somatic history of the mother — a spontaneous abortion; complications of pregnancy — chronic intrauterine fetal hypoxia and chronic fetoplacental insufficiency; the results of clinical manifestations in the first days of life — the presence of respiratory failure. Based on the obtained data, a model was developed with a sensitivity of 90.6 %, specificity of 92.1 % and the area under the ROC curve = 0.930 ± 0.054, p < 0.001 (95% confidence interval 0.88–0.98). Threshold values were calculated using a predictive model: for spontaneous abortion — 0.836; for chronic intrauterine fetal hypoxia — 0.537; for chronic fetoplacental insufficiency — 0.533; the presence of respiratory failure — 0.939, which at threshold values of ≥ 0.53 of the ROC curve makes it possible to identify a group at high risk of developing congenital pneumonia among full-term newborns. The current mathematical model for determining the probability of developing congenital pneumonia in full-term newborns using the express method can be found on the website http://pneu.bsmu.by or https://www.bsmu.by (at the bottom of the page, there is Doctor/Pharmacist: Diagnosis of Congenital Pneumonia menu).
модель; фактори ризику; доношені новонароджені; вроджена пневмонія
модель; факторы риска; доношенные новорожденные; врожденная пневмония
model; risk factors; full-term newborns; congenital pneumonia
Введение
Материалы и методы
Результаты и обсуждение
/78_2.jpg)
Выводы
1. Пневмония. Информационный бюллетень ВОЗ. 2 августа 2019 [Электронный ресурс]. Режим доступа: https://www.who.int/ru/news-room/fact-sheets/detail/pneumonia. Дата доступа: 27.02.2020.
2. Основные показатели здоровья матери и ребенка, деятельность службы охраны детства и родовспоможения в Российской Федерации за 2018 год. [Электронный ресурс]. Режим доступа: https://www.rosminzdrav.ru/ministry/61/22/stranitsa-979/statisticheskie-i-informatsionnye-materialy/statisticheskiy-sbornik-2018-god. Дата доступа: 14.01.2020.
3. Врожденная пневмония (клинические рекомендации). А.Г. Антонов, Е.Н. Байбарина, Е.Н. Балашов, В.В. Зубков, Д.О. Иванов, О.В. Ионов [и др.] [под ред. Д. Д. Дегтярева]. Неонатология. Новости, мнения, обучение. Журнал для непрерывного медицинского образования врачей. М.: ГЭОТАР-Медиа, 2017. № 4 (18). С. 133-148.
4. Bhutta Z.A. Interventions to address deaths from childhood pneumonia and diarrhoea equitably: what works and at what cost? The Lancet. 2013. № 9875. P. 1417-1429.
5. Косьянчук А.В. Инфекционный фактор у женщин с неразвивающейся беременностью и хроническим эндометритом. Материалы Х Съезда акушеров-гинекологов и неонатологов Республики Беларусь, Минск, 9–10 ноября 2017 г. Репродуктивное здоровье. Восточная Европа. 2017. № 5. С. 791-795.
6. Gill C.J. Bottlenecks, barriers, and solutions: results from multicountry consultations focused on reduction of childhood pneumonia and diarrhoea deaths. The Lancet. 2013. № 9876. P. 1487-1498.
7. Можейко Л.Ф. Невынашивание беременности: учеб.-метод. пособие. Минск: БГМУ, 2013. 38 с.
8. McGuire W. Infection in the preterm infant. BMJ. 2004. Vol. 2. P. 329-341.
9. Мудров В.А. Возможности модификации способов определения объема околоплодных вод. Журнал акушерства и женских болезней. 2016. № 34. С. 12-17.
10. Малевич Ю.К. Фетоплацентарная недостаточность Минск: Беларусь, 2007. 157 с.
11. Савельева Г.М., Федорова М.В., Клименко П.А. и др. Плацентарная недостаточность. М.: Медицина, 1991. 272 с.
12. Тютюнник В.Л. Хроническая плацентарная недостаточность при бактериальной и вирусной инфекции (патогенез, диагностика, профилактика, лечение): автореф. дис. … д-ра мед. наук. В.Л. Тютюнник. М., 2002. 46 с.
13. Александрович А.С. Макроскопические и микроскопические особенности плаценты у беременных с фетоплацентарной недостаточностью. Современные перинатальные медицинские технологии в решении проблем демографической безопасности: сб. науч. тр. Министерства здравоохранения Республики Беларусь, Республиканский научно-практический центр «Мать и дитя»; редкол.: Е.А. Улезко, И.В. Курлович. Минск, 2019. Вып. 12. С. 16-22.
14. Анистратов С.В. Хламидийная инфекция и ее роль в патологии плаценты: автореф. дис. … канд. мед. наук: 14.00.15. Анистратов Сергей Владимирович. Волгогр. мед. акад. Волгоград, 2001. 23 с.
15. Володин Н.Н. Детские болезни. Т. 1. Неонатология. [Под ред. Н.Н. Володина, Ю.Г. Мухиной, А.И. Чубаровой]. М.: Династия, 2011. 512 с.
16. Шабалов Н.П. Неонатология: учеб. пособие в 2 т. Т. I. 3-е изд., испр. и доп. М.: МЕДпресс-информ, 2004. 608 с.
17. Сукало А.В. Справочник по поликлинической педиатрии. Национальная академия наук Беларуси. Минск: Беларуская навука, 2015. 313 с.
18. Рооз Р. Практические рекомендации: пер. с нем.; ред. пер.: Р. Вауэр, Г.А. Шишко. М.: Медицинская литература, 2011. 592 с.
19. Дмитриев В.В. Практические вопросы клинической коагулологии. Минск: Беларуская навука, 2017. 278 с.
20. Зубовская Е.Т. и др. Диагностическое значение лабораторных показателей: практ. пособие. Респ. науч.-практ. центр «Мать и дитя». Бел. мед. акад. последиплом. образования. 3-е изд., доп. Минск: БГУФК, 2013. 421 с.
21. Горячко А.Н. Прогностическая модель для определения вероятности развития врожденной пневмонии у доношенных новорожденных. Здоров’я дитини. 2019. Т. 14. № 4. С. 256-261.

/75.jpg)
/77.jpg)
/78.jpg)