Журнал «Здоровье ребенка» Том 15, №3, 2020
Вернуться к номеру
Нова парадигма порушення росту у хворих на ювенільний ідіопатичний артрит
Авторы: Марушко Т.В., Голубовська Ю.Є.
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
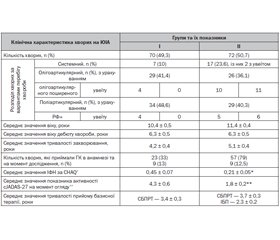
Актуальність. Фізичний розвиток може порушуватися при ювенільному ідіопатичному артриті (ЮІА). Причини порушення росту при ЮІА залежать від комплексу чинників, що пов’язані як з конституційно-генетичними особливостями дитячого організму, так і з патогенетичними механізмами захворювання та отримуваною терапією. Мета дослідження: оцінити показники фізичного розвитку хворих на ЮІА залежно від різних лікувальних режимів для визначення факторів, що впливають на його порушення, з метою розробки рекомендацій, спрямованих на профілактику порушення росту у даної категорії дітей. Матеріали та методи. Оцінено дані антропометрії (ріст за коефіцієнтом стандартного відхилення (Standart Deviation Score — SDS)), показник швидкості росту за попередній рік у 142 хворих на ЮІА, у частини дітей — дані динамометрії. Порівняння отриманих результатів проведено з використанням як параметричних (t-критерій Стьюдента), так і непараметричних (U-критерій Манна — Уїтні) методів, а кореляційний зв’язок між показниками вивчено з використанням множинного регресійного аналізу. Результати. Під час дослідження в жодної дитини з олігоартикулярним варіантом перебігу ЮІА відхилень у рості не виявлено. У 12 пацієнтів (8,5 %) з обох груп виявлено порушення фізичного розвитку (показник росту менше за –1 SD): у 1/2 випадків — при системній формі хвороби (6), в іншої половини — при поліартикулярній (6). При використанні в схемі лікування імунобіологічних препаратів відносна швидкість росту є вірогідно вищою в пацієнтів як з олігоартикулярною (U = 225,5, р = 0,009), так і з поліартикулярною (U = 222,5, р = 0,0001) формами хвороби. Згідно з множинним регресійним аналізом, чим більший сумарний показник активності хвороби, тим більшою є затримка у швидкості зростання та рості. Діти з поліартикулярним (49,0 %) та системним (54,5 %) варіантами перебігу ЮІА мають порушення м’язової сили. Висновки. Виявлення порушення росту є основою для поглибленого обстеження та перегляду терапії хворих на ЮІА. Ступінь активності хвороби впливає на показники росту.
Актуальность. Физическое развитие может нарушаться при ювенильном идиопатическом артрите (ЮИА). Причины нарушения роста при ЮИА зависят от комплекса факторов, связанных как с конституционно-генетическими особенностями детского организма, так и с патогенетическими механизмами заболевания и получаемой терапией. Цель исследования: оценить показатели физического развития больных ЮИА в зависимости от различных лечебных режимов для определения факторов, влияющих на его нарушение, с целью разработки рекомендаций, направленных на профилактику нарушения роста у данной категории детей. Материалы и методы. Оценены данные антропометрии (рост по коэффициенту стандартного отклонения (Standard Deviation Score — SDS)), показатель скорости роста за предыдущий год у 142 больных ЮИА, у части детей — данные динамометрии. Сравнение полученных результатов проведено с использованием как параметрических (t-критерий Стьюдента), так и непараметрических (U-критерий Манна — Уитни) методов, а корреляционная связь между показателями изучена с использованием множественного регрессионного анализа. Результаты. В ходе исследования ни у одного ребенка с олигоартикулярным вариантом течения ЮИА отклонений в росте не было обнаружено. У 12 пациентов (8,5 %) из обеих групп выявлены нарушения физического развития (показатель роста меньше –1 SD): в 1/2 случаев — при системной форме болезни (6), у другой половины — при полиартикулярной (6). При использовании в схеме лечения иммунобиологических препаратов относительная скорость роста достоверно выше у пациентов как с олигоартикулярной (U = 225,5, р = 0,009), так и с полиартикулярной (U = 222,5, р = 0,0001) формами болезни. Согласно результатам множественного регрессионного анализа, чем выше суммарный показатель активности болезни, тем больше задержка в скорости роста. Дети с полиартикулярным (49,0 %) и системным (54,5 %) вариантами течения ЮИА имели нарушения мышечной силы. Выводы. Выявление нарушения роста является основой углубленного обследования и пересмотра терапии больных ЮИА. Степень активности болезни влияет на показатели роста.
Background. The natural processes of the physical development in a pediatric patient are disturbed by juvenile idiopathic arthritis (JIA). The causes for this are found to originate from the disease pathogenesis, the developmental characteristics of the child’s body, and the chosen JIA therapy. The objective was to evaluate the physical development indices in our JIA patients depending on various treatment regimens in order to synthesize optimal recommendations aimed at preventing growth impairments in this category of patients. Materials and methods. Anthropometry data (growth by Standard Deviation Score), the growth rate for the previous year in 142 patients with JIA, and hand dynamometry in some children were evaluated. The results were compared using both parametric (Student’s t-test) and non-parametric (Mann-Whitney U test) methods, and the correlation was studied by multiple regression analysis. Results. There was no child with oligoarticular form of the disease diagnosed with growth delay during the study. Physical development disorders (height less than –1 SD) were detected in 12 patients (8.5 %) from both groups: in 6 — with the systemic form and in another 6 individuals — with the polyarticular form. When using immunobiological agents (disease-modifying anti-rheumatic drugs), the relative growth velocity was significantly higher in patients with both oligoarticular (U = 225.5, p = 0.009) and polyarticular (U = 222.5, p = 0.0001) forms of the disease. According to the results of multiple regression analysis, the higher was the total disease activity score, the greater was the growth delay. Children with polyarticular (49.0 %) and systemic (54.5 %) forms of JIA had impaired muscle strength. Conclusions. The identification of growth disorders is the basis of an in-depth examination and treatment arrangements in patients with JIA. The degree of disease activity affects growth rates.
ювенільний ідіопатичний артрит; фізичний розвиток
ювенильный идиопатический артрит; физическое развитие
juvenile idiopathic arthritis; physical development
Вступ
Матеріали та методи
Результати та обговорення
Висновки
1. Марушко Т.В., Голубовська Ю.Є. Особливості фізичного розвитку та стану кістково-м’язової системи у хворих на ювенільний ревматоїдний артрит. Збірник наукових праць співробітників НМАПО імені П.Л. Шупика. 2018. № 30. С. 282-296. http://nbuv.gov.ua/UJRN/Znpsnmapo_2018_30_29.
2. Zuber Z. Oligoarticular onset juvenile idiopathic arthritis as the most common cause of disability of children and young adults. Reumatologia. 2019. 57(4). P. 189-191. doi: 10.5114/reum.2019.87607.
3. Minden K. Adult outcomes of patients with juvenile idiopathic arthritis. Horm. Res. 2009. 72 (Suppl. 1). P. 20-25. doi: 10.1159/000229759.
4. Серая В.А. Динамика роста у детей с ювенильным идиопатическим артритом на фоне различных режимов терапии: диссертация на соискание ученой степени кандидата медицинских наук: 14.01.08. Москва. 2018. 155 с.
5. Umlawska W., Prusek-Dudkiewicz A. Growth retardation and delayed puberty in children and adolescents with juvenile idiopathic arthritis. Arch. Med. Sci. 2010. 6(1). P. 19-23. doi: 10.5114/aoms.2010.13501.
6. Woo P.M. Growth retardion and osteoporosis in juvenile chronic arthritis. Clin. Exp. Rheumatol. 1994. 12 (Suppl. 10). P. 87-90. PMID: 7955635.
7. Widrowska J., Zygmunt A., Biernacka-Zielinsska M., Stanczyk J., Smolewska E. Influence of biologic therapy on growth in children with chronic inflammatory connective tissue diseases. Reumatologia. 2015. 53(1). P. 14-20. doi: 10.5114/reum.2015.50552.
8. Mehls O., Himmele R., Homme M., Kiepe D., Klaus G. The interaction of glucocorticoids with the growth hormone-insulin-like growth factor axis and its effects on growth plate chondrocytes and bone cells. J. Pediatr. Endocrinol. Metab. 2001. 14 (Suppl. 6). P. 1475-1482. PubMed PMID: 11837502.
9. McErlane F., Carrasco R., Kearsley-Fleet L. et al. Growth patterns in early juvenile idiopathic arthritis: Results from the Childhood Arthritis Prospective Study (CAPS). Semin. Arthritis. Rheum. 2018. 48(1). P. 53-60. doi: 10.1016/j.semarthrit.2017.11.002.
10. Guzman J., Kerr T., Ward L.M. et al. Growth and weight gain in children with juvenile idiopathic arthritis: results from the ReACCh-Out cohort. Pediatr. Rheumatol. Online J. 2017. 15(1). P. 68. doi: 10.1186/s12969-017-0196-7.
11. Бойко Я.Є., Грицюк І.І., Буряк Т.В. Аналіз причин затримки росту у дітей, хворих на ювенільний ідіопатичний артрит. Український ревматологічний журнал. 2006. 24(2). C. 70-73.
12. Бережной В.В., Марушко Т.В., Гляделова Н.П., Герман А.Б., Лисовец Т.В. Нарушение роста у детей с ювенильным ревматоидным артритом. Педиатрия. Восточная Европа. 2015. 3(11). С. 90-102. eLIBRARY ID: 24858897.
13. Ошлянська О.А., Меланчук Н.А. Особливості фізичного розвитку у дітей з ювенільним ідіопатичним артритом. Український ревматологічний журнал. 2019. 76(2). С. 52-57.
14. Simon D. Inflammation and growth. J. Pediatr. Gastroenterol. Nutr. 2010. 51 (Suppl. 3). P. 133-134. doi: 10.1097/MPG.0b013e3181f7feef.
15. Shiff N.J., Brant R., Guzman J. et al. Glucocorticoid-related changes in body mass index among children and adolescents with rheumatic diseases. Arthritis Care & Research. 2013. 65(1). P. 113-121. doi: 10.1002/acr.21785.
16. Elkan A.C., Engvall I.L., Cederholm T., Hafstrom I. Rheumatoid cachexia, central obesity and malnutrition in patients with low-active rheumatoid arthritis: feasibility of anthropometry, Mini Nutritional Assessment and body composition techniques. Eur. J. Nutr. 2009. 48(5). P. 315-322. doi: 10.1007/s00394-009-0017-y.
17. Sandstedt E., Fasth A., Eek M.N., Beckung E. Muscle strength, physical fitness and well-being in children and adolescents with juvenile idiopathic arthritis and the effect of an exercise programme: a randomized controlled trial. Pediatr. Rheumatol. Online J. 2013. 11(1). P. 7. doi: 10.1186/1546-0096-11-7.
18. Petty R.E., Southwood T.R., Manners P. et al. International league of associations for rheumatology classification of juvenile idiopathic arthritis: second revision, Edmonton, 2001. J. Rheumatol. 2004. 31(2). P. 390-392. PubMed PMID: 14760812.
19. Протоколи надання медичної допомоги дітям за спеціальністю «Дитяча ендокринологія» (№ 254 від 27.04.2006) зі змінами (№ 55 від 03.02.2009 та № 864 від 07.10.2013). https://zakononline.com.ua/documents/show/89079_535333.
20. Uettwiller F., Perlbarg J., Pinto G. et al. Effect of biologic treatments on growth in children with juvenile idiopathic arthritis. J. Rheumatol. 2014. 41(1). P. 128-135. doi: 10.3899/jrheum.130311.
21. Akioka S. Interleukin-6 in juvenile idiopathic arthritis. Mod. Rheumatol. 2019. 29(2). P. 275-286. doi: 10.1080/14397595.2019.1574697.

/9.jpg)
/10.jpg)
/11.jpg)
/12.jpg)