Резюме
Метою дослідження було вивчення ефективності та безпечності застосування препарату Мовіксикам® ОДТ (виробництво компанії MoviHealth, Швейцарія) у хворих з остеоартрозом (ОА) колінних суглобів. Матеріали та методи. У дослідженні брали участь 22 особи віком 50–75 років з ОА колінних суглобів ІІ–ІІІ стадії, які були розподілені на 2 групи. До основної групи увійшли 11 осіб, які приймали Мовіксикам® ОДТ у дозі 7,5 мг 2 рази на добу; група порівняння — 11 осіб, які приймали таблетовану форму мелоксикаму (Моваліс) в дозі 7,5 мг 2 рази на добу впродовж 10 днів. Усім пацієнтам проводили анкетування (оцінка больового синдрому, скутості, повсякденної активності за шкалою WOMAC, визначення альгофункціонального індексу Лекена), функціональне тестування та лабораторне дослідження рівня аланінамінотрансферази й аспартатамінотрансферази перед початком лікування та на 10-ту добу. Результати. На 10-ту добу терапії зареєстроване вірогідне зменшення вираженості больового синдрому за субшкалою болю WOMAC на 28,7 % у пацієнтів, які приймали Мовіксикам® ОДТ (t = 2,7, р = 0,02), та на 31,3 % (t = 4,1, р = 0,002) у групі порівняння, проявів скутості — на 45,0 % (t = 4,5, р = 0,001) проти 25,0 % (t = 2,95, р = 0,01) й обмеження повсякденної активності — на 33,5 % (t = 3,27, р = 0,008) проти 23,3 % (t = 6,72, р < 0,00001). Встановлене вірогідне покращення результатів виконання 3-метрового тесту лише в групі пацієнтів, які приймали Мовіксикам® ОДТ, на 8 % (t = 3,18, р = 0,009). Тривалість виконання тесту «сісти — встати» в основній групі зменшилась на 12,6 % (t = 3,27, р = 0,008), у групі порівняння — на 8,0 % (t = 3,02, р = 0,01). Пацієнти обох груп відзначили вірогідне покращення самопочуття, пов’язаного з ОА колінних суглобів, за індексом Лекерта: t = 2,19, р = 0,049 та t = 3,13, р = 0,01 відповідно. У групі пацієнтів, які приймали Мовіксикам® ОДТ, рівень аланінамінотрансферази мав тенденцію до зниження на 0,5 % (t = 0,13, р = 0,9) на 10-ту добу терапії, в той час як у групі пацієнтів, які лікувались таблетованою формою мелоксикаму, його рівень збільшився на 13,5 % (t = 1,24, р = 0,24). Спостерігалася схожа тенденція до зниження концентрації аспартатамінотрансферази у сироватці крові в основній групі на 6 % (t = 0,28, р = 0,23) та до його підвищення на 11,7 % (t = 1,87, р = 0,09) у групі порівняння. Висновки. Мовіксикам® ОДТ є високобіодоступною формою лікарського засобу, що викликає прихильність серед пацієнтів, особливо геріатричного профілю, завдяки зручності використання та швидкому початку дії. Таблетки, що розчиняються у ротовій порожнині, показали високий профіль безпеки з боку печінки, органів шлунково-кишкового тракту та хорошу ефективність за результатами проведених функціональних тестів та анкетування.
Целью исследования было изучение эффективности и безопасности применения препарата Мовиксикам® ОДТ (производства компании MoviHealth, Швейцария) у больных с остеоартрозом (ОА) коленных суставов. Материалы и методы. В исследовании приняли участие 22 человека в возрасте 50–75 лет с ОА коленных суставов II–III стадии, которые были разделены на 2 группы. В основную группу вошли 11 человек, принимавших Мовиксикам® ОДТ в дозе 7,5 мг 2 раза в сутки; группа сравнения — 11 человек, которые принимали таблетированную форму мелоксикама (Мовалис) в дозе 7,5 мг 2 раза в сутки в течение 10 дней. Всем пациентам проводили функциональное тестирование, анкетирование (WOMAC, индекс Лекерта) и лабораторное исследование уровня аланинаминотрансферазы и аспартатаминотрансферазы перед началом лечения и на 10-е сутки. Результаты. На десятый день терапии зарегистрировано достоверное уменьшение выраженности болевого синдрома согласно субшкалам боли WOMAC на 28,7 % у пациентов, принимавших Мовиксикам® ОДТ (t = 2,7, р = 0,02), и на 31,3 % (t = 4,1, р = 0,002) в группе сравнения, проявлений скованности — на 45,0 % (t = 4,5, р = 0,001) против 25,0 % (t = 2,95, р = 0,01) и ограничения повседневной активности — на 33,5 % (t = 3,27, р = 0,008) против 23,3 % (t = 6,72, р < 0,00001). Установлено достоверное улучшение результатов выполнения 3-метрового теста только в группе пациентов, принимавших Мовиксикам® ОДТ, на 8 % (t = 3,18, р = 0,009). Продолжительность выполнения теста «сесть — встать» в основной группе уменьшилась на 12,6 % (t = 3,27, р = 0,008), в группе сравнения — на 8 % (t = 3,02, р = 0,01). Пациенты обеих групп отметили достоверное улучшение самочувствия, связанного с ОА коленных суставов, по индексу Лекерта: t = 2,19, р = 0,049 и t = 3,13, р = 0,01 соответственно. В группе пациентов, принимавших Мовиксикам® ОДТ, уровень аланинаминотрансферазы имел тенденцию к снижению на 0,5 % (t = 0,13, р = 0,9) на 10-й день терапии, в то время как в группе пациентов, лечившихся таблетированной формой мелоксикама, его уровень увеличился на 13,5 % (t = 1,24, р = 0,24). Наблюдалась похожая тенденция к снижению концентрации аспартатаминотрансферазы в сыворотке крови в основной группе на 6 % (t = 0,28, р = 0,23) и к ее повышению на 11,7 % (t = 1,87, р = 0,09) в группе сравнения. Выводы. Мовиксикам® ОДТ — высокобиодоступная форма лекарственного средства, которая вызывает приверженность среди пациентов, особенно гериатрического профиля, благодаря удобству использования и быстрому началу действия. Таблетки, растворяющиеся в ротовой полости, показали высокий профиль безопасности со стороны печении, органов желудочно-кишечного тракта и хорошую эффективность по результатам проведенных функциональных тестов и анкетирования.
Background. The perpose was to study the efficacy and safety of Movixicam® ODT (MoviHealth, Switzerland) therapy in patients with knee osteoarthritis (OA). Materials and methods. The study included 22 persons aged 50–75 years old with knee OA of stages II–III. The main group included 11 persons aged 65.3 ± 7.5 years, who received 7.5 mg of Movixicam® ODT twice a day for 10 days. The comparison group included 11 persons aged 65.82 ± 6.10 years, who took a tablet form of meloxicam (Movalis) at a dose of 7.5 mg 2 times a day for 10 days. At the beginning of the study (before treatment) and on the 10th day, all patients underwent functional tests, questionnaires (WOMAC, Leguesne), and laboratory tests (ALT, AST). Results. In the Movixicam® ODT group on the 10th day of therapy, there was a significant reduction in the intensity of pain: according to the WOMAC scale, it decreased by 28.7 % (t = 2.7, p = 0.02), compared with 31.3 % (t = 4.1, p = 0.002) in the comparison group; reduction of stiffness — by 45.0 % (t = 4.5, p = 0.001) in main group and by 25.0 % (t = 2.95, p = 0.01) in comparison group; and restriction of the daily activity by 33.5 % (t = 3.27, p = 0.008) and 23.3 % (t = 6.72, p < 0.001) in main group and comparison, respectively. In terms of the functional tests in the main group, there was a significant improvement in the results of the 3-meter test: by 8 % (t = 3.18, р = 0.009) only in the Movixicam® ODT group. The duration of the sit-up test in the group of patients receiving Movixicam ODT decreased by 12.6 % (t = 3.27, p = 0.08), in the comparison group — by 8 % (t = 3.02, p = 0.01). Patients receiving Movixicam ODT and Movalis reported a significant improvement in their well-being associated with the knee OA, according to the Leckert index: t = 2.19, p = 0.049 and t = 3.13, p = 0.01, respectively. In the group of patients receiving Movixicam® ODT, the level of alanine aminotransferase tended to decrease by 0.5 % (t = 0.13, p = 0.9) on the 10th day of therapy, while in the group patients treated with tablet form of meloxicam, its level increased by 13.5 % (t = 1.24, p = 0.24). There was a similar tendency to decrease the concentration of aspartate aminotransferase in the serum in the main group by 6 % (t = 0.28, p = 0.23) and to increase it by 11.7 % (t = 1.87, p = 0.09) in the comparison group. Conclusions. Movixicam® ODT is a highly bioavailable form of the drug, which is popular among patients, especially geriatric subjects, due to its easy usage and rapid effect. Orally disintegrating tablets showed a high safety profile for the gastrointestinal tract and good efficacy, according to the results of functional tests and analysis of questionnaires.
Вступ
Таблетки, що диспергуються в ротовій порожнині (англ. Orally Disintegrating Tablets, надалі — ОДТ), набувають популярності серед медичних препаратів різних способів введення. Це пов’язано з покращенням прихильності пацієнта до лікування та низкою додаткових переваг порівняно з іншими формами препаратів [1]. Основною метою їх створення є підвищення безпеки, ефективності та зручності введення лікарського засобу (ЛЗ) [2, 3]. Сучасна технологія, за якою лікарська форма, що містить активні фармацевтичні інгредієнти, швидко розчиняється в ротовій порожнині за допомогою слини, зазвичай за лічені секунди, всмоктується в слизову оболонку, не потребуючи для цього води або розжовування, позитивно впливає на біодоступність препарату, його ефективність та якість життя пацієнтів з точки зору комфорту [4, 5].
На сьогодні пероральний спосіб введення ЛЗ є золотим стандартом у фармацевтичній промисловості, де він розглядається як найбезпечніший, найзручніший та найбільш економічно раціональний спосіб надходження ліків до організму, що сприяє найвищій прихильності пацієнтів до лікування [6]. У структурі всіх форм ЛЗ пероральний прийом препаратів становить 50–60 % [7].
ОДТ-форми ЛЗ вперше з’явилися на фармацевтичному ринку в 1980-х роках і зрештою стали одним із найшвидших способів пероральної доставки ліків [8]. На сьогодні Всесвітня організація охорони здоров’я наголошує на людиноцентрованому підході під час вибору тактики лікування та ведення пацієнта [9], що базується на врахуванні бажань і потреб пацієнта або членів його родини. За даними літератури, труднощі при ковтанні виникають у приблизно від 15 % осіб, старших за 60 років [10], та до 35 % дорослого населення [5]. Таким чином, цей спосіб надходження ЛЗ до організму є оптимальним у педіатричній, геріатричній практиці та серед пацієнтів з особливими потребами, коли є ризик виникнення труднощів під час ковтання. Багато людей літнього та старечого віку стикаються із труднощами при прийомі звичайних (таблетованих) пероральних лікарських форм, що пов’язано з тремором рук, дисфагією, хворобою Паркінсона. Також ця форма ідеально підходить для активних людей, які часто подорожують [2], або осіб, умови праці яких пов’язані з тривалим перебуванням на нарадах [5], спецзавданнях, або, навпаки, для осіб з обмеженими фізичними можливостями, які не мають під рукою питної води. Приємний смак та аромат ОДТ підвищують прихильність пацієнтів до лікування серед численних груп населення порівняно з таблетованими препаратами, органолептичні властивості яких можуть бути менш привабливими [8].
Управління з продовольства й медикаментів США (United States Food and Drug Administration — USFDA) визначила ОДТ як тверду лікарську форму, що містить діючу речовину, швидко розпадається в ротовій порожнині з часом розпаду in vitro приблизно 30 секунд або менше [12, 13]. Завдяки присутності супердезінтегрантів ОДТ розчиняється в ротовій порожнині, що призводить до активного всмоктування препарату, і це, у свою чергу, забезпечує швидкий початок дії. Оскільки всмоктування відбувається безпосередньо з ротової порожнини, біодоступність препарату зростає [1, 2, 11].
Основними перевагами ОДТ є: можливість введення лікарських препаратів у необхідній дозі пацієнтам, які мають труднощі при ковтанні, що складніше досягнути під час застосування рідких лікарських форм. Вони всмоктуються із ротової порожнини, глотки та стравоходу, рухаючись травною системою за допомогою слиновиділення, що сприяє збільшенню доступності препарату. Кількість препарату, що піддається пресистемному метаболізму, або ефекту первинного проходження, є меншою порівняно з традиційною таблеткою. На біодоступність впливає невиражений «ефект першого проходження» (від проходження крізь стінку шлунково-кишкового тракту (ШКТ) і печінку до потрапляння в системне кров’яне русло), що асоціюється зі зменшенням кількості небажаних побічних ефектів [8].
Серед основних недоліків виділяють, зокрема, необхідність дотримання вимог зберігання ЛЗ через їх виражені гігроскопічні властивості та пористу структуру, таблетки є більш крихкими. У зв’язку з цим виникає потреба у використанні спеціальних упаковок.
Метою нашого дослідження було вивчення ефективності та безпечності терапії препарату Мовіксикам® ОДТ у хворих з остеоартрозом (ОА) колінних суглобів.
Матеріали та методи
У відділенні клінічної фізіології та патології опорно-рухового апарату Державної установи «Інститут геронтології ім. Д.Ф. Чеботарьова НАМН України» та Українському науково-медичному центрі проблем остеопорозу були обстежені 22 особи чоловічої та жіночої статі віком 50–75 років з остеоартрозом колінних суглобів ІІ–ІІІ стадії. До основної групи увійшли 11 осіб віком 65,3 ± 7,5 року, які приймали препарат Мовіксикам® ОДТ у дозі 7,5 мг 2 рази на добу протягом 10 днів. До групи порівняння увійшли 11 осіб віком 65,82 ± 6,10 року, які приймали таблетовану форму мелоксикаму (Моваліс) в дозі 7,5 мг 2 рази на добу протягом 10 днів.
Критеріями включення у дослідження були встановлений ОА на основі скарг пацієнта (біль, обмеження обсягу рухів у колінних суглобах, порушення пов’язаної з цим життєдіяльності), даних клінічного й рентгенологічного обстеження (II–ІІІ стадія за класифікацією Kellgren J.H., Lawrence J.S. 1957 року [15]), вираженість больового синдрому > 40 мм за візуальною аналоговою шкалою болю та підписана пацієнтом власноруч інформована згода на участь у дослідженні до початку проведення будь-яких процедур скринінгу.
Критеріями виключення з дослідження були: гіперчутливість до мелоксикаму або до інших складових лікарського засобу чи активних речовин з подібною дією; наявність симптомів астми, ангіоневротичного набряку або кропив’янки після прийому ацетилсаліцилової кислоти або інших нестероїдних протизапальних препаратів (НПЗП); кровотеча із шлунково-кишкового тракту або перфорація в анамнезі; активна пептична виразка, гостра або тяжка серцева недостатність, порушення функції печінки та нирок. Крім того, до критеріїв виключення належав прийом інших НПЗП протягом 2 тижнів або глюкокортикостероїдів протягом 4 тижнів до моменту включення в дослідження та прийом симптом- та структурномодифікуючих засобів (SYSADOA), що використовуються в терапії ОА, протягом 2 тижнів до участі в дослідженні.
Клінічне обстеження та функціональні тести, антропометричні виміри (зріст, маса тіла та розрахунок індексу маси тіла) та лабораторні дослідження (визначення рівня аланінамінотрансферази (АЛТ) та аспартатамінотрансферази (АСТ) у сироватці крові) проводили перед початком терапії та на 10-ту добу лікування.
Вираженість больового синдрому, функціональний стан колінних суглобів та їх динаміку оцінювали за допомогою шкали WOMAC та трьох її субшкал (болю (А), скутості (Б) та повсякденної активності (В)), індекс тяжкості ОА колінних суглобів визначали за допомогою індексу Лекена. Оцінку самопочуття пацієнта, пов’язаного з захворюванням, визначали за індексом Лекерта, якість життя — за шкалою EuroQol-5D. Вираженість гастроентерологічних скарг проводили з використанням спеціалізованого опитувальника GSRS (Gastrointestinal Symptom Rating Scale), що складається з п’яти шкал: абдомінального болю, діарейного, диспептичного, рефлюкс-синдрому та синдрому запорів. Вираженість симптомів оцінювали згідно з кількістю набраних балів: 0 балів — немає скарг, 1 бал — незначний дискомфорт, 2 бали — помірний дискомфорт, 3 бали — середній, 4 бали — відносно сильний, 5 балів — сильний, 6 балів — дуже сильний дискомфорт [16]. Оцінку функціональних можливостей визначали шляхом проведення 3-метрового (с), 4-метрового (с), 15-метрового (с), 6-хвилинного (м) тесту та тесту «сісти — встати».
Статистичний аналіз проводили з використанням програми Statistica 10.0. Нормальність розподілу отриманих результатів визначали за критерієм Шапіро — Уїлка. Результати статистичного аналізу наведені у вигляді M ± SD, де M — середнє значення, SD — стандартне відхилення. Різницю показників вважали вірогідною за умови р < 0,05. Для проведення статистичного аналізу використовували t-критерій Стьюдента для споріднених та незалежних вибірок.
Результати
На час початку дослідження не було зареєстровано відмінностей між пацієнтами основної групи та групи порівняння за віком і антропометричними даними (табл. 1).
Також на початку дослідження пацієнти двох груп вірогідно не відрізнялися за результатами анкетування за шкалою WOMAC, індексом Лекена та тривалістю виконання тесту «сісти — встати», 3-метрового, 4-метрового, 15-метрового тесту та рівнем АЛТ та АСТ у сироватці крові (табл. 2).
У пацієнтів основної групи, які приймали Мовіксикам® ОДТ, зареєстроване вірогідне зменшення вираженості больового синдрому за даними субшкали болю опитувальника WOMAC на 28,7 % через 10 діб лікування (t = 2,7, р = 0,02) (рис. 1А). На 10-ту добу терапії Мовіксикамом® ОДТ у пацієнтів також виявлене вірогідне та більш виражене при зіставленні з групою порівняння зменшення проявів скутості на 45,0 % (рис. 2А) за субшкалою WOMAC (t = 4,5, р = 0,001) та обмеження повсякденної активності на 33,5 % (t = 3,27, р = 0,008) (рис. 3А).
Серед пацієнтів групи порівняння (рис. 1Б), які приймали таблетовану форму мелоксикаму, через 10 діб лікування вираженість больового синдрому за даними субшкали болю опитувальника WOMAC вірогідно зменшилась на 31,3 % (t = 4,1, р = 0,002), прояви скутості (рис. 2Б) — на 25,0 % (t = 2,95, р = 0,01) та обмеження повсякденної активності — на 23,3 % (t = 6,72, р < 0,00001) (рис. 3Б).
В основній групі встановлене вірогідне покращення результатів виконання 3-метрового тесту після лікування (рис. 4А) на 8 % (t = 3,18, р = 0,009). Так, перед початком терапії ОДТ-формою мелоксикаму середня тривалість виконання функціонального тесту становила 12,5 ± 3,8 секунди, тоді як через 10 днів від початку лікування — 11,5 ± 4,2 секунди. У групі порівняння не виявлено вірогідних відмінностей (рис. 4Б).
Після проведеного лікування виявлено вірогідне зниження тривалості виконання тесту «сісти — встати» в обох групах (рис. 5). У групі пацієнтів, які приймали Мовіксикам® ОДТ, спостерігалася більш виражена динаміка на 10-ту добу терапії, коли швидкість виконання тесту зменшилась на 12,6 % (t = 3,27, р = 0,008), в той час як у групі порівняння — на 8 % (t = 3,02, р = 0,01).
За результатами 15-метрового тесту в групах І та ІІ виявлене вірогідне зменшення тривалості його виконання після 10-денного лікування на 12,1 % (t = 2,26, р = 0,03) та 13 % (t = 2,6, р = 0,03) відповідно (рис. 6).
Пацієнти, які приймали препарат Мовіксикам® ОДТ та таблетовану форму мелоксикаму, відзначали вірогідне покращення самопочуття, пов’язаного з ОА колінних суглобів, за індексом Лекерта: t = 2,19, р = 0,049 та t = 3,13, р = 0,01 відповідно (рис. 7).
За результатами вивчення тяжкості ОА колінних суглобів за допомогою індексу Лекена, оцінки якості життя пацієнтів за шкалою EuroQol-5D, функціональних 4-метрового та 6-хвилинного тесту в обох групах спостерігалася позитивна динаміка, проте вірогідних відмінностей між групами не виявлено.
/14.jpg)
За шкалою GSRS вираженість симптомів абдомінального болю у вигляді незначного дискомфорту в групі лікування препаратом Мовіксикам® ОДТ відзначали 18,2 % пацієнтів та 45,5 % представників групи порівняння (під час проведення статистичного аналізу за критерієм χ2 вірогідної різниці не виявлено). 18,2 % пацієнтів, які приймали мелоксикам в таблетованій формі, оцінили вираженість рефлюкс-синдрому на рівні незначного дискомфорту, в той час як у жодного пацієнта, які приймали його в формі Мовіксикам® ОДТ, ознак рефлюксу не виявлено. Лише 1 пацієнт основної групи відзначав у себе наявність діарейного синдрому, що викликав незначний дискомфорт, разом із цим у пацієнтів групи порівняння проявів діареї не було. Наявності диспептичного синдрому та синдрому запорів пацієнти обох групах у себе не спостерігали.
/15.jpg)
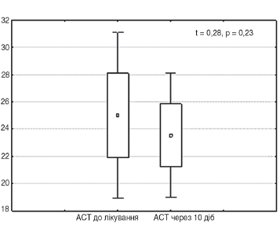
У групі пацієнтів, які приймали Мовіксикам® ОДТ, рівень АЛТ мав тенденцію до зниження на 0,5 % (t = 0,13, р = 0,9) на 10-ту добу терапії, в той час як у групі пацієнтів, які лікувались таблетованою формою мелоксикаму, його рівень збільшився на 13,5 % (t = 1,24, р = 0,24) (рис. 8A, Б). Спостерігалася схожа тенденція до зниження концентрації АСТ у сироватці крові в основній групі на 6 % (t = 0,28, р = 0,23) та до його підвищення на 11,7 % (t = 1,87, р = 0,09) у групі порівняння (рис. 8В, Г).
Проведене лікування не виявило суттєвої різниці між групами лікування Мовіксикамом® ОДТ та таблетованою формою мелоксикаму, за винятком вірогідного зменшення тривалості виконання 3-метрового тесту в групі лікування ОДТ. Разом із цим виявлені вірогідні зміни в обох групах до початку лікування та на 10-ту добу (табл. 3).
Обговорення
Дослідження, проведені на експериментальних моделях та тканинах людини, показують, що мелоксикам є більш потужним інгібітором циклооксигенази (ЦОГ) 2, ніж ЦОГ-1, та має добру переносимість [17]. Його терапевтична ефективність була перевірена на великій кількості пацієнтів із запальними захворюваннями суглобів, такими як ОА, ревматоїдний артрит та анкілозуючий спондиліт, і серед хворих з гострим болем у спині, болем у плечі [17]. За результатами нашого дослідження, пацієнти основної групи з ОА колінних суглобів, які приймали Мовіксикам® ОДТ, відзначали вірогідне зниження вираженості больового синдрому за даними субшкали болю опитувальника WOMAC (t = 2,7, р = 0,02), зменшення проявів скутості (t = 4,5, р = 0,001) та обмеження повсякденної активності (t = 3,27, р = 0,008). Подібні результати були виявлені у пацієнтів із групи порівняння, які приймали таблетовану форму мелоксикаму, в яких також зменшувались вираженість больового синдрому (t = 4,1, р = 0,002), прояви скутості (t = 2,95, р = 0,01) та обмеження повсякденної активності (t = 6,72, р < 0,00001). Також у пацієнтів відзначалась позитивна динаміка самопочуття, пов’язаного з ОА колінних суглобів, за індексом Лекерта в основній групі (t = 2,19, р = 0,05) та групі порівняння (t = 3,13, р = 0,01). За оцінкою індексу тяжкості ОА колінного суглоба та оцінкою якості життя пацієнтів за шкалою EuroQol-5D виявлена позитивна, проте невірогідна динаміка серед хворих обох груп.
Фармакокінетичні властивості мелоксикаму, що характеризуються тривалим періодом напіввиведення та відсутністю ефекту накопичення, дозволяють приймати препарат один раз на добу, що, у свою чергу, є ще одним фактором, який сприяє підвищенню комплаєнтності. Розчинення та всмоктування препарату, а також настання клінічного ефекту та біодоступності ОДТ можуть бути значно вищими порівняно зі звичайними лікарськими формами [18]. Крім того, не спостерігалося клінічно значущих змін у фармакокінетиці мелоксикаму в пацієнтів літнього віку чи в осіб з незначним порушенням функції нирок або під час одночасного прийому інших ліків, включаючи дигоксин, фуросемід, варфарин або метотрексат.
У нормі водневий показник (рН) слини та ротової порожнини людини, де починається метаболізм Мовіксикаму® ОДТ, має значення 6,2–7,6 [19] а середньодобовий рівень рН у порожньому шлунку становить близько 1,5 [20]. За даними досліджень, розчинення мелоксикаму ОДТ при рН 1,2; 4,0 та 6,8 становило 7,3; 7,8 та 61,8 % відповідно. Під час розчинення 15 мг мелоксикаму ОДТ виявлено дуже швидке вивільнення активного інгредієнта з досягненням розчинення на 98,6 % через 10 хвилин, у той час як розчинення таблетованої форми мелоксикаму у дозі 15 мг досягає рівня 88,4 % через 15 хвилин. Згідно з рекомендаціями FDA та Європейського агентства з лікарських засобів (European Medicines Agency — АМА) щодо досліджень розчинення та біоеквівалентності, схожість між двома препаратами підтверджується, оскільки обидва вони досягли розчинення понад 85 % протягом 15 хвилин [10].
Контрольовані клінічні випробування та постмаркетингові епідеміологічні дослідження показали як хорошу системну переносимість мелоксикаму, так і меншу частоту побічних ефектів з боку шлунково-кишкового тракту порівняно з частотою, що спостерігається після лікування загальновживаними неселективними НПЗП, такими як диклофенак або піроксикам [17].
У 16 рандомізованих контрольованих дослідженнях (РКД), в яких взяли участь 22 886 осіб, вивчали ефективність НПЗП, а саме селективних інгібіторів ЦОГ-2. Встановлено, що мелоксикам у дозі від 7,5 до 22,5 мг на добу має еквівалентну ефективність і демонструє чудову переносимість з боку шлунково-кишкового тракту порівняно з іншими неселективними НПЗП. Повідомлялося про значно меншу кількість клінічних ускладнень з боку верхніх відділів ШКТ (відносний ризик (ВР) 0,53; 95% диференційний індекс (ДІ) 0,29–0,97) [21].
В ще одному РКД взяли участь 20 374 особи (352 — з гострим люмбаго, 379 — з ревматоїдним артритом і 19 643 — з ОА). У пацієнтів, які застосовували мелоксикам, спостерігалися менше випадків виникнення диспепсії (ВР 0,73; 95% ДІ 0,64–0,84, тест на однорідність р = 0,62), менша кількість кровотеч з ШКТ (ВР 0,52; 95% ДІ 0,28–0,96, тест на гомогенність р = 0,69) та менша частота припинення прийому НПЗП через несприятливі події з ШКТ (ВР 0,59; 95% ДІ 0,52–0,67, тест на однорідність р = 0,09) порівняно з селективними НПЗП, що не є ЦОГ-2 [22].
У нашому дослідженні вираженість симптомів ураження ШКТ в основній групі та групі порівняння була невеликою. У двох пацієнтів основної групи та в п’яти пацієнтів групи порівняння виявлений абдомінальний біль за шкалою GSRS у вигляді незначного дискомфорту. Рефлюкс виявлений у двох пацієнтів, які приймали мелоксикам в таблетованій формі та оцінили його на рівні незначного дискомфорту, в той час як жодний пацієнт, який приймав його в формі препарату Мовіксикам® ОДТ, не мав скарг такого характеру. Лише 1 пацієнт основної групи відзначав у себе наявність діарейного синдрому, що завдавав йому незначного дискомфорту, разом з цим у пацієнтів групи порівняння проявів діареї не було. Диспептичного синдрому та синдрому запорів пацієнти обох груп у себе не спостерігали.
Мелоксикам має переваги перед неселективними НПЗП з точки зору переносимості з боку шлунково-кишкового тракту і, отже, заслуговує на увагу як відповідний кандидат для фармакологічного лікування ОА. Терапевтичний потенціал мелоксикаму за цим показанням вивчався в рандомізованих контрольованих дослідженнях порівняно з плацебо або іншими встановленими НПЗП, відкритих дослідженнях та спостережних когортних дослідженнях. Для більшості досліджень первинним результатом було зменшення болю при русі та/або у стані спокою, що зазвичай оцінювали за допомогою візуально-аналогової шкали в ураженому суглобі.
Висновки
Мовіксикам® ОДТ (виробництво компанії MoviHealth, Швейцарія) є високобіодоступною формою ЛЗ, що викликає прихильність серед пацієнтів, особливо геронтологічних, завдяки зручності у використанні та швидкому початку дії. Таблетки, що розчиняються у ротовій порожнині, продемонстрували високий профіль безпеки з боку печінки, органів ШКТ та хорошу ефективність за результатами проведених функціональних тестів та анкетування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Список литературы
1. Rameesa C.K., Drisya M.K. Orodispersible Tablet: A Patient Friendly Dosage Form (a Review). Bali Med. J. 2015. 4. 17. https://doi.org/10.15562/bmj.v4i1.101
2. Iswariya V.T., Babu V.L., Avanapu S.R. Formulation and Evaluation of Oro Dispersive Tablets of Saxagliptin. Int. J. Pharm. Sci Rev. Res. January — Febr 2015. 30(2). 42. 230-234; 30. 230-234.
3. Demyanenko O.S., Krykliva I.O. Justification of the choice of active pharmaceutical ingredients and excipients in organized tablets for the treatment of treatment. In: Proceedings Papers: collection of scientific works. Issue 3. Kharkiv, Ukraine. 2019. 72-74.
4. Richy F., Scarpignato C., Lanas A., Reginster J.Y. Efficacy and safety of piroxicam revisited. A global meta-analysis of randomised clinical trials. Pharmacol. Res. 2009. 60. 254-263. https://doi.org/10.1016/j.phrs.2009.03.021
5. Vronska L.V., Demchuk M.B., Hroshovyi T.A. Modern state of creation, production and research of drugs. Pharmatsevtychnyy chasopys. 2014. 3. 105-112.
6. Konapure S.A., Chaudhari P.S., Oswal R.J., Kshirsagar S.S., Antre R.V. Mouth Dissolving Tablets an Innovative Technology. Int. J. Appl. Biol. Pharm. Technol. 2011. 2. 496-503.
7. Shinde A., Yadav V., Gaikwad V., Dange S. Fast Disintegration Drug Delivery System: a Review. Int. J. Pharm. Sci Res. 2013. 4(7). 2548-2561. https://doi.org/10.13040/IJPSR.0975-8232.
8. Akshay Kumar S., Gowda D.V., Sharadha M. The insights on Oro-dispersible tablet. Int. J. Res. Pharm. Sci. 2020. 2743. https://doi.org/10.26452/ijrps.v11i1
9. Campbell H.T. Patient- vs People-Centred Care: What’ s the difference? Heal Stand Organ. 2020. 1-2.
10. Radicioni M., Connolly S., Stroppolo F. et al. Bioequivalence study of a novel orodispersible tablet of meloxicam in a porous matrix after single-dose administration in healthy volunteers. Int. J. Clin. Pharmacol. Ther. 2013. 51. 234-243. https://doi.org/10.5414/CP201781
11. Dey P., Maiti S. Orodispersible tablets: A new trend in drug delivery. J. Nat. Sci Biol. Med. 2010. 1. 2-5. https://doi.org/10.4103/0976-9668.71663
12. FDA U Guidance for Industry Orally Disintegrating Tablets. 2008. Fed. Regist 1–3.
13. Зупанець І.В., Рубан О.А., Колісник Т.Є. Сучасний стан розробки таблеток , що розпадаються у ротовій порожнині. 2019. 3. 6-12.
14. Pintu D., Dutta S. Formulation of fast disintegrating tablets. International J. Drug Formul. Res. 2011. 2. 45-51.
15. Menkes C.J. Radiographic criteria for classification of osteoarthritis. J. Rheumatol. 1991. 18. 13-15.
16. Barkhatov I.V. Application of gastroenterological questionnaire gsrs in early diagnosis of chronic abdominal ischemia syndrome. Med. J. Kazan. 2013. 94. 7-9.
17. Del Tacca M., Colucci R., Fornai M., Blandizzi C. Efficacy and tolerability of meloxicam, a COX-2 preferential nonsteroidal anti-inflammatory drug: A review. Clin. Drug Investig. 2002. 22. 799-818. https://doi.org/10.2165/00044011-200222120-00001
18. Vishali T., Damodharan N. Orodispersible tablets: A review. Res. J. Pharm. Technol. 2020. 13. 2522-2529. https://doi.org/10.5958/0974-360X.2020.00449.7
19. Baliga S., Muglikar S., Kale R. Salivary pH: A diagnostic biomarker. J. Indian Soc. Periodontol. 2013. 17. 461-465. https://doi.org/10.4103/0972-124X.118317
20. Holzer P. Acid sensing in the gastrointestinal tract. Am. J. Physiol. Gastrointest. Liver Physiol. 2007. 292. G699-705. https://doi.org/10.1152/ajpgi.00517.2006.Acid
21. Chen Y.F., Jobanputra P., Barton P., Bryan S., Fry-Smith A., Harris G. Cyclooxygenase-2 selective non-steroidal anti-inflammatory drugs (etodolac, meloxicam, celecoxib, rofecoxib, etoricoxib, valdecoxib and lumiracoxib) for osteoarthritis and rheumatoid arthritis: a systematic review and economic evaluation. Heal. Technol. Assess. 2020. 2008. 1-278. https://doi.org/10.3310/hta12110
22. Schoenfeld P. Gastrointestinal safety profile of meloxicam: A meta-analysis and systematic review of randomized controlled trials. Am. J. Med. 1999. 107. 48-54. https://doi.org/10.1016/s0002-9343(99)00367-8

/11.jpg)
/12.jpg)
/13.jpg)
/14.jpg)
/15.jpg)
/16.jpg)