Вступ
Гострий тонзилофарингіт — одна з найбільш поширених патологій у дітей [1]. У структурі хвороб органів дихання захворюваність на гострий фарингіт і тонзиліт у дітей становить 7,32 % [2, 3]. Біль у горлі посідає друге місце за частотою скарг при гострих респіраторних захворюваннях після кашлю [4]. У США щорічно лікарями загальної практики та педіатрами здійснюється до 15 мільйонів консультацій у зв’язку з подібною скаргою [5, 6].
За статистичними даними, у період з 2011 по 2015 рік в Україні спостерігалася тенденція до зростання показників захворюваності на гострий фарингіт і гострий тонзиліт серед дітей віком від 0 до 17 років [3]. За останні 5 років захворюваність зросла на 6,23 % (з 58,9 до 62,6 % на 1000 дітей). Проведений аналіз у розрізі вікових груп показав, що з віком захворюваність на гострий фарингіт і тонзиліт має тенденцію до зменшення. Так, захворюваність серед дітей 0–6 років становить 66,07 на 1000 дітей, 7–14 років — 59,07 на 1000 дітей, 15–17 років — 62,3 на 1000 дітей, 18 років і старше — 11,37 на тисячу осіб. Висока захворюваність дитячого населення молодшої вікової категорії пов’язана з незрілістю елементів місцевого та загального імунного захисту [2]. Порівняно низьку захворюваність дорослого населення можна пояснити тим, що багато хворих із болем у горлі віддають перевагу самолікуванню та з різних причин воліють не звертатися до лікаря за допомогою [7, 8], тому випадків недіагностованого гострого тонзилофарингіту в дорослих може бути набагато більше.
Установлено, що в 5–17 % дорослих осіб збудником гострого тонзилофарингіту є бактерії, передусім β-гемолітичний стрептокок групи А [9, 10]. В дитячому віці цей збудник вважають причиною 15–30 % випадків гострого тонзилофарингіту [11, 12]. Інші 70–85 % випадків гострого тонзилофарингіту в дітей мають переважно вірусну етіологію [13, 14]. Етіологічне значення мають аденовіруси, вірус Епштейна — Барр, віруси грипу та парагрипу, риновіруси тощо. У літню пору року актуальними стають ентеровіруси, що спричиняють гострий тонзиліт, схожий на бактеріальний [15].
Системна антибактеріальна терапія неефективна при вірусних тонзилітах; не запобігаючи бактеріальній суперінфекції, вона потенціює розмноження бактеріальної флори, нечутливої до протимікробного препарату, а також грибів, не кажучи про можливі побічні дії препаратів. Тому, згідно з сучасними рекомендаціями, основну масу хворих на гострий тонзиліт рекомендується вести без антибіотиків (АБ) [16, 17].
Проте в реальності антибіотикотерапія в даної категорії хворих проводиться часто [18, 19]. У наукових дослідженнях останніх років неодноразово наголошується, що гострий тонзиліт — один із топових діагнозів у контексті необґрунтованого використання антибактеріальної терапії [20]. За даними статистики (PROXIMA Pharma, 2017), антибіотики при діагнозі «гострий тонзиліт» призначають: отоларингологи — у 64 % випадків; терапевти/сімейні лікарі — у 72 %; педіатри — у 53 % випадків. За протоколами NICE (National Institute for Health and Care Excellence), середній рівень антибіотиків, призначених при ангіні, становить 60 % [10]. Наведені цифри значно перевищують статистично обґрунтовані дані раціонального використання антибіотиків. Зрозуміло, що надалі це призводить до розвитку й поширення надскладної сучасної проблеми людства — антибіотикорезистентності. Сьогодні пандемія SARS-CoV-2 наочно й болісно продемонструвала, наскільки беззахисні люди перед інфекціями, коли не мають проти них дієвої зброї у вигляді ефективної фармакотерапії. За прогнозами NICE, до 2050 року антимікробна резистентність може спричинити 10 мільйонів смертей щороку у всьому світі [10].
Для визначення показань до антибіотикотерапії як у дітей, так і в дорослих рекомендовано застосовувати шкалу Сentor [16, 21] (у дітей — у модифікації McIsaac [22]). Згідно з цими шкалами, стратегія антибактеріальної терапії визначається тим, що для кожної суми балів прорахована статистична ймовірність виявлення бета-гемолітичного стрептокока в мазку із зіва. Для трьох балів вона становить 35 %, для 4–5 балів — 50 %. Це означає, що половина всіх найяскравіших гострих тонзилітів із нальотами, гіпертермією та лімфаденітами так само мають вірусну природу.
З огляду на переважно вірусну етіологію захворювання й обмежені можливості антибіотикотерапії в лікуванні гострих тонзилофарингітів на перший план виходить місцеве лікування.
Як було показано в наших попередніх дослідженнях, місцева терапія гострих фарингітів із використанням комбінованого препарату лізоциму й деквалінію хлориду (Лізак) прискорює зворотний розвиток запалення носоглотки за рахунок нормалізації місцевого імунітету й безпосередньої протизапальної [23] і протимікробної активності [24–27].
Лізоцим — це мукополісахарид, ефективний щодо грампозитивних бактерій, вірусів і грибів. Має протизапальну дію, підвищує опірність організму. Деквалінію хлорид має антисептичну, антибактеріальну та протигибкову дію. Він також здатний знижувати поверхневий натяг, завдяки чому забезпечує проникнення діючих речовин у більш глибокі ділянки слизової оболонки.
На сьогодні переконливо доведено, що застосування Лізаку пришвидшує нормалізацію температури тіла і зникнення болю у горлі, знижує тривалість захворювання, сприяє більш швидкому регресуванню порівняно з контрольною групою таких ознак, як гіперемія слизової оболонки ротоглотки і набряклість піднебінних дужок [24, 25, 28].
Дослідження місцевого імунітету в дітей, в комплексі лікування яких застосовували Лізак, продемонструвало позитивну динаміку збільшення вмісту секреторного імуноглобуліну А і зниження рівня мономерної форми цього імуноглобуліну, що свідчить про зменшення впливу мікробних гідролаз на розщеплення димерної структури секреторного імуноглобуліну. Під час лікування гострого фарингіту в дітей препаратом Лізак відбувається нормалізація вмісту альфа-інтерферону і клітинного складу ротоглоткового секрету [22].
Схожі ефекти препарату Лізак були відмічені і при хронічному тонзиліті в дітей [29].
Дані мікробіологічного обстеження продемонстрували, що після терапії Лізаком знизилася колонізація слизової оболонки ротоглотки патогенною та умовно-патогенною флорою, змінювався мікробний спектр мигдаликів. Так, в основних дослідних групах значно рідше висівався St. aureus, ніж у групах порівняння. Найбільші позитивні зрушення спостерігалися щодо вмісту дефензіну β і лактоферину [25, 30].
Проспективне багатоцентрове наглядове клініко-імунологічне дослідження [28] 25 229 пацієнтів із 24 регіонів України у віці від 4 до 17 років 11 місяців показало відновлення стану еубіозу в 37 % спостережень при контрольних посівах зі слизових ротоглотки після закінчення курсу лікування препаратом Лізак. Відновлення мікробіоценозу відбувалось в основному за рахунок зменшення кількості патогенної та умовно-патогенної флори і збільшення кількості індигенної флори. Навіть у разі неповного відновлення еубіозу, що мало місце в дітей із частими повторними респіраторними захворюваннями, після лікування препаратом Лізак кількість індигенної флори значно збільшувалась.
Метою роботи було порівняння динаміки клінічної картини в дітей, що застосовували Лізак як місцеву терапію гострого тонзилофарингіту, залежно від того, приймали вони антибіотики чи ні.
Матеріали та методи
У рамках мультицентрового проспективного дослідження, що проходило в 14 регіонах України (усього взяли участь 21 416 дітей) і було присвячене вивченню ефективності застосування комбінованого антисептичного препарату Лізак у дітей, проведений аналіз динаміки клінічної картини і даних об’єктивного обстеження 2441 дитини віком 4–14 років із гострим тонзилофарингітом.
У рамках дослідження лікарі-педіатри первинної ланки заповнювали анкети, що стосувалися перебігу гострої респіраторної інфекції. Бактеріологічні дослідження практичними лікарями не проводилися. Це певною мірою відповідає чинним рекомендаціям більшості керівництв щодо ведення пацієнтів на амбулаторному етапі. Питання антибактеріальної терапії вирішувалися з урахуванням шкали McIsaac.
Імовірність бактеріальної інфекції визначалася за шкалою McIsaac (табл. 1).
Ми враховували, що 4–5 балів за шкалою вказують на високу імовірність (51–53 %) бактеріальної інфекції і є показанням до емпіричної антибіотикотерапії. Три бали за шкалою визначають ризик бактеріальної інфекції 28–35 %.
Оцінювалася наявність і вираженість ознак, що включені у шкалу McIsaac: біль у горлі, кашель, наліт на мигдаликах, збільшення регіонарних лімфатичних вузлів, підвищення температури тіла понад 38 °С.
Для характеристики інтенсивності скарг та інших клінічних проявів застосовували бальну шкалу: три бали — значна вираженість ознаки, два бали — помірна; один бал — незначна; нуль балів — відсутність ознаки.
Температура тіла вище 38 °С оцінювалася у 3 бали; коливання протягом доби 37,5–38 °С — 2 бали; 36,6–37,5 °С — 1 бал; відсутність підвищеної температури протягом доби — 0 балів.
Критеріями включення в дослідження були скарги на значний біль у горлі (максимальна кількість балів за бальною шкалою) та дані клінічної картини, що визначали помірний або високий ризик бактеріальної інфекції згідно із шкалою McIsaac: вік 4–14 років (1 бал); температура тіла на початку терапії вище від 38 °С (1 бал), болючість і збільшення шийних лімфатичних вузлів і/або набряк і ексудат на мигдаликах (1–2 бали).
Залежно від способу лікування діти були розділені на дві групи. Перша група — 1030 дітей, які застосовували в комплексній терапії препарат Лізак (по 3–4 таблетки залежно від віку, розсмоктуючи в ротовій порожнині). У другу групу ввійшли 1411 дітей, які додатково до такого ж комплексу лікування, що і в першій групі, отримували емпіричну ентеральну антибіотикотерапію (захищені пеніциліни або цефалоспорини другого чи третього покоління).
Оцінювання скарг і об’єктивного обстеження проводилось на початку лікування, через 3 й 7 днів терапії. Окремо відмічалося, на який день зменшився і зник біль у горлі. Вивчалися побічні ефекти, ефективність і переносимість місцевої терапії.
Кількість балів за шкалою McIsaac у першій групі (Лізак) становила 3,88 ± 0,02 бала, у другій групі (Лізак + антибіотик) — 4,21 ± 0,02 бала (р < 0,001). Тому з метою стандартизації вихідних даних кожну групу було поділено на три підгрупи залежно від кількості балів за шкалою McIsaac (табл. 2).
В обох групах більшість дітей мали 4 бали за шкалою McIsaac. Проте в першій групі було відносно більше дітей із 3 балами, у другій — із 5 балами. Тому оцінювання скарг і клінічної картини в динаміці проводилось окремо в кожній підгрупі.
У пацієнтів та їх батьків було отримано письмову інформовану згоду на проведення дослідження.
Статистична обробка результатів проходила з використанням GraphPad PRISM v. 8. Порівняльний аналіз проводився з використанням тесту Фішера і t-тесту Стьюдента (М ± m). Порівняння змін між вихідними показниками в групах аналізували за допомогою програмного забезпечення SAS JMP v. 15, використовуючи тест Вілкоксона для парних ненормально розподілених даних. Для обчислення співвідношення шансів використовувався Medcalc (https://www.medcalc.org/calc/relative_risk.php).
Результати та обговорення
Оскільки одним із критеріїв відбору дітей у дослідження була значна інтенсивність болю в горлі за даними анкетування, то на початку лікування біль у горлі у всіх дітей оцінювався у 3 бали (табл. 3).
На третій день лікування зменшувалася інтенсивність болів у горлі у всіх підгрупах. При цьому в дітей, які застосовували антибіотики в комплексі з місцевою терапією Лізаком, на третій день лікування зберігалася вірогідно більша інтенсивність скарг на біль у горлі порівняно з тими дітьми, які застосовували Лізак без антибіотиків. На сьомий день лікування в дітей із помірним ризиком бактеріальної інфекції біль у горлі мав однакову інтенсивність незалежно від того, застосовувався Лізак самостійно чи в комбінації з антибіотиком. Серед хворих з оцінкою за шкалою McIsaac 4 бали зберігалася вірогідна різниця між тими, хто приймав і не приймав антибіотик разом із препаратом Лізак, і була вона не на користь антибіотика. У дітей з оцінкою за шкалою McIsaac 5 балів показники в групі антибіотикотерапії були кращими.
Отримані дані дали нам підставу вважати, що ті лікарі, які не призначили антибіотикотерапію при 5 балах за шкалою McIsaac, недооцінили тяжкість стану дітей і ризик бактеріальної інфекції. Разом із тим у групі дітей з оцінкою 3 і 4 бали доцільність призначення антибіотиків була сумнівною. Їх додавання до місцевої терапії Лізаком не пришвидшило зменшення болів у горлі.
Надалі ми порівняли, на який день зменшився і зник біль у горлі у досліджуваних групах (табл. 4).
Виявилося, що в дітей із помірним ризиком бактеріальної інфекції (3 бали за шкалою McIsaac) не було відзначено вірогідної різниці за днем як зменшення, так і зникнення болю в горлі залежно від прийому антибіотиків. В обох підгрупах біль у горлі зменшився в середньому на третій день і на п’ятий день зник. Тобто антибіотики не пришвидшили зменшення і зникнення болю у горлі. У дітей із високим ризиком бактеріальної інфекції зменшення болю в горлі наставало пізніше. Зникнення болю при високому ризику відбувалося в ті ж самі терміни, що і при середньому.
Ці дані підтверджують думку про те, що антибіотики не пришвидшують ліквідацію клінічних симптомів при гострому тонзилофарингіті. Більше того, в окремих випадках можуть навіть сповільнювати ліквідацію больового синдрому.
Ураховуючи, що відсутність кашлю була критерієм відбору дітей у підгрупи, частота й інтенсивність кашлю виявилися вищими в дітей із трьома балами за шкалою. Проте достатньо висока бальна оцінка кашлю була на початку лікування і в групі з оцінкою 4 бали, у якій приймали антибіотики. Можливо, саме тому в цій групі пізніше відбувалося покращення клінічної картини (табл. 5).
Можна припустити, що ці діти мали ще інші причини кашлю, крім гострого тонзилофарингіту. Однією з таких причин може бути алергічний фон захворювання, що, можливо, подовжує перебіг гострих запальних змін. Не виключена й наявність супутніх запальних змін пазух носа, які також можуть давати збільшення регіонарних лімфатичних вузлів. На жаль, у даному дослідженні у нас не було можливості оцінити наявність супутніх синуситів у дітей.
Дані об’єктивного обстеження також показали, що в дітей із високим ризиком бактеріальної інфекції гіперемія зіва зникає пізніше при застосуванні антибіотиків, ніж без них (рис. 1).
Причому на третій день лікування різниці в групах не відмічалося. Гіперемія зіва виявлялася у 97,5–98,9 % дітей незалежно від групи. На сьомий день лікування гіперемія зіва зберігалася у 31,5–32,3 % дітей із високим ризиком, які отримували антибіотики, і у 8,8–13,3 % дітей із високим ризиком, які їх не отримували (р < 0,001). У дітей із середнім ризиком (три бали за шкалою McIsaac) застосування антибіотиків не впливає на динаміку цього показника. Гіперемія зіва в цій групі на сьомий день лікування у випадку застосування Лізаку виявлялася в 19,1 % дітей, при комбінації Лізаку й антибіотиків — у 14 % дітей (р > 0,05).
Оцінювання наявності й інтенсивності нальотів на мигдаликах показало, що застосування Лізаку само по собі сприяє їх ліквідації (рис. 2).
На сьомий день лікування в дітей з оцінкою за шкалою McIsaac 3 і 4 бали не була виявлена статистична різниця в частоті цього показника серед дітей, які приймали і не приймали антибіотики. Можна стверджувати, що у дітей з оцінкою за шкалою McIsaac 3 і 4 бали антибіотики не пришвидшували ліквідацію нальотів на мигдаликах при гострому тонзилофарингіті у випадку застосування Лізаку. У дітей з оцінкою за шкалою McIsaac 5 балів при застосуванні антибіотиків нальоти зникали пізніше. На початку лікування нальоти на мигдаликах були в усіх дітей з оцінкою за шкалою McIsaac 5 балів (100 %), на третій день зберігалися у 49,6 % дітей першої групи і у 94,3 % дітей другої групи (р < 0,001). На сьомий день лікування нальоти на мигдаликах були присутні в 1,3 % дітей першої групи і 13,8 % дітей другої групи (р < 0,001).
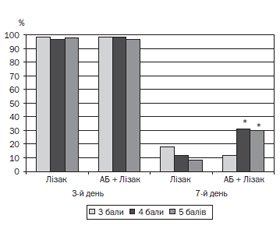
Зменшення регіонарних лімфатичних вузлів у дітей як із помірним, так і з високим ризиком бактеріальної інфекції відбувалося більш швидкими темпами в групі дітей, яким антибіотики не застосовували (рис. 3).
/18_2.jpg)
У дітей із помірним ризиком (3 бали за шкалою McIsaac), які не отримували антибіотики, частота виявлення збільшених регіонарних лімфатичних вузлів зменшилась з 61,8 % на початку лікування до 18,2 % на сьомий день (на 43,6 %). У дітей, у лікуванні яких застосовували антибіотики, цей показник зменшився з 78,1 до 58,4 % (на 19,7 %). Такі ж тенденції спостерігалися й у дітей із високим ризиком бактеріальної інфекції. У дітей з оцінкою за шкалою McIsaac 4 бали на початку лікування збільшені регіонарні лімфатичні вузли відмічалися у 94,5 % випадків в першій групі і в 92 % випадків — у другій. На сьомий день лікування збільшеними лімфатичні вузли залишалися у 21,5 % дітей першої групи і 30,6 % дітей другої групи (р < 0,001). У всіх дітей з оцінкою за шкалою McIsaac 5 балів на початку лікування були збільшені регіонарні лімфатичні вузли (100 %). На сьомий день лікування збільшеними лімфатичні вузли залишалися у 9,2 % дітей першої групи і 50,9 % дітей другої групи (р < 0,001).
При оцінюванні температури тіла в динаміці лікування ми дійшли висновку, що в дітей із помірним ризиком бактеріальної інфекції (3 бали за шкалою McIsaac) застосування антибіотиків сповільнювало нормалізацію температури. У дітей із високим ризиком бактеріальної інфекції застосування антибіотиків пришвидшувало нормалізацію температури тіла (табл. 6).
Таким чином, позитивний вплив антибіотикотерапії на клінічну картину при гострому тонзилофарингіті проявлявся тільки в дітей із високим ризиком бактеріальної інфекції (4 і 5 балів за шкалою McIsaac) і полягав у поліпшенні динаміки зменшення болю в горлі (у дітей з оцінкою 5 балів) і температури тіла (у дітей з оцінкою 4 бали) на 7-й день захворювання.
Загалом у результаті дослідження було виявлено, що місцева терапія деквалінію хлоридом і лізоцимом (препарат Лізак) у дітей 4–14 років із помірним ризиком бактеріальної інфекції (3 бали за шкалою McIsaac) завдяки протизапальній і бактерицидній дії може бути альтернативою застосування емпіричної антибіотикотерапії, оскільки комбінація препарату з антибіотиками не пришвидшувала видужування дітей. При оцінці за шкалою McIsaac 4 і 5 балів (високий ризик бактеріальної інфекції) підхід до застосування антибіотиків повинен бути більш диференційованим. Слід враховувати, що, незважаючи на те, що під дією антибіотикотерапії пришвидшується нормалізація температури тіла і зменшується ризик ускладнень гострого тонзилофарингіту, є висока ймовірність того, що довше будуть зберігатися гіперемія зіва, нальоти на мигдаликах і збільшені регіонарні лімфатичні вузли. Можна припустити, що причиною цього може бути дисбіоз носоглотки, що приєднується до гострого запалення внаслідок застосування антибіотиків. В цьому аспекті лізоцим, що входить до складу Лізаку, чинить позитивну дію, показаний при антибіотикотерапії, проте не слід розраховувати, що він може у всіх випадках запобігти зрушенню мікрофлори мигдаликів, що викликають антибіотики.
Висновки
1. За рекомендаціями більшості сучасних досліджень, при гострому тонзилофарингіті в дітей за неможливості проведення швидкого тесту на виявлення бета-гемолітичного стрептокока групи А перед тим, як приймати рішення про застосування емпіричної антибіотикотерапії, перш за все лікар повинен застосувати шкалу McIsaac.
2. У випадку оцінки стану пацієнта за шкалою McIsaaс 5 балів призначення антибіотиків доцільне, проте до них слід додати місцеву терапію препаратом, що впливає на місцевий імунний захист (одним із них є Лізак). При оцінці 4 бали слід співвіднести фактори користі й ризику, оскільки ризик затримки нормалізації стану слизової оболонки й регіонарних лімфатичних вузлів високий, і тільки після того приймати рішення про застосування антибіотиків, якщо користь перевищує ризик. При оцінці за шкалою McIsaac 2–3 бали застосування місцевої терапії препаратами з імуномодулюючою, протизапальною, протинабряковою й антимікробною дією достатньо для лікування гострого тонзилофарингіту без системного застосування антибіотиків.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Марушко Ю.В. Профілактика та терапія частих і рецидивних респіраторних захворювань у дітей — актуальна проблема педіатрії. Современная педиатрия. 2006. 2 (11). 32-36.
2. Пальчун В.Т., Лучихин Л.А., Крюков А.И. Воспалительные заболевания глотки. М.: ГЭОТАР-Медиа, 2012. 288 с.
3. Машейко А.М. Аналіз захворюваності на гострий фарингіт і тонзиліт та їх постстрептококових ускладнень у дітей в Україні. Соціальна фармація в охороні здоров’я. 2017. 3(1). 14-22.
4. Абдулкеримов Х.Т., Гаращенко Т.И., Кошель В.И., Рязанцев С.В., Свистушкин В.М. Тонзиллофарингиты. Санкт-Петербург: Полифорум Групп, 2014. 40 с.
5. Shulman S.T., Bisno A.L., Clegg H.W. еt al. Clinical practice guideline for the diagnosis and management of group A streptococcal pharyngitis: 2012 update by the Infectious Diseases Society of America. Practice Guideline. 2012 Nov 15. 55(10). 1279-82.
6. Little P., Moore M., Kelly J. еt al. Delayed antibiotic prescribing strategies for respiratory tract infections in primary care: pragmatic, factorial, randomised controlled trial. BMJ. 2014 Mar 6. 348.
7. Зайченко А.В., Мищенко О.Я. Местная эмпирическая терапия при острой боли в горле. Український медичний часопис. 2016. 1(111). 84-86.
8. Weber R. Pharyngitis. PrimaryCare: Clinics in Office Practice. 2014. 41(1). 91-98.
9. Ashworth M., Charlton J., Ballard K., Latinovic R., Gulliford M. Variations in antibiotic prescribing and consultation rates for acute respiratory infection in UK general practices 1995–2000. Br. J. Gen. Pract. 2005. 55. 603-8.
10. National Institute for Health and Care Excellence (NICE). Sore Throat (Acute): Antimicrobial Prescribing: NICE Guideline [NG84]. Leeds: NICE. 2018. URL: www.nice.org.uk/guidance/ng84 (accessed 2 April 2019).
11. World Health Organization. Rheumatic fever and rheumatic heart disease: report of a WHO Expert Consultation. WHO Technical Report Series. Retrieved from: http://apps.who.int/iris/bitstream/10665/42898/1/WHO_TRS_923.pdf
12. Shulman et al. IDSA Guideline for GAS Pharyngitis, Clinical Practice Guideline for the Diagnosis and Management of Group A Streptococcal Pharyngitis: 2012 Update by the Infectious Diseases Society of America. Clinical Infectious Diseases. 2012. 3. 1-17.
13. Ebell M.Н. et al. The rational clinical examination. Does this patient have strep throat? JAMA. 2000. 284(22). 2912-2918.
14. Spinks A., Glasziou P.P., Del Mar C.B. Antibiotics for sore throat. Cochrane Database Syst. Rev. 2013. 11. CD000023.
15. Hsieh T.H., Chen P.Y., Huang F.L. et al. Are empiric antibiotics for acute exudative tonsillitis needed in children? J. Microbiol. Immunol. Infect. 2011. 44(5). 328-332.
16. Clinical Knowledge Summaries. Sore Throat — Acute: Background Information. Leeds: NICE, 2018. https://cks.nice.org.uk/sore-throat-acute#!background (accessed 5 April 2019).
17. Martin E. Concise Medical Dictionary. New York, NY: Oxford University Press, 2015. https://www.oxfordreference.com/view/10.1093/acref/9780199687817.001.0001.
18. Gulliford M.C., Dregan A., Moore M.V. et al. Continued high rates of antibiotic prescribing to adults with respiratory tract infection: survey of 568 UK general practices. BMJ Open. 2014. 4. e006245.
19. Dolk F.С.К., Pouwels K.B., Smith D.R.M., Robotham J.V., Smieszek T. Antibiotics in primary care in England: which antibiotics are prescribed and for which conditions? J. Antimicrob. Chemother. 2018. 73 (2). ii2-ii10.
20. Fletcher-Lartey S., Yee M., Gaarslev C., Khan R. Why do general practitioners prescribe antibiotics for upper respiratory tract infections to meet patient expectations: a mixed methods study. BMJ Open. 2016. 6(10). e012244.
21. Сentor R.M., Witherspoon J.M., Dalton H.P., Brody C.E., Link K. The diagnosis of strep throat in adults in the emergency room. Med. Decis. Making. 1981. 1. 239-46.
22. McIsaac W.J., Goel V., To T. et al. The validity of sore throat score in family practice. CMAJ. 2000. 163(7). 811-815.
23. Мельников О.Ф., Пелешенко Н.А., Тимченко М.Д. и др. Противовоспалительные механизмы в действии антисептического препарата Лизак (клинико-иммунологическое исследование). Оториноларингологія. 2020. 4(3). 34-39.
24. Мельников О.Ф., Марушко Ю.В., Зелена Н.А., Мовчан О.В. Місцева терапія гострих фарингітів. Здоров’я України. 27.03.2015.
25. Марушко Ю.В., Мельников О.Ф., Зелена Н.А., Мовчан О.С. Місцева терапія гострих фарингітів. Совр. педиатрия. 2011. 4(38). 107-110.
26. Марушко Ю.В., Гищак Т.В. Санація ротоглотки при інфекційній патології у дітей. Сучасна педіатрія. 2017. 1(81). 20-25.
27. Марушко Ю.В., Московенко О.Д., Дуда О.В., Ананченко Н.Б., Чабанович О.В. Досвід використання комбінованого препарату лізоциму та деквалінію хлориду у дітей з гострими респіраторними інфекціями та афтозним стоматитом. Современная педиатрия. 2013. 7(55). 98-103.
28. Абатуров О.Є., Агафонова О.О., Токарева Н.М. Застосування препарату лізоциму й деквалінію хлориду в лікуванні гострих респіраторних захворювань верхніх дихальних шляхів у дітей. Здоровье ребенка. 2018. 13(6). 576-584.
29. Марушко Ю.В., Мельников О.Ф., Мовчан О.С. Досвід застосування деквалінію хлориду та лізоциму у терапії захворювань верхніх дихальних шляхів у дітей. Sovremennaya pediatriya. 2014. 7(63). 63-68.
30. Марушко Ю.В., Мельников О.Ф., Зелена Н.А., Мовчан О.С. Актуальні проблеми терапії хронічного тонзиліту нестрептококової етіології. Здоров’я України. 2012. 1. 36-39.
/17.jpg)
/17_2.jpg)
/18_2.jpg)

/15.jpg)
/16.jpg)
/17_3.jpg)
/18.jpg)