Артеріальна гіпертензія (АГ) залишається найбільш поширеним хронічним захворюванням, що призводить до зростання числа серцево-судинних (СС) і цереброваскулярних захворювань, а також смертності. Незважаючи на значні успіхи, досягнуті в покращенні діагностики й фармакологічної терапії АГ, рівень контролю артеріального тиску (АТ) в популяції в Україні залишається низьким. У свою чергу, це приводить до того, що рівень серцево-судинної захворюваності й смертності не знижується. З часу відкриття в 1957 році тіазидних діуретиків, що вперше дали можливість ефективно знижувати АТ, ці препарати стали основним інструментом для лікування АГ. Цю лекцію ми присвятили групі антигіпертензивних препаратів першого ряду, які, на нашу думку, залишаються недооціненими і, відповідно, призначаються не настільки часто, як це було б необхідно для покращання контролю АТ. Ітиметься про тіазидні й тіазидоподібні діуретики.
Роль затримки натрію й рідини в патогенезі АГ. Класичні уявлення про роль затримки натрію і води в розвитку артеріальної гіпертензії лежать в основі так званого об’єм-залежного механізму. І нирки при цьому відіграють провідну роль як орган, що регулює водно-сольовий гомеостаз.
У той же час показано, що затримка натрію і води призводить до накопичення деяких інших електролітів, у тому числі кальцію, не тільки в плазмі крові, а й у стінці судин. Таке накопичення може збільшувати чутливість судинної стінки до пресорних регуляторних впливів. При цьому може спостерігатися така активація механізмів регуляції АТ (ренін-ангіотензин-альдостеронова система (РААС), натрійуретичні пептиди (НУП), симпатоадреналова система (САС)), що порушує природний баланс вазоконстрикторних і вазодилататорних субстанцій. Отже, як збільшення чутливості судинної стінки до впливу вазопресорних механізмів, так і збільшення вмісту цих субстанцій у плазмі крові замикають порочне коло, необхідне для стійкого підвищення артеріального тиску. Одночасно збільшується об’єм позаклітинної рідини, що приводить до набухання судинної стінки. Важливим доповненням до цього є те, що накопичення вазоактивних субстанцій у стінці артеріол і підвищений АТ супроводжуються порушеннями функції ендотелію, локальним і системним спазмом судин, можуть запускати системне запалення, процес ремоделювання судин, що врешті-решт призводить до зміни перфузії та ураження органів-мішеней (рис. 1). Отже, затримка натрію і рідини — це не тільки збільшення об’єму циркулюючої крові, але й активація системних процесів та активне ураження органів-мішеней.
/16.jpg)
Вплив антигіпертензивних засобів на патогенетичні ланки при АГ. Есенціальна АГ має багатофакторний механізм як розвитку, так і підтримки високого АТ в подальшому. У клініці ми дуже рідко можемо вказати на провідний патогенетичний механізм, вплив на який буде забезпечувати найбільший ефективний контроль АТ. Класичні уявлення про вплив антигіпертензивних препаратів першого ряду на ланки патогенезу АГ подані на рис. 2. Так, бета-адреноблокатори (ББ), інгібітори ангіотензинперетворювального ферменту (ІАПФ) і блокатори рецепторів ангіотензину ІІ (БРА) є препаратами, що зменшують нейрогуморальної вплив на серцево-судинну систему. ІАПФ і блокатори рецепторів ангіотензину ІІ, а також антагоністи кальцію є класичними представниками вазодилататорів. Також є окремий підклас препаратів — так звані вазодилатуючі бета-адреноблокатори. Вважають, що всі вазодилататори можуть позитивно впливати на функцію ендотелію. Також доведено позитивний вплив на процеси ремоделювання серця й судин ІАПФ, блокаторів рецепторів ангіотензину ІІ і блокаторів кальцієвих каналів (БКК). Незважаючи на те, що діуретики як клас антигіпертензивних препаратів використовуються найдовше, їх механізми дії залишаються мало вивченими. Традиційно їм приписують вплив на затримку натрію і рідини в організмі, а також, можливо, вони впливають на збільшення чутливості до дії вазодилататорних препаратів.
Важливість жорсткого контролю АТ для запобігання серцево-судинним ускладненням АГ. У європейському дослідженні Cardio-Sis було продемонстровано, що при жорсткому контролі АТ у пацієнтів частота серцево-судинних ускладнень знижувалася вдвічі порівняно з хворими, у яких застосовувалася стратегія звичайного контролю тиску [3]. Дані наведені на рис. 3.
У дослідженні SPRINT (2015) жорсткий конт-роль АТ зумовлював достовірне зниження ризику досягнення кінцевих точок (СС-смерть, СС-події, смерть від усіх причин). У цьому випробуванні в групі жорсткого контролю тиску частка призначення тіазидних і тіазидоподібних діуретиків у монотерапії становила 16 %, а комбінації з ними налічували > 50 % від усіх багатокомпонентних схем терапії. З 2179 учасників, яким призначили ≥ 3 антигіпертензивних препарати на початку, 62 % отримували тіазид. Навіть ці результати показують, що призначення тіазидів продовжує залишатися неоптимальним. Зрозуміло, що для подальшого покращення конт-ролю АТ частка призначення тіазидів повинна бути значно більшою [4].
У метааналізі M.A. Suchard і співавт. (2019), у якому були вивчені дані майже 5 млн пацієнтів, науковці проаналізували всі можливі кінцеві точки й визначили ефективність класів препаратів І ряду. З’ясувалося, що в контексті зниження ризику досягнення таких кінцевих точок, як інфаркт міокарда (ІМ), госпіталізація щодо серцевої недостатності, інсульт, СС-події, раптова смерть, нестабільна стенокардія, ІАПФ поступаються тіазидним і тіазидоподібним діуретикам. У своїй здатності знижувати ризик серцево-судинних ускладнень діуретики не поступилися жодній групі препаратів. А найменш ефективними порівняно з іншими групами виявилися недигідропіридинові антагоністи кальцію [5]. Дані наведено на рис. 4.
Отже, тіазидні й тіазидоподібні діуретики на даний момент мають найбільш вагомі докази щодо їх ефективності в лікуванні АГ — досягнення цільового рівня АТ і запобігання розвитку серцево-судинних і судинно-мозкових ускладнень.
Механізми дії тіазидних і тіазидоподібних діуретиків. Діуретичні препарати, як правило, класифікуються, по-перше, за переважним місцем дії вздовж нефрона, а по-друге, за механізмом, за допомогою якого вони інгібують транспорт натрію і води (рис. 5). Основним місцем дії тіазидів є початкові відділи дистальних звивистих канальців, де вони порушують реабсорбцію натрію за рахунок гальмування роботи натрій-хлорного котранспортера [6]. Як видно з рис. 5, тіазидні діуретики можуть потенційно вплинути на 6 % реабсорбції натрію і, відповідно, є слабкими діуретичними засобами порівняно з петльовими діуретиками або інгібіторами карбоангідрази.
/18.jpg)
Незважаючи на структурні відмінності між окремими представниками, термін «тіазидні діуретики» включає всі діуретики, що чинять первинну дію на дистальні канальці. Сьогодні вважається, що в їх дії присутня ще й антикарбоангідразна активність, яку проявляють не всі тіазиди, але, на думку експертів, вона не робить істотного внеску в механізм їх дії, оскільки натрій, що не всмоктується проксимально, реабсорбуєтся далі по ходу ниркових канальців, у товстій частині висхідного коліна петлі Генле. Більше того, видається малоймовірним те, що вплив тіазидоподібних діуретиків на звуження судин також опосередковується через натрійхлорний котранс-портер, оскільки миші з нокаутом його гена мають нормальний рівень АТ.
Отже, механізми, за допомогою яких тіазидоподібні діуретики знижують АТ, усе ще недостатньо вивчені. Гемодинамічні ефекти тіазидів можуть бути розподілені на короткочасні й тривалі. Початкове зниження АТ пов’язане зі зменшенням кількості позаклітинної рідини й об’єму плазми, що зменшує переднавантаження на серце і, як наслідок, зменшує серцевий викид. Уведення в цей період декстранів відновлює об’єм плазми й повертає АТ до тих рівнів, що спостерігалися до лікування. Тривалі антигіпертензивні ефекти тіазидів не пов’язані з величиною початкового зниження об’єму циркулюючої плазми крові, який швидко повертається практично до нормальних величин. На цій стадії збільшення об’єму циркулюючої крові за рахунок декстранів більше не приводить до збільшення артеріального тиску до рівнів, які спостерігалися до лікування [7]. Найбільш достовірне пояснення стійких антигіпертензивних ефектів, що викликаються більшістю тіазидів, полягає в зниженні загального опору судин, хоча точні механізми цього процесу не з’ясовані.
Використання діуретиків пов’язане з розвитком коротко- і довгострокових механізмів адаптації, спрямованих на підтримку внутрішньосудинного об’єму рідини. Короткочасна толерантність може бути наслідком післядозового антинатрійурезу, який виникає при зниженні концентрації лікарського засобу в плазмі й рідини у канальцях нижче від діуретичного порога й посилюється за рахунок первинного зниження об’єму міжклітинної рідини. У формування короткочасної толерантності також роблять внесок активація РААС і САС, пригнічення секреції передсердного натрійуретичного гормону й простагландинів нирок. Післядозова затримка натрію значною мірою залежить від кількості солі, яку споживають з їжею: обмеження солі збільшує загальний негативний баланс натрію в організмі й підсилює терапевтичну ефективність тіазидів, у той час як високе споживання солі нівелює цей ефект [8].
Припускають, що індукована тіазидами вазодилатація опосередковується відкриттям активованих кальцієм калієвих каналів, можлива все ж таки участь у цьому інгібування карбоангідрази, але точні механізми, за допомогою яких тіазидоподібні діуретики пригнічують звуження і ремоделювання судин, точно не з’ясовані. В експериментальних дослідженнях було показано вплив тіазидних діуретиків на систему простагландинів, тоді як лікування ніфедипіном і каптоприлом не впливало на генерацію судинного PGI2 [9].
Низка досліджень вказує на те, що тіазидоподібні діуретики інгібують індуковану ангіотензином ІІ вазоконстрикцію шляхом десенсибілізації кальцію в клітинах гладких м’язів, пов’язаних із шляхом Rho-Rho-кінази. Дослідники вважають, що необхідні подальші дослідження щодо розкриття механізмів дії тіазидоподібних діуретиків або структурно споріднених речовин, які можуть допомогти визначити нові механізми патогенетичного впливу й розробити нові антигіпертензивні препарати [10].
Крім того, за даними деяких досліджень, хлорталідон (ХТД) має значущі плейотропні ефекти, не обов’язково спільні з іншими діуретиками, на агрегацію тромбоцитів, транскрипцію генів, ангіогенез і проникність судин. Показано, що хлорталідон, як сильний інгібітор карбоангідрази серед діуретиків, що застосовуються для лікування АГ, зменшує агрегацію тромбоцитів і проникність судин і сприяє ангіогенезу набагато ефективніше, ніж препарати тіазидів, що мають мінімальний вплив на активність карбоангідрази [11].
Отже, основним механізмом дії діуретиків при АГ є вазодилатація і зниження чутливості судинної стінки до вазопресорних агентів. Хлорталідон, на відміну від чистих тіазидів, має додаткові механізми дії, які можуть збільшувати його ефективність як щодо контролю АТ, так і для запобігання серцево-судинним ускладненням.
Фармакокінетичні відмінності хлорталідону. У табл. 1 наведені фармакокінетичні характеристики тіазидних і тіазидоподібних діуретиків. Тіазиди й тіазидоподібні діуретики мають високу біодоступність. Завдяки значній ліпофільності й помірній здатності зв’язуватися з білками вони глибоко проникають в органи й тканини. Гідрохлортіазид (ГХТЗ) і хлорталідон слабо метаболізуються в печінці й виводяться із сечею в майже незмінному вигляді. Індапамід майже повністю метаболізується в печінці, і лише невелика частина активного препарату виводиться нирками. Крім того, хлорталідон має значний обсяг розподілу за рахунок проникнення в еритроцити. При цьому вивільнення з еритроцитів у плазму здійснюється дискретно й повільно, що забезпечує поступову екскрецію нирками й градуйовану дію на канальці [12].
/19.jpg)
Після одноразових пероральних доз гідрохлортіазид досягав пікових концентрацій за ≈ 2 год і мав період напіввиведення від ≈ 6,5 до 9 год. Період напіввиведення гідрохлортіазиду передбачає, що препарат слід давати двічі на день. Порівняно з гідрохлортіазидом хлорталідон має більш тривалий період напіввиведення, майже 42 години (діапазон 2 –48 годин). Як видно з табл. 1, хлорталідон має переваги щодо тривалості ефекту й періоду напіввиведення, отже, якщо пацієнт з якихось причин пропустив прийом препарату, це не матиме критичних наслідків.
Дози й антигіпертензивний ефект хлорталідону. Підходи до дозування тіазидів еволюціонували паралельно з поглибленням нашого розуміння їх механізму дії і залежності між дозою і ефектом. Початкове використання високих доз ґрунтувалося на уявленні про те, що ефективність даних лікарських засобів прямо пов’язана з кількістю натрію, що виділяється нирками, і зменшенням об’єму плазми крові. Більша доза передбачала більш виражене зниження АТ. Сьогодні тіазиди використовують в значно менших дозах, і термін «тіазид у малій дозі» став синонімом гідрохлортіазиду в дозі 12,5–25 мг/день або еквівалентної дози іншого тіазиду. Низькі дози тіазидів знижують АТ одразу приблизно в 50 % пацієнтів. Збільшення дози гідрохлортіазиду з 12,5 до 25 мг/день може привести до зростання ефекту ще у 20 % пацієнтів. Гідрохлортіазид у дозі 50 мг/день призводить до помітного зниження АТ у 80–90 % пацієнтів.
Аналіз наявних досліджень показує, що ефект 50 мг гідрохлортіазиду приблизно еквівалентний 25–37 мг хлорталідону. Іншими словами, це передбачає, що еквівалентні дози хлорталідону, як правило, повинні становити 50–75 % від типових доз гідрохлортіазиду [13].
У дослідженні SHEP (дослідження систолічної гіпертензії в літніх осіб) низька доза хлорталідону (12,5 мг/день) сприяла підтриманню контролю АТ протягом декількох років більше ніж у 50 % пацієнтів. Оскільки більш високі дози діуретиків викликають масивну втрату електролітів, їх рутинне застосування для лікування АГ вважають недоцільним.
Вплив різних доз хлорталідону на рівень АТ і вміст калію подано на рис. 6. Як видно з рис. 6, прийом цього препарату в дозі 25 мг протягом 12 тижнів зумовлював зниження систолічного АТ (САТ) на 11 мм рт.ст.; збільшення дози принципово не впливало на антигіпертензивний ефект, проте спостерігалося більш суттєве знижується вміст калію (–0,4 ммоль при прийомі 25 мг ХТД і –0,7 ммоль — при застосуванні ХТД у дозі 50–75 мг) [14].
/20.jpg)
Актуальність вибору дози тіазидних діуретиків можна оцінити, беручи до уваги вплив різних доз цих препаратів на смертність від серцево-судинних захворювань і захворюваність на них, а також криву реакції «доза — ефект» з точки зору антигіпертензивної ефективності й метаболічних ефектів. Що стосується першого, то метааналіз клінічних досліджень показав, що внаслідок терапії діуретиками в низьких (від 12,5 до 25 мг/добу хлорталідону або гідрохлоротіазиду) і високих дозах (50 мг/добу або більше) ступені зниження АТ були подібними, і ці дози мали еквівалентну користь щодо зменшення інсульту, застійної серцевої недостатності, серцево-судинної захворюваності й загальної смертності, але лише терапія низькими дозами діуретиків достовірно знижувала частоту коронарних ускладнень [15]. Отже, на поточний момент домінує концепція оптимальної дози тіазидних і тіазидоподібних діуретиків, що рекомендує застосовувати низькі клінічно ефективні дози.
Порівняння антигіпертензивної ефективності гідрохлортіазиду й хлорталідону
У дослідженні М.Е. Ernst зі співавт. за даними добового моніторування АТ показали, що хлорталідон достовірно більш ефективний у зниженні АТ, ніж гідрохлортіазид [16]. Гідрохлортіазид не забезпечував контроль АТ протягом доби, у той час як хлорталідон підтримував добрий контроль АТ у ранкові години й зберігав його до моменту прийому наступної дози препарату. Подібні дані було наведено в більш пізньому дослідженні A.K. Pareek зі співавт., які показали, що після 12 тижнів прийому препаратів гідрохлортіазид не забезпечував ефективного добового контролю АТ, який спостерігався при прийомі хлорталідону (рис. 7) [17].
/20_2.jpg)
У систематичному огляді 9765 публікацій було виявлено 14 рандомізованих досліджень, що включали 883 пацієнтів, які порівнювали гідрохлортіазид з індапамідом і хлорталідоном за антигіпертензивною ефективністю й метаболічними ефектами. Для правильного порівняння дози діуретика в кожній групі було визначено 3 рівні дози. При метааналізі випадкових рандомізованих досліджень індапамід і хлорталідон знижували систолічний АТ більше, ніж гідрохлортіазид: на –5,1 мм рт.ст. (95% довірчий інтервал від –8,7 до –1,6; Р = 0,004) і –3,6 мм рт.ст. (95% довірчий інтервал від –7,3 до 0,0; Р = 0,05) відповідно. Для обох порівнянь спостерігалася мінімальна неоднорідність, що мала місце під час випробувань, і не було доказів упередженості публікацій [18]. Дані наведені на рис. 8.
/21.jpg)
При проведенні аналізу в рамках дослідження MRFIT (Інтервенційне дослідження множинних факторів ризику) в групі хворих, випадково розподілених до впливу «спеціального втручання», переважне використання хлорталідону було пов’язане з більш низькою смертністю, ніж переважне використання гідрохлортіазиду. Однак призначення того чи іншого діуретика не було відповідним чином рандомізовано, і дизайн дослідження не дозволив надійно відокремити ефекти діуретиків від ефектів інших одночасних втручань [16].
Отже, відомі на поточний момент дані підтверджують більш потужний, тривалий і стабільний антигіпертензивний ефект хлорталідону порівняно з гідрохлортіазидом.
Вплив хлорталідону на центральний АТ та індекс аугментації. Останніми роками важливу роль відводять впливу антигіпертензивного лікування не тільки на АТ, виміряний на плечовій артерії, але й на центральний АТ та індекс аугментації. Причому вплив на останні вважають більш важливим, оскільки він більш точно відображає вплив тиску на органи-мішені. У дослідженні L.A. Fernandes зі співавт. було показано, що через 6 місяців лікування хлорталідоном у дозі 25 мг у комбінації з амілоридом 5 мг у дорослих з гіпертонічною хворобою 1-ї стадії достовірно знижувалася величина центрального САТ (123,3 ± 14,2 мм рт.ст. проти 113,4 ± 111,4 мм рт.ст., P = 0,0103) та індексу аугментації (87,7 ± 9,6 проти 83,8 ± 8,9; P = 0,0289), тоді як у групі лозартану в дозі 50 мг (двічі на день) не було виявлено достовірних змін як величини центрального САТ, так і індексу аугментації. Отже, лікування хлорталідоном/амілоридом, але не лозартаном протягом 6 місяців приводило до достовірного зменшення центрального систолічного АТ та індексу аугментації [19]. Дані наведено на рис. 9.
/21_2.jpg)
Вплив терапії АГ хлорталідоном на ризик серцево-судинних ускладнень. Ефективність хлорталідону при лікування АГ було оцінено в декількох великих рандомізованих контрольованих дослідженнях, у тому числі тих, що фінансувалися з незалежних від фармацевтичної індустрії джерел: програма виявлення й подальшого спостереження за гіпертензією (Hypertension Detection and Follow-Up Program — HDFP), дослідження з втручанням множинних факторів ризику (Multiple Risk Factor Intervention Trial — MRFIT), програма систолічної гіпертензії в людей похилого віку (Systolic Hypertension in the Elderly Program — SHEP) і дослідження антигіпертензивного й гіполіпідемічного лікування для запобігання серцевим нападам (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial — ALLHAT), і неодноразово було показано, що він зменшує захворюваність і смертність від серцево-судинних захворювань у стандартних клінічних дозах.
У дослідженні MRFIT у 9 клініках, у яких переважно спочатку призначали гідрохлортіазид, спостерігалася більша на 44 % смертність від ішемічної хвороби серця (ІХС), тоді як тенденція щодо смертності була сприятливою в 6 клініках, які переважно застосовували хлорталідон. Керуючий комітет дослідження MRFIT рекомендував переключити всіх учасників з гідрохлортіазиду на хлорталідон. Після цього при застосуванні хлоталідону та ж група хворих мала на 28 % нижчий ризик смерті від ІХС [20]. Надалі було проведено ретроспективний аналіз кардіоваскулярних подій у пацієнтів, які брали участь у дослідженні MRFIT. Виявилося, що продовження лікування діуретиками (як хлорталідоном, так і гідрохлортіазидом) супроводжувалося кращим виживанням без подій порівняно з групою пацієнтів, які припинили прийом препаратів. Однак при порівнянні ефекту хлорталідону й гідрохлортіазиду виявилося, що краще на 21 % виживання без подій було в групі хлорталідону (Р = 0,0016), в основному за рахунок впливу на частоту розвитку інфаркту міокарда, аортокоронарного шунтування й захворювань периферичних артерій. Дослідники зробили висновок, що для тривалого прийому, імовірно, перевагу слід віддавати тіазидоподібним діуретикам, зокрема хлорталідону [21].
У дослідженні ALLHAT порівнювали чотири різних типи терапії: дигідропіридинові антагоністи кальцію (амлодипін), ІАПФ (лізиноприл), альфа-блокатори (доксазозин) і тіазидоподібні діуретики (хлорталідон). Це було найбільше в історії антигіпертензивної терапії дослідження, що включало понад 42 тисячі пацієнтів. На відміну від сотень інших досліджень із сурогатними кінцевими точками це дослідження мало на меті встановити впив терапії на жорсткі клінічні кінцеві точки: частоту виникнення серцево-судинних, судинно-мозкових ускладнень і смерті. Первинною кінцевою точкою були фатальні коронарні події і нефатальний інфаркт міокарда, вторинними кінцевими точками були: загальна смертність, фатальний і нефатальний інсульт, комбінована коронарна точка, комбінована серцево-судинна захворюваність. Планувалося спостереження від 4 до 8 років. Середній строк спостереження становив приблизно 5 років. Попередній звіт показав, що хлорталідон був кращим за доксазозин у запобіганні серцево-судинним подіям, особливо серцевій недостатності, і ця гілка дослідження була закрита. Усі препарати порівняння достовірно знижували рівень АТ, хоча ступінь зниження не був еквівалентним: зниження АТ у групі хлорталідону було дещо більшим, ніж у групі лізиноприлу; амлодипін знижував діастолічний АТ дещо більше за систолічний АТ, але з тенденцією до меншого ефекту порівняно із хлорталідоном. Через 5 років спостереження контроль АТ (< 140/90 мм рт.ст.) був досягнутий приблизно у двох третин учасників, приблизно однаковою мірою в усіх групах. Частота розвитку первинної кінцевої точки в групах порівняння не різнилися, так само між групами не різнилася величина загальної смертності. Хлорталідон переважав амлодипін у запобіганні розвитку серцевої недостатності, але різниці в частоті коронарних подій між групами не було. Хлорталідон переважав лізиноприл щодо ступеня зниження АТ, запобігання інсульту, комбінованої серцево-судинної захворюваності й серцевої недостатності. Результати дослідження ALLHAT навели докази того, що тіазидоподібні діуретики повинні бути препаратами початкового вибору терапії АГ, особливо якщо обирати між препаратами, з якими їх тестували в цьому дослідженні. На сьогодні, коли ми на початку застосовуємо комбінацію з двох препаратів майже для всіх пацієнтів, ці результати свідчать на користь вибору тіазидоподібних діуретиків до застосування початкової комбінації [22]. Докази випробування ALLHAT та інших клінічних досліджень підтверджують, що ні альфа-адреноблокатори, ні ІАПФ, ні блокатори кальцієвих каналів не перевершують тіазидоподібні діуретики як початкову терапію для зменшення серцево-судинного або ниркового ризику. Отже, дані доказової медицини на поточний момент надають незаперечливі докази необхідності застосування тіазидоподібних діуретиків на першому кроці терапії АГ.
Цукровий діабет і застосування хлорталідону. Існують застереження щодо застосування діуретиків через можливі несприятливі метаболічні ефекти, зокрема порушення обміну глюкози. Так, відомо, що тривалий прийом тіазидних діуретиків збільшує ризик розвитку цукрового діабету на 5–7 %, але це не впливає на їх ефективність у запобіганні кардіоваскулярним ускладненням. Чи є підстави відмовлятися від призначення тіазидних і тіазидоподібних діуретиків?
В учасників дослідження ALLHAT із метаболічним синдромом до включення в дослідження за 4 роки спостереження частота нових випадків цукрового діабету (глюкоза натще > 126 мг/дл) становила 17,1 % для хлорталідону, 16,0 % для амлодипіну (Р = 0,49, хлорталідон проти амлодипіну) і 12,6 % для лізиноприлу (Р < 0,05; лізиноприл проти хлорталідону). Для тих, хто не мав метаболічного синдрому, частота розвитку діабету становила 7,7 % для хлорталідону, 4,2 % для амлодипіну та 4,7 % для лізиноприлу (P < 0,05 для обох порівнянь). У пацієнтів з метаболічним синдромом не було різниці у відносних ризиках щодо розвитку серцево-судинних ускладнень у групі амлодипіну порівняно з хлорталідоном. У тих, хто не мав метаболічного синдрому, у групі амлодипіну був вищий ризик розвитку серцевої недостатності (СР = 1,55; 95% ДІ 1,25–1,35]). У пацієнтів з метаболічним синдромом порівняно з лізиноприлом хлорталідон був кращим щодо частоти розвитку серцевої недостатності (1,31; 95% ДІ 1,04–1,64) і серцево-судинної захворюваності (1,19; 95% ДІ 1,07–1,32). Значної взаємодії між групою лікування і метаболічним синдромом не відзначено [23].
Аналіз даних дослідження ALLHAT показав, що середні рівні глюкози в плазмі крові натще зростали під час спостереження в усіх групах лікування. На другий рік у тих пацієнтів, які були рандомізовані до групи хлорталідону, спостерігалось найбільше збільшення (+8,5 мг/дл [0,47 ммоль/л] проти +5,5 мг/дл [0,31 ммоль/л] для амлодипіну та +3,5 мг/дл [0,19 ммоль/л] для лізиноприлу). За 2 роки коефіцієнти ризику щодо розвитку діабету порівняно з лізиноприлом (0,55; 95% ДІ 0,43–0,70) або амлодипіном (0,73; 95% ДІ 0,58–0,91) були значно нижчими, ніж у групі хлорталідону (1,0; P < 0,01). Не було значущої асоціації зміни вмісту глюкози в плазмі крові натще через 2 роки з подальшим розвитком коронарних подій, інсульту, серцево-судинною захворюваністю, загальною смертністю або кінцевою стадією хвороби нирок [24].
У давньому дослідженні SHEP із початку 90-х років, що тривало 5 років, брали участь пацієнти похилого й старечого віку з ізольованою систолічною АГ. Вивчали ефективність хлорталідону порівняно з плацебо. Протягом періоду спостереження на тлі прийому хлорталідону значно знижувалася кількість серцево-судинних подій. Через 5 років обидві когорти хворих почали лікувати однаково. Через 14,5 року після закінчення дослідження в групі хворих, які під час випробування отримували плацебо, загальна смертність становила: серед пацієнтів з початковим цукровим діабетом — 54 %, із цукровим діабетом, що розвинувся в процесі спостереження, — 47 %, без цукрового діабету — 40 %. У групі ХТД аналогічні показники становили 47, 39 і 40 % відповідно [25]. Дані наведено на рис. 10.
/23.jpg)
При post hoc аналізі дослідження ALLHAT, а також при подальшому спостереженні протягом 4 років дослідили вплив розвитку цукрового діабету на загальну смертність на тлі прийому хлорталідону, амлодипіну й лізиноприлу. Загалом розвиток цукрового діабету асоціювався зі збільшенням ризику смерті на 31 %. Однак, якщо проаналізувати групи окремо, виявилося, що в групі хлорталідону розвиток діабету практично не впливав на показник смертності. У групі амлодипіну на тлі розвитку цукрового діабету показник смертності збільшувався майже вдвічі, а в групі лізиноприлу — на 31 % [26]. Дані наведені в табл. 2.
Показники було стандартизовано за віком, расою, статтю, курінням, початковим рівнем глюкози, індексом маси тіла, рівнем артеріального тиску, терапією статинами й бета-блокаторами.
Було проаналізовано дані 22 418 учасників дослідження ALLHAT з початковим діабетом, діабетом, що виник протягом дослідження (7,5 % при лікуванні хлорталідоном, 5,6 % — амлодипіном і 4,3 % — лізиноприлом), або без діабету протягом перших 2 років спостереження, які в подальшому спостерігалися протягом 7 років (2,9 року до кінця дослідження і ще 4 додаткові роки після його закінчення). Первинним результатом була смерть від серцево-судинних захворювань (від ІХС, інсульту, серцевої недостатності або інших серцево-судинних причин). Пацієнти в групі хлорталідону з індукованим діабетом порівняно з його відсутністю мали такий самій ризик смерті від серцево-судинних захворювань (коефіцієнт ризику (КР) 1,04; 95% ДІ 0,74–1,47), смерті від усіх причин (КР 1,04; 95% ДІ 0,82 –1,30) і смерті від несерцево-судинних причин (КР 1,05; 95% ДІ 0,77–1,42). У групах амлодипіну або лізиноприлу при виникненні цукрового діабету ці показники були достовірно вищими (діапазон КР 1,22–1,53). Пацієнти з діабетом, який виник протягом спостереження, мали підвищений ризик ІХС порівняно з тими, у кого діабет був відсутній (КР 1,46; 95% ДІ 1,09–1,96), однак у тих, хто отримував хлорталідон, був значно нижчий ризик, ніж у групі лізиноприлу (КР 1,18 проти 2,57; Р = 0,04) [27]. Ці дані наведені на рис. 11.
/24.jpg)
Отримані дані свідчать про те, що пов’язаний із прийомом тіазидоподібного діуретика цукровий діабет мав менш несприятливий довгостроковий вплив на ризик серцево-судинних ускладнень, ніж діабет, що розвивався під час прийому інших антигіпертензивних препаратів. Тобто гіперглікемія, що виникає при тривалому прийомі тіазидних діуретиків, імовірно, обумовлена не розвитком або прогресуванням порушення чутливості тканин організму до глюкози і не має такого негативного прогностичного ефекту у випадках, коли цукровий діабет виникає спонтанно.
Вплив хлорталідону на функцію нирок при АГ. У вже згаданому дослідженні ALLHAT у когорті хворих, які мали різні початкові показники функції нирок, а саме швидкості клубочкової фільтрації (ШКФ) (≥ 90 мл/хв/1,73 м2; 60–90 мл/хв/1,73 м2; ≤ 60 мл/хв/1,73 м2), вивчали вплив порівнюваних препаратів на основні кінцеві точки — нефатальний ІМ і фатальні серцево-судинні події. За результатами аналізу між трьома групами учасників достовірної різниці не виявлено, тобто хлорталідон, який застосовувався для лікування хворих на АГ, мав такий же позитивний вплив на функцію нирок, серцево-судинні ускладнення і смертність, що й ІАПФ лізиноприл [28]. Дані наведені в табл. 3.
/25.jpg)
Традиційно вважають, що при зниженні ШКФ ≤ 40 мл/хв/1,73 м2 тіазидні й тіазидоподібні діуретики можуть не дати належного сечогінного ефекту, і їх рекомендують замінити на петльові діуретики. Вважають, що знижена ШКФ обмежує надходження натрію в дистальні канальці, тому тіазидним діуретикам немає на що впливати. Однак у хворих зі зниженою функцією нирок зазвичай є проблема контролю АТ. У дослідженні R. Agarwal зі співавт. (2014) пацієнтам з початковим рівнем ШКФ 20–45 мл/хв/1,73 м2 до базової терапії додавали хлорталідон протягом 12 тижнів. Препарат додатково сприяв достовірному зниженню САТ і діастолічного АТ (ДАТ), тобто тіазидоподібний діуретик хлорталідон можна призначати хворим зі зниженою функцією нирок з метою підсилення антигіпертензивного ефекту [29]. Дані наведено на рис. 12. Згідно з інструкцією до застосування хлорталідону його дозу не слід зменшувати до рівня ШКФ < 10 мл/хв/1,72 м2.
/25_2.jpg)
Вплив лікування АГ хлорталідоном на перебіг супутньої ішемічної хвороби серця. Відомо, що ББ і БКК використовуються як антиангінальні препарати і вони зменшують частоту нападів стенокардії. Якщо проаналізувати прогноз виживання в таких хворих, то препарати груп ІАПФ і ББ мають позитивний вплив на цей показник. Також відомо, що БКК не погіршують прогноз у пацієнтів з ІХС. А як щодо діуретиків?
Post hoc аналіз дослідження ALLHAT порівнював довгострокові клінічні результати в пацієнтів, яким був призначений амлодипін (n = 9048) або лізиноприл (n = 9 054), і тих, яким був призначений хлорталідон (n = 15 255), стратифікованих за статусом наявності ІХС до початку дослідження. Через 4–8 років рандомізоване лікування було припинено. Загальне спостереження (активне лікування + пасивне спостереження з використанням національних баз даних щодо смертності й госпіталізації) становило 8–13 років. Для більшості результатів серцево-судинних захворювань, термінальної стадії ниркової недостатності і загальної смертності не було відмінностей між рандомізованими групами лікування незалежно від початкового статусу ІХС. Частота серцево-судинних захворювань була достовірно вищою в групі лізиноприлу порівняно з хлорталідоном, а частота серцевої недостатності була значно вищою для амлодипіну порівняно з хлорталідоном у пацієнтів з ІХС і без неї (КР 1,10; Р < 0,001 і КР 1,38; Р < 0,001 відповідно). Під час тривалого спостереження були виявлені достовірні результати відповідно до взаємодії статусу ІХС (Р = 0,012) з амлодипіном і хлорталідоном щодо смерті від серцево-судинних захворювань та ІХС у пацієнтів з ІХС на початку дослідження (КР 0,88; Р = 0,04 і КР 0,84; Р = 0,04 відповідно) і в пацієнтів без неї (КР 1,06; Р = 0,15 і 1,08; Р = 0,17 відповідно). Результати збільшеної смертності від інсульту в групі лізиноприлу порівняно з хлорталідоном (КР 1,2; Р = 0,03) і госпіталізації внаслідок серцевої недостатності в групі амлодипіну порівняно з хлорталідоном (КР 1,12; Р = 0,01) під час тривалого спостереження не відрізнялися за базовим статусом ІХС. Дані наведені на рис. 13.
/26.jpg)
Автори зробили висновок, що ці результати не дають жодних підстав для зміни рекомендації включати тіазидоподібний діуретик у правильній дозі (такий як хлорталідон у дозі від 12,5 до 25 мг/добу) у початкову антигіпертензивну терапію для більшості хворих на АГ, у тому числі із супутньою ІХС [30].
Комбінована антигіпертензивна терапія як основа початкового лікування АГ. У багатьох хворих на АГ для досягнення бажаного рівня АТ необхідно використовувати кілька лікарських засобів. Включення в подібні комбінації тіазидів дозволяє досягти терапевтичного синергізму й одночасно мінімізує кількість побічних ефектів. Тіазиди потенціюють дію інших антигіпертензивних засобів при використанні в комбінації з ними, зазвичай викликаючи додаткове зниження АТ. Включення в схему лікування тіазидів мінімізує расові відмінності в ефектах, що спостерігаються при використанні інгібіторів РААС. У свою чергу, інгібітори РААС зменшують вираженість гіпокаліємії і метаболічних порушень, що можуть бути викликані тіазидами.
Відповідно до актуальних рекомендацій ESC/ESH щодо ведення хворих на неускладнену АГ розпочинати терапію слід з подвійної комбінації ІАПФ або БРА + БКК або діуретик (рис. 14) [31].
На другому кроці, при неефективності подвійної комбінації, рекомендовано призначити потрійну комбінацію (блокатор РААС, БКК і діуретик), бажано в одній таблетці. Третій крок передбачає, що при неефективності потрійної комбінації слід додати четвертий препарат, частіше — спіронолактон або інший діуретик, альфа- або бета-блокатор. Отже вибір між діуретиком і БКК існує тільки на початку лікування. Аналіз європейських рекомендацій дозволив сформулювати певні критерії щодо вибору діуретика або БКК як другого препарату. Критерії, на які слід звертати увагу під час вибору БКК або діуретика як другого компонента початкової терапії, наведено в табл. 4.
/27.jpg)
Роль терапії хлорталідоном у запобіганні резистентній АГ і її лікуванні. Було проведено ретроспективний аналіз дослідження ALLHAT щодо розвитку резистентної АГ при лікуванні різними препаратами першого ряду. Під час візиту хворих на етапі 2 роки спостереження в тих, у кого систолічний АТ був ≥ 140 мм рт.ст. або діастолічний АТ був ≥ 90 мм рт.ст., визначали резистентну до лікування АГ. 14 684 учасників відповідали указаним критеріям, і їх дані були проаналізовані. Серед учасників дослідження, яким призначили хлорталідон, амлодипін або лізиноприл, стійку до лікування АГ мали 9,6; 11,4 і 19,7 % відповідно. Дані наведені на рис. 15. Отже, у дослідженні ALLHAT, у якому титрували ліки до досягнення цільового рівня АТ, у групі призначення хлорталідону рідше розвивалася резистентна до лікування АГ [32].
/27_2.jpg)
Наведені результати дослідження ALLHAT були враховані при написанні рекомендацій Американської асоціації серця та інших інституцій щодо лікування резистентної АГ. Рекомендовано призначати тіазидоподібні діуретики у максимальних переносимих дозах для запобігання розвитку резистентної АТ. Крім цього, при лікування резистентної АГ після впровадження змін способу життя, виключення вторинних АГ і підтвердження прихильності до лікування пацієнтам, які приймають тіазидні діуретики, рекомендовано замінити їх на тіазидоподібні, такі як хлорталідон або індапамід [33]. Дані рекомендації наведені на рис. 16.
/27_3.jpg)
Роль терапії хлорталідоном у запобіганні розвитку хронічної серцевої недостатності (ХСН). Критерії діагностики ХСН були попередньо визначені в протоколі дослідження ALLHAT. Дані фракції викиду (ФВ), оціненої за допомогою контрастної вентрикулографії, ехокардіографії чи радіонуклідного дослідження, були доступні в 910 з 1367 госпіталізованих пацієнтів (66,6 %) через кінцеві точки, що відповідали критеріям дослідження. Для вивчення відмінностей у лікуванні ХСН (загалом, зі зниженою і збереженою ФВ) використовувались регресійні моделі Кокса, скориговані з урахуванням початкових характеристик. Оцінювали рівень смертності від ХСН. З тих, хто мав дані про ФВ, 44,4 % мали збережену і 55,6 % — знижену ФВ. Хлорталідон знижував ризик розвитку ХСН зі збереженою ФВ порівняно з амлодипіном, лізиноприлом або доксазозином; коефіцієнти ризику становили 0,69 (95% ДІ 0,53–0,91; Р = 0,009), 0,74 (95% ДІ 0,56–0,97; Р = 0,032) і 0,53 (95% ДІ 0,38–0,73; Р < 0,001) відповідно. Хлорталідон знижував ризик розвитку ХСН зі зниженою ФВ порівняно з амлодипіном або доксазозином; коефіцієнти ризику становили 0,74 (95% ДІ 0,59–0,94; Р = 0,013) і 0,61 (95% ДІ 0,47–0,79; Р < 0,001) відповідно. Хлорталідон був подібним до лізиноприлу за частотою розвитку ХСН зі зниженою ФВ (КР 1,07; 95% ДІ 0,82–1,40; Р = 0,596). Отже, за даними дослідження ALLHAT, хлорталідон достовірно зменшував частоту госпіталізації хворих унаслідок розвитку ХСН як із збереженою, так і зі зниженою ФВ порівняно з амлодипіном і доксазозином. Хлорталідон також знижував частоту госпіталізації хворих унаслідок розвитку ХСН у хворих зі збереженою ФВ порівняно з лізиноприлом [34]. Дані наведені на рис. 17.
/28.jpg)
Вплив антигіпертензивної терапії на ризик переломів тазостегнового суглоба і кісток таза в осіб похилого віку. Зв’язок між терапією трьома різними антигіпертензивними препаратами й ризиком перелому тазостегнового суглоба й кісток таза в осіб похилого віку в дослідженні ALLHAT: 22 180 учасників спостерігалися протягом 8 років (під час дослідження), а 16 622 із них спостерігалися додатково ще протягом 5 років після завершення дослідження. Учасників, яким призначили амлодипін і лізиноприл, об’єднали в одну групу й порівнювали з групою, що одержувала хлорталідон. Кінцевими критеріям оцінки були госпіталізація з приводу переломів тазостегнового суглоба й кісток таза. Співвідношення ризиків у групі хлорталідону порівняно з групою амлодипіну або лізиноприлу становило: під час дослідження скориговане СР — 0,79 (ДІ 95% 0,63 –0,98), при подальшому спостереженні після закінчення дослідження скориговане СР — 0,87 (ДІ 95%, 0,74–1,03) [35]. Дані наведено на рис. 18.
/29.jpg)
Частота виникнення гіпокаліємії і гіперкаліємії при лікуванні хлорталідоном хворих на АГ. Як уже було показано раніше, частота розвитку гіпокаліємії при терапії хлорталідоном є дозозалежною, вона різко виникає при застосуванні доз менше за 50 мг (рис. 6). Аналіз даних дослідження ALLHAT показав, що помірний рівень гіпокаліємії протягом одного року (3,2–3,4 ммоль/л) в основному спостерігався в групі хлорталідону (9,5 % порівняно з 1,7 % у групі амлодипіну і 0,8 % у групі лізиноприлу). Розвиток гострої гіпокаліємії (< 3,2 ммоль/л) спостерігався нечасто (3,5 % у групі хлорталідону). Для порівняння: гіперкаліємія (K+ > 5,4 ммоль/л) в основному розвивалась у пацієнтів групи лізиноприлу (3,6 %) і була менш поширеною серед хворих групи хлорталідону (1,2 %). Препарати калію було призначено 10 % учасників дослідження [36].
Частота виникнення побічних ефектів при лікуванні хлорталідоном хворих на АГ. Для того щоб визначитися з переліком і частотою побічних ефектів, ми використали ресурс www.pdr.net, який є найбільш відомим у світі сайтом, що надає професійним медичним працівникам доступ до найбільш повної інформації про ліки, доступні в США. Частота зареєстрованих тяжких і середньої тяжкості побічних ефектів і час їх появи при тривалому прийомі хлорталідону за даними цього ресурсу подана в табл. 5.
З огляду на відсутність чіткої цифрової інформації (через низьку частоту < 1 %) щодо побічних ефектів хлорталідону ми звернулися до іншого ресурсу — https://clincalc.com/DrugStats, який забезпечує безкоштовний доступ до оцінок даних про використання ліків, що відпускаються за рецептом, для пацієнтів у Сполучених Штатах і дозволяє оцінити основні показники використання ліків, що включають: річну частоту призначень, середню вартість, річну частоту рапортування про побічні ефекти тощо.
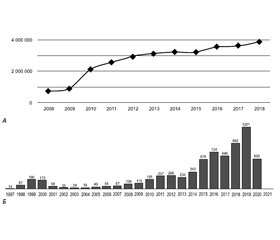
На рис. 19 наведено доступні дані щодо частоти призначення хлорталідону (відпускається тільки за рецептом) і кількості звітів про побічні ефекти хлорталідону, що подаються протягом року.
У 2018 році частота призначень хлорталідону в США сягнула майже 4 мільйонів пацієнтів, тоді як кількість звітів про побічні ефекти становила 892 випадки (< 0,025 %). Такі дані свідчать про низьку частоту виникнення побічних ефектів при хронічному прийомі хлорталідону і його високу безпечність для пацієнтів.
* * *
У березні 2021 року на українському фармацевтичному ринку з’явився новий лікарський засіб Таклор, таблетки по 25 мг № 30 виробництва АТ «Київмедпрепарат» (корпорація «Артеріум») — перший вітчизняний монопрепарат з молекулою хлорталідону. Таклор має доведену біоеквівалентність і розширює вибір препаратів для ефективного контролю артеріального тиску.
Висновки
Дані доказової медицини свідчать, що тіазидні й тіазидоподібні діуретики — ефективні антигіпертензивні препарати, які дозволяють як ефективно контролювати рівень АТ, так і запобігати розвитку серцево-судинних ускладнень АГ. Дані доказової медицини свідчать про те, що використання тіазидоподібних діуретиків, таких як хлорталідон, має переваги перед застосуванням гідрохлортіазиду.
Конфлікт інтересів. Не заявлений.
Отримано/Received 05.04.2021
Рецензовано/Revised 20.04.2021
Прийнято до друку/Accepted 26.04.2021
Список литературы
1. Titze J., Machnik A. Sodium sensing in the interstitium and relationship to hypertension. Curr. Opin. Nephrol. Hypertens. 2010. 19(4). 385-392.
2. Kirabo A. A new paradigm of sodium regulation in inflammation and hypertension. Am. J. Physiol. Integr. Comp. Physiol. 2017. 313(6). R706-R710.
3. Verdecchia P., Staessen J.A., Angeli F. et al. for Cardio-Sis investigators. Usual versus tight control of systolic blood pressure in non-diabetic patients with hypertension (Cardio-Sis): an open-label randomised trial. Lancet. 2009. 374(9689). 525-33.
4. Chang T.I., Evans G., Cheung A. et al. for the SPRINT Study Research Group. Correlates of Baseline Thiazide-Type Diuretic Prescription in the Systolic Blood Pressure Intervention Trial. Hypertension. 2016. 67. 550-555.
5. Suchard M.A., Schuemie M.J., Krumholz H.M. et al. Comprehensive comparative effectiveness and safety of first-line antihypertensive drug classes: a systematic, multinational, large-scale analysis. Lancet. 2019 Nov 16. 394(10211). 1816-1826.
6. Ellison D.H., Velázquez H., Wright F.S. Thiazide-sensitive sodium chloride cotransport in early distal tubule. Am. J. Physiol. 1987. 253. F546-F554.
7. Winer B.M. The antihypertensive actions of benzothiadiazines. Circulation. 1961. 23. 211-218.
8. Ram C.V., Garrett B.N., Kaplan N.M. Moderate sodium restriction and various diuretics in the treatment of hypertension. Arch. Intern. Med. 1981. 141. 1015-1019.
9. Numabe A., Uehara Y., Hirawa N. et al. Effects of thiazide diuretic on vascular eicosanoid system of spontaneously hypertensive rats. J. Hypertens. 1989. 6. 493-499.
10. Zhu Z., Zhu S., Liu D., Cao T., Wang L., Tepel M. Thiazide-like diuretics attenuate agonist-induced vasoconstriction by calcium desensitization linked to Rho kinase. Hypertension. 2005. 45. 233-239.
11. Woodman R., Brown C., Lockette W. Chlorthalidone decreases platelet aggregation and vascular permeability and promotes angiogenesis. Hypertension. 2010. 56(3). 463-70.
12. Sica D.A. Chlorthalidone: has it always been the best thiazide-type diuretic? Hypertension. 2006. Vol. 47. P. 321-322.
13. Carter B.L., Ernst M.E., Cohen J.D. Hydrochlorothiazide versus chlorthalidone: evidence supporting their interchangeability. Hypertension (Dallas, Tex: 1979). 2004. 43. 4-9.
14. Materson B.J., Oster J.R., Michael U.F. et al. Dose response to chlorthalidone in patients with mild hypertension. Efficacy of a lower dose. Clin. Pharmacol. Ther. 1978. 24(2). 192-198.
15. Psaty B.M., Smith N.L., Siscovick D.S. et al. Health outcomes associated with antihypertensive therapies used as first-line agents. A systematic review and meta-analysis. JAMA. 2004. 277. 739 -745.
16. Ernst M.E., Carter B.L., Goerdt C.J. et al. Comparative antihypertensive effects of hydrochlorothiazide and chlorthalidone on ambulatory and office blood pressure. Hypertension. 2006. 47. P. 352-358.
17. Pareek A.K., Messerli F.H., Chandurkar N.B. et al. Efficacy of Low-Dose Chlorthalidone and Hydrochlorothiazide as Assessed by 24-h Ambulatory Blood Pressure Monitoring. J. Am. Coll. Cardiol. 2016. 67(4). 379-389.
18. Roush G.C., Ernst M.E., Kostis J.B., Tandon S., Sica D.A. Head-to-head comparisons of hydrochlorothiazide with indapamide and chlorthalidone: antihypertensive and metabolic effects. Hypertension. 2015. 65(5). 1041-1046.
19. Fernandes L.A., Cestario E.D., Cosenso-Martin L.N. et al. Chlorthalidone Plus Amiloride Reduces the Central Systolic Blood Pressure in Stage 1 Hypertension Patients. Cardiol. Res. 2016. 6. 196-201.
20. Multiple Risk Factor Intervention Trial Research Group. Mortality after 10 1/2 years for hypertensive participants in the Multiple Risk Factor Intervention Trial. Circulation. 1990. 82(5). 1616-28.
21. Dorsch M.P., Gillespie B.W., Erickson S.R. et al. Chlorthalidone reduces cardiovascular events compared with hydrochlorothiazide: a retrospective cohort analysis. Hypertension. 2011. 57. P. 689-694.
22. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial: Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA. 2002. 288. 2981-2997.
23. Black H.R., Davis B., Barzilay J. et al for Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial. Metabolic and clinical outcomes in nondiabetic individuals with the metabolic syndrome assigned to chlorthalidone, amlodipine, or lisinopril as initial treatment for hypertension: a report from the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). Diabetes Care. 2008. 31(2). 353-360.
24. Barzilay J.I., Davis B.R., Cutler J.A. et al. for ALLHAT Collaborative Research Group. Fasting glucose levels and incident diabetes mellitus in older nondiabetic adults randomized to receive 3 different classes of antihypertensive treatment: a report from the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). Arch. Intern. Med. 2006. 166(20). 2191-2201.
25. Kostis J.B., Wilson A.C., Freudenberger R.S. et al. Long-term effect of diuretic-based therapy on fatal outcomes in subjects with isolated systolic hypertension with and without diabetes. Am. J. Cardiol. 2005. Vol. 95. P. 29-35.
26. Wright J.T. Jr, Probstfield J.L., Cushman W.C. et al. ALLHAT findings revisited in the context of subsequent analyses, other trials, and meta-analyses. Archives of Internal Medicine. 2009. 169(9). 832-842.
27. Barzilay J.I., Davis B.R., Pressel S.L. et al. ALLHAT Collaborative Research Group. Long-term effects of incident diabetes mellitus on cardiovascular outcomes in people treated for hypertension: the ALLHAT Diabetes Extension Study. Circ. Cardiovasc. Qual. Outcome. 2012. 5. 153-162.
28. Rahman M., Pressel S., Davis B.R. et al. for the ALLHAT Collaborative Research Group. Cardiovascular Outcomes in High-Risk Hypertensive Patients Stratified by Baseline Glomerular Filtration Rate. Ann. Intern. Med. 2006. 144. 172-180.
29. Agarwal R., Sinha A.D., Pappas M.K., Ammous F. Chlorthalidone for poorly controlled hypertension in chronic kidney disease: an interventional pilot study. Am. J. Nephrol. 2014. 39(2). 171-182.
30. Alderman M.H., Davis B.R., Piller L.B. et al. for ALLHAT Collaborative Research Group. Should Antihypertensive Treatment Recommendations Differ in Patients With and Without Coronary Heart Disease? (from the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial [ALLHAT]). Am. J. Cardiol. 2016. 117(1). 105-115.
31. Williams B., Mancia G., Spiering W. et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. J. Hypertens. 2018. 36. 1953-2041.
32. Bangalore S., Davis B.R., Cushman W.C. et al. for ALLHAT Collaborative Research Group. Treatment-Resistant Hypertension and Outcomes Based on Randomized Treatment Group in ALLHAT. Am. J. Med. 2017. 130(4). 439-448.e9.
33. Carey R.M., Calhoun D.A., Bakris G.L. et al. American Heart Association Professional/Public Education and Publications Committee of the Council on Hypertension; Council on Cardiovascular and Stroke Nursing; Council on Clinical Cardiology; Council on Genomic and Precision Medicine; Council on Peripheral Vascular Disease; Council on Quality of Care and Outcomes Research; and Stroke Council. Resistant Hypertension: Detection, Evaluation, and Management: A Scientific Statement From the American Heart Association. Hypertension. 2018. 72(5). e53-e90.
34. Davis B.R., Kostis J.B. et al. for ALLHAT Collaborative Research Group. Heart failure with preserved and reduced left ventricular ejection fraction in the antihypertensive and lipid-lowering treatment to prevent heart attack trial. Circulation. 2008. 25. 118(22). 2259-2267.
35. Puttnam R., Davis B.R., Pressel S.L. et al. for ALLHAT Collaborative Research Group. Association of 3 Different Antihypertensive Medications With Hip and Pelvic Fracture Risk in Older Adults: Secondary Analysis of a Randomized Clinical Trial. JAMA Intern. Med. 2017. 177(1). 67-76.
36. Alderman M.H., Piller L.B., Ford C.E. et al. for Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial Collaborative Research Group. Clinical significance of incident hypokalemia and hyperkalemia in treated hypertensive patients in the antihypertensive and lipid-lowering treatment to prevent heart attack trial. Hypertension. 2012. 59(5). 926-933.
37. https://www.pdr.net/drug-summary/Chlorthalidone-chlorthalidone-1961.605.
38. https://clincalc.com/DrugStats/Drugs/Chlorthalidone.
39. https://www.ehealthme.com/drug/chlorthalidone/side-effects.
/18.jpg)
/23.jpg)
/23_2.jpg)
/27_2.jpg)

/16.jpg)
/17.jpg)
/19.jpg)
/20.jpg)
/20_2.jpg)
/21.jpg)
/21_2.jpg)
/24.jpg)
/25.jpg)
/25_2.jpg)
/26.jpg)
/26_2.jpg)
/27.jpg)
/27_3.jpg)
/28.jpg)
/29.jpg)
/29_2.jpg)
/30.jpg)
/30_2.jpg)