Резюме
Актуальність. За даними Всесвітньої організації охорони здоров’я, у світі більше 2 мільйонів дітей віком до п’яти років щорічно вмирають від пневмонії, що становить майже 1 із 5 випадків смерті. Мета дослідження: розроблення математичної моделі для визначення ймовірності розвитку вродженої пневмонії у недоношених новонароджених із низькою масою тіла експрес-методом. Матеріали та методи. Проведено комплексне обстеження 171 новонародженого, які перебували в пологовому фізіологічному відділенні, відділенні анестезіології та реанімації (з палатами для новонароджених дітей) та педіатричному відділенні для недоношених новонароджених ДУ «РНПЦ «Мати і дитя». Результати. Проведено порівняльний аналіз понад 200 даних анамнезу життя, результатів попередніх вагітностей, ускладнень теперішньої вагітності у матерів, клінічних та лабораторних методів дослідження в новонароджених у перші три доби життя. У подальшому визначені найбільш значущі фактори, асоційовані з розвитком уродженої пневмонії в недоношених новонароджених із низькою масою тіла. Проведено математичний аналіз понад 380 млн зв’язків змінних. У результаті проведеного обстеження порівняно з групою порівняння і контрольною групою встановлені найбільш значущі фактори: з акушерсько-гінекологічного та соматичного анамнезу життя матері — вагітність (ОR = 13,46 (10,11–17,91); ОR = 32,72 (24,76–43,22)) і мимовільний викидень (ОR = 3,79 (2,69–5,35); ОR = 19,19 (14,57–25,26)); з ускладнень теперішньої вагітності — хронічна фетоплацентарна недостатність (ОR = 3,47 (2,48–4,87); ОR = 38,29 (28,78–50,91)), синдром затримки розвитку плода (ОR = 11,56 (8,70–15,35)) і загроза переривання вагітності (ОR = 2,73 (1,76–4,23); ОR = 3,96 (2,51–6,25)); за результатами клінічних проявів у немовляти в перші три доби життя — дихальної недостатності тяжкого ступеня (ОR = 6,90 (5,01–9,49)). На підставі отриманих даних розроблена математична модель із чутливістю, що дорівнює 76,4 %, специфічністю — 83,0 % і площею під ROC-кривою AUC = 0,840 ± 0,056 (0,76–0,91), р < 0,001. Висновки. За допомогою моделі розраховані порогові значення: для вагітності, що не розвивається, — 0,769, мимовільного викидня — 0,493, хронічної фетоплацентарної недостатності — 0,366, синдрому затримки розвитку плода — 0,334, загрози переривання вагітності — 0,283, дихальної недостатності III ступеня — 0,703, що при порогових значеннях ≥ 0,49 дозволяє виділити групу високого ризику щодо розвитку вродженої пневмонії серед недоношених новонароджених із низькою масою тіла.
Актуальность. По данным Всемирной организации здравоохранения, в мире более 2 миллионов детей в возрасте до пяти лет ежегодно умирают от пневмонии, что составляет почти 1 из 5 случаев смерти. Цель исследования: разработка математической модели для определения вероятности развития врожденной пневмонии у недоношенных новорожденных с низкой массой тела экспресс-методом. Материалы и методы. Проведено комплексное обследование 171 новорожденного, находившегося в родильном физиологическом отделении, отделении анестезиологии и реанимации (с палатами для новорожденных детей) и педиатрическом отделении для недоношенных новорожденных ГУ «РНПЦ «Мать и дитя». Результаты. Проведен сравнительный анализ более 200 данных анамнеза жизни, исходов предыдущих беременностей, осложнений настоящей беременности у матерей, клинических и лабораторных методов исследования у новорожденных в первые трое суток жизни. В последующем определены наиболее значимые факторы, ассоциированные с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела. Проведен математический анализ более 380 млн связей переменных. В результате проведенного обследования в сопоставлении с группой сравнения и контрольной группой установлены наиболее значимые факторы: из акушерско-гинекологического и соматического анамнеза жизни матери — неразвивающаяся беременность (ОR = 13,46 (10,11–17,91); ОR = 32,72 (24,76–43,22)) и самопроизвольный выкидыш (ОR = 3,79 (2,69–5,35); ОR = 19,19 (14,57–25,26)); из осложнений настоящей беременности — хроническая фетоплацентарная недостаточность (ОR = 3,47 (2,48–4,87); ОR = 38,29 (28,78–50,91)), синдром задержки развития плода (ОR = 11,56 (8,70–15,35)) и угроза прерывания беременности (ОR = 2,73 (1,76–4,23); ОR = 3,96 (2,51–6,25)); по результатам клинических проявлений у младенца в первые трое суток жизни — дыхательная недостаточность тяжелой степени (ОR = 6,90 (5,01–9,49)). На основании полученных данных разработана математическая модель с чувствительностью, равной 76,4 %, специфичностью — 83,0 % и площадью под ROC-кривой AUC = 0,840 ± 0,056 (0,76–0,91), р < 0,001. Выводы. С помощью модели рассчитаны пороговые значения: для неразвивающейся беременности — 0,769, самопроизвольного выкидыша — 0,493, хронической фетоплацентарной недостаточности — 0,366, синдрома задержки развития плода — 0,334, угрозы прерывания беременности — 0,283, дыхательной недостаточности III степени — 0,703, что при пороговых значениях ≥ 0,49 позволяет выделить группу высокого риска по развитию врожденной пневмонии среди недоношенных новорожденных с низкой массой тела.
Background. According to the World Health Organization, more than 2 million children under the age of five die from pneumonia every year, accounting for almost 1 in 5 deaths. Therefore, the aim of the study was to develop a mathematical model for determining the probability of developing congenital pneumonia in premature infants with low body weight by the express method. Materials and methods. A comprehensive examination of 171 newborns who stayed at the maternity physiology department, the department of anesthesiology and resuscitation (with wards for newborns) and the pediatric department for premature newborns of the State Institution “Republican Scientific and Practical Center “Mother and Child” was conducted. Results. A comparative analysis was carried out of more than 200 life history data, outcomes of previous pregnancies, complications of present pregnancy and clinical and laboratory methods of research in newborns in the first three days of life. Subsequently, the most significant factors associated with the development of congenital pneumonia in premature infants with low body weight were determined. The mathematical analysis of more than 380 million connections of variables is carried out. As a result of the survey, compared with the comparison group and the control group, the most significant factors were established: from the obstetric-gynecological and somatic history of the mother’s life — non-developing pregnancy (odds ratio (OR) = 13.46 (10.11–17.91); OR = 32.72 (24.76–43.22)) and spontaneous miscarriage (OR = 3.79 (2.69–5.35); OR = 19.19 (14.57–25.26)); from the complications of a present pregnancy — chronic fetoplacental insufficiency (OR = 3.47 (2.48–4.87); OR = 38.29 (28.78–50.91)), intrauterine growth restriction syndrome (OR = 11.56 (8.70–15.35)) and the threatened miscarriage (OR = 2.73 (1.76–4.23); OR = 3.96 (2.51–6.25)); according to the results of clinical manifestations in infant in the first three days of life — severe respiratory failure (OR = 6.90 (5.01–9.49)). Based on the obtained data, a mathematical model was developed with a sensitivity of 76.4 %, specificity — 83.0 %, and the area under the ROC curve = 0.840 ± 0.056 (0.76–0.91), p < 0.001. Conclusions. Using the model, threshold values were calculated: for non-developing pregnancy — 0.769, spontaneous miscarriage — 0.493, chronic fetoplacental insufficiency — 0.366, intrauterine growth restriction syndrome — 0.334, threatened miscarriage — 0.283, respiratory failure degree III — 0.703, which at the threshold values ≥ 0.49 allows us to single out a high-risk group for the development of congenital pneumonia among premature infants with low body weight.
Введение
По данным Всемирной организации здравоохранения, в мире более 2 миллионов детей в возрасте до пяти лет ежегодно умирают от пневмонии, что составляет почти 1 из 5 случаев смерти. Во всем мире от пневмонии умирает больше детей, чем от вируса иммунодефицита человека, малярии и кори, вместе взятых. В совместном докладе ЮНИСЕФ ежегодно рассматриваются эпидемиологические данные о распространении пневмонии, а также дается оценка текущего состояния лечения и профилактики. Это призыв к действиям по снижению смертности от пневмонии, что является ключевым шагом на пути к достижению цели развития тысячелетия [1].
Цель исследования — разработать математическую модель для определения вероятности развития врожденной пневмонии у недоношенных новорожденных с низкой массой тела экспресс-методом.
Материалы и методы
Проведено обследование 171 новорожденного, находившихся в родильном физиологическом отделении, отделении анестезиологии и реанимации (с палатами для новорожденных детей) и педиатрическом отделении для недоношенных новорожденных Государственного учреждения «Республиканский научно-практический центр «Мать и дитя» (ГУ «РНПЦ «Мать и дитя»). Дети поступали на лечение и выхаживание из 22 роддомов и отделений анестезиологии и реанимации учреждений здравоохранения Республики Беларусь в период с 2017 по 2019 г.
Тип исследования — случай — контроль. Все новорожденные были разделены на три группы.
Исследуемую группу составили 55 новорожденных с низкой массой тела при рождении, синдромом дыхательных расстройств и врожденной пневмонией, родившихся в сроке гестации Ме = 35,0 (33,0–36,0) недели, с массой тела Ме = 2080,0 (1870,0–2420,0) г, длиной тела Ме = 45,0 (42,0–46,0) см, окружностью головы Ме = 31,0 (31,0–33,0) см, окружностью груди Ме = 30,0 (28,0–31,0) см.
В группу сравнения вошли 53 условно здоровых недоношенных с низкой массой тела при рождении и синдромом дыхательных расстройств, родившиеся в сроке гестации Ме = 35,0 (35,0–36,0) недели, с массой тела Ме = 2300,0 (2140,0–2400,0) г, длиной тела Ме = 45,0 (45,0–47,0) см, окружностью головы Ме = 32,0 (31,0–33,0) см, окружностью груди Ме = 30,0 (29,0–32,0) см.
При оценке показателей физического развития и срока гестации недоношенных новорожденных с низкой массой тела обеих групп статистически значимых различий не выявлено.
Контрольную группу составили 63 здоровых доношенных новорожденных, родившиеся в сроке гестации Ме = 39,0 (39,0–40,0) недели, с массой тела Ме = 3370,0 (3250,0–3620,0) г, длиной тела Ме = 52,0 (52,0–53,0) см, окружностью головы Ме = 35,0 (34,0–36,0) см, окружностью груди Ме = 34,0 (33,0–34,0) см.
Критерии постановки диагноза «врожденная пневмония»: клинические и лабораторные данные, наличие инфильтративных теней на рентгенограмме легких в первые 72 часа жизни. Критериями исключения являлись: антенатально выявленные пороки развития, наличие генетических заболеваний и хромосомной патологии, рождение в результате применения вспомогательных репродуктивных технологий.
Проведен анализ анамнестических данных матерей обследованных детей: возраст, количество и исходы предыдущих беременностей, наличие гинекологических заболеваний и экстрагенитальной патологии, особенности течения беременности и родов.
Средний возраст матерей новорожденных исследуемой группы составил 30,60 ± 4,94 (29,2–31,9) года, возраст женщин группы сравнения — 30,70 ± 5,71 (29,1–32,3) года, в контрольной группе — 31,00 ± 4,75 (29,8–32,1) года. Статистически значимых различий между группами не выявлено.
Статистическая обработка данных выполнялась с помощью пакета программ Statistica 10 и Microsoft Excel. Нормальность распределения количественных признаков оценивалась тестами Колмогорова — Смирнова и Лиллиефорса. При нормальном распределении величин рассчитывалось среднее и его среднеквадратичное отклонение (М ± SD) с указанием доверительного интервала (± 95,5% ДИ), критерий Стьюдента (t). При отличном от нормального — медиана (Ме) и интерквартильный размах (25–75 %), критерий Манна — Уитни (U). Для определения статистически значимых различий качественных величин использовался хи-квадрат Пирсона (χ2), уточняющий критерий с поправкой Йетса (χ2Й) или точный критерий Фишера (F), уточняющий критерий — Фишер двусторонний (Fдв). При статистически значимых различиях проводился расчет отношения шансов (ОR) с доверительным интервалом (± 95% ДИ). Различия считали статистически значимыми при р < 0,05 [2, 3].
Прогностическая ценность факторов, ассоциированных с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела, оценивалась с помощью бинарной логистической регрессии, анализа ROC-кривой, отрицательного удвоенного логарифма функции правдоподобия (–2LL) и меры определенности (R2 Нэйджелкерка). Использование данных для построения модели основывалось на гипотезе, объеме выборки и отсутствии между факторами статистически значимых корреляционных связей [4].
Работа выполнена в рамках проекта Белорусского республиканского фонда фундаментальных исследований № М17-002, сроки выполнения 18.04.2017 — 31.03.2019.
Карты обследования новорожденных детей и информированное согласие для выполнения исследований утверждены на заседании комиссии по медицинской этике ГУ «Республиканский научно-практический центр «Мать и дитя».
На всех обследованных новорожденных получено информированное согласие от законных представителей (мать или отец).
Результаты и обсуждение
На основании анамнеза перенесенных матерями заболеваний, данных акушерско-гинекологического и соматического статуса проведена оценка по наиболее часто встречаемым факторам: пиелонефрит, самопроизвольный выкидыш, вакуумный аборт, неразвивающаяся беременность, медикаментозный аборт, гипотиреоз, хронический тонзиллит, хронический гастрит, герпес, миопия. По результатам отношения шансов наиболее статистически значимыми факторами у матерей новорожденных исследуемой группы в сопоставлении с данными группы сравнения и контрольной группы доля женщин с неразвивающейся беременностью (НБ) (Fдв = 0,15, р < 0,001, ОR = 13,46 (10,11–17,91); Fдв = 0,19, р < 0,001, ОR = 32,72 (24,76–43,22)) и самопроизвольным выкидышем (СВ) (Fдв = 0,05, р = 0,033, ОR = 3,79 (2,69–5,35); Fдв = 0,12, р < 0,001, ОR = 19,19 (14,57–25,26)) была статистически значимо больше [5–8].
Из осложнений настоящей беременности анализ проводился по следующим факторам: хроническая внутриматочная гипоксия плода, хроническая фетоплацентарная недостаточность, пиелонефрит беременной, эрозия шейки матки, синдром задержки развития плода, изменение объема околоплодных вод (мало- или многоводие), гестоз, кольпит, острые респираторные инфекции, анемия беременной, истмико-цервикальная недостаточность, угроза прерывания. Выявлено, что у матерей новорожденных исследуемой группы по сравнению с матерями младенцев из группы условно здоровых детей и группы контроля статистически значимо чаще наблюдались синдром задержки развития плода (СЗРП) (F = 0,07, р = 0,005, ОR = 11,56 (8,70–15,35)), хроническая фетоплацентарная недостаточность (ХФПН) (χ2Й = 6,20, р = 0,013, ОR = 3,47 (2,48–4,87); Fдв = 0,22, р < 0,001, ОR = 38,29 (28,78–50,91)), угроза прерывания беременности (УПБ) (χ2Й = 5,36, р = 0,021, ОR = 2,73 (1,76–4,23); χ2Й = 11,42, р < 0,001, ОR = 3,96 (2,51–6,25)) [5–13].
Проведен сравнительный анализ постнатальных факторов, ассоциированных с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела. Проведен анализ клинических проявлений и лабораторных данных в первые 72 часа жизни новорожденного ребенка.
При анализе оценки по шкале Апгар у 14 (25,5 %) недоношенных новорожденных исследуемой группы по сравнению с 6 (11,3 %) младенцами группы сравнения в первые минуты жизни отмечалась умеренная асфиксия, что не имело статистически значимых различий. У здоровых доношенных группы контроля случаи асфиксии не зарегистрированы.
Осложнением врожденной пневмонии у всех детей исследуемой группы являлась дыхательная недостаточность (ДН) I степени — у 12 (21,8 %), II степени — у 18 (32,7 %) и III степени — у 25 (45,5 %) младенцев. В группе сравнения: ДН I степени наблюдалась у 34 (64,2 %), II степени — у 11 (20,8 %) и III степени — у 2 (3,8 %) младенцев, 6 (11,3 %) недоношенных новорожденных ДН не имели. В контрольной группе ДН I степени на первые сутки отмечалась у 2 (3,2 %) доношенных новорожденных. Таким образом, доля недоношенных детей исследуемой группы, имеющих ДН III степени, была статистически значимо больше, чем в группе условно здоровых новорожденных (F = 0,23, р < 0,001, ОR = 21,25 (15,69–28,77)).
В связи с тяжестью состояния 23 (41,8 %) младенцам с врожденной пневмонией в первые сутки жизни проводилась искусственная вентиляция легких (ИВЛ), что статистически более часто, чем 5 (9,4 %) случаев в группе сравнения (χ2 = 14,74, р < 0,001, ОR = 6,90 (5,01–9,49)) и 0 (0,0 %) — в группе контроля. На фоне проводимой ИВЛ 21 (38,2 %) недоношенному младенцу потребовалось введение сурфактантсодержащих лекарственных средств. Дети группы сравнения и контрольной группы в данном виде лечения не нуждались.
Проведен сравнительный анализ гематологических показателей у младенцев исследуемой группы и группы сравнения в первые трое суток жизни. По данным биохимических показателей у недоношенных новорожденных статистически значимых различий не выявлено. В анализе периферической крови у новорожденных исследуемой группы по сравнению с группой условно здоровых регистрировались статистически значимо более низкие уровни эритроцитов (р = 0,025) на фоне более высоких значений среднего объема эритроцита (р = 0,014) и среднего содержания гемоглобина в эритроците (р < 0,001) [14–18].
В последующем определены наиболее значимые факторы, ассоциированные с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела. На основании бинарной логистической регрессии и ROC-анализа выведена математическая модель с универсальным критерием коэффициента χ2 = 46,84, р < 0,001, что свидетельствует о ее высокой статистической значимости. При выборе модели учитывался объем выборки, отсутствие между факторами статистически значимых корреляционных связей и возможность включения факторов в зависимости от числа наблюдений (табл. 1).
Для представления работоспособности разработанной математической модели в табл. 2 приведены параметры с указанием отрицательного удвоенного логарифма функции правдоподобия и меры определенности [4].
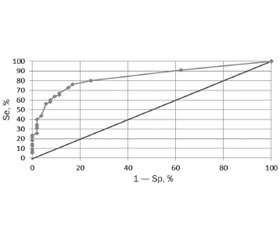
ROC-кривая, являясь графической характеристикой качества бинарного классификатора, показывает зависимость доли верных положительных результатов от доли ложных положительных результатов при варьировании оптимального порога. На данной кривой оптимальный порог ≥ 0,49. Следовательно, пороговые значения (≥ 0,49) показывают высокую вероятность наличия врожденной пневмонии у недоношенных новорожденных с низкой массой тела.
Для данной модели определена чувствительность и специфичность. Чувствительность, отражающая долю положительных результатов, которые правильно идентифицированы как больные, была равна 76,4 %. Специфичность, отражающая долю отрицательных результатов, которые правильно идентифицированы как здоровые, — 83,0 %, с площадью под ROC-кривой AUC = 0,84 ± 0,056 (0,76–0,91), р < 0,001 (рис. 1).
/35_2.jpg)
При расчете прогностической модели получены пороговые данные для наиболее значимых факторов, ассоциированных с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела: из анамнеза жизни матери — неразвивающаяся беременность с пороговым значением 0,769 и самопроизвольный выкидыш (0,493); из осложнений настоящей беременности — хроническая фетоплацентарная недостаточность с пороговым значением 0,366, синдром задержки развития плода (0,334) и угроза прерывания беременности (0,283); по результатам клинических и лабораторных данных у младенца в первые трое суток жизни — наличие дыхательной недостаточности III степени с пороговым значением 0,703.
Выводы
1. В результате проведенного обследования установлены наиболее значимые факторы, ассоциированные с развитием врожденной пневмонии у недоношенных новорожденных с низкой массой тела: из акушерско-гинекологического и соматического анамнеза жизни матери — неразвивающаяся беременность и самопроизвольный выкидыш; из осложнений настоящей беременности — хроническая фетоплацентарная недостаточность, синдром задержки развития плода и угроза прерывания беременности; по результатам клинических проявлений у младенца в первые трое суток жизни — дыхательная недостаточность тяжелой степени.
2. С помощью прогностической модели рассчитаны пороговые значения: для неразвивающейся беременности — 0,769, самопроизвольного выкидыша — 0,493, хронической фетоплацентарной недостаточности — 0,366, синдрома задержки развития плода — 0,334, угрозы прерывания беременности — 0,283, дыхательной недостаточности III степени — 0,703, что при пороговых значениях ≥ 0,49 позволяет выделить группу высокого риска по развитию врожденной пневмонии среди недоношенных новорожденных с низкой массой тела.
Получено/Received 17.02.2021
Рецензировано/Revised 01.03.2021
Принято в печать/Accepted 12.03.2021
Список литературы
1. Pneumonia: the forgotten killer of children. Информационный бюллетень ВОЗ [Электронный ресурс]. Режим доступа: https://www.who.int/maternal_child_adoles-cent/documents/9280640489/en. Дата доступа: 27.01.2021.
2. Ланг Т.А., Сесик М. Как описать статистику в медицине. Аннотированное руководство для авторов, редакторов и рецензентов: Пер. с англ. под ред. В.П. Леонова. М.: Практическая медицина, 2011. 480 с.
3. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ Statistica. М.: МедиаСфера, 2002. 312 с.
4. Петри А., Сэбин К. Наглядная медицинская статистика: учеб. пособие. Пер. с англ. под ред. В.П. Леонова. 3-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2015. 216 с.
5. Bhutta Z.A. Interventions to address deaths from childhood pneumonia and diarrhoea equitably: what works and at what cost? The Lancet. 2013. № 9875. P. 1417-1429.
6. Косьянчук А.В. Инфекционный фактор у женщин с неразвивающейся беременностью и хроническим эндометритом: материалы X cъезда акушеров-гинекологов и неонатологов Республики Беларусь. Минск, 9–10 ноября 2017 г. Репродуктивное здоровье. Восточная Европа. 2017. № 5. С. 791-795.
7. Gill C.J. Bottlenecks, barriers, and solutions: results from multicountry consultations focused on reduction of childhood pneumonia and diarrhoea deaths. The Lancet. 2013. № 9876. P. 1487-1498.
8. Можейко Л.Ф. Невынашивание беременности: учеб.-метод. пособие. Минск: БГМУ, 2013. 38 с.
9. McGuire W. Infection in the preterm infant. BMJ. 2004. Vol. 2. P. 329-341.
10. Мудров В.А. Возможности модификации способов определения объема околоплодных вод. Журнал акушерства и женских болезней. 2016. № 34. С. 12-17.
11. Малевич Ю.К., Шостак В.А. Фетоплацентарная недостаточность. Беларусь, 2007. 157 с.
12. Савельева Г.М., Федорова М.В., Клименко П.А. и др. Плацентарная недостаточность. М.: Медицина, 1991. 272 с.
13. Тютюнник В.Л. Хроническая плацентарная недостаточность при бактериальной и вирусной инфекции (патогенез, диагностика, профилактика, лечение): Автореф. дис… д-ра мед. наук. М., 2002. 46 с.
14. Антонов А.Г., Байбарина Е.Н., Балашов Е.Н., Зубков В.В., Иванов Д.О., Ионов О.В. [и др.]. Врожденная пневмония: клинические рекомендации. Под ред. Д.Д. Дегтярева. Неонатология. Новости, мнения, обучение. 2017. № 4 (18). С. 133-148.
15. Володин Н.Н. Детские болезни. Т. 1. Неонатология. Под ред. Н.Н. Володина, Ю.Г. Мухиной, А.И. Чубаровой. М.: Династия, 2011. 512 с.
16. Шабалов Н.П. Неонатология: Учеб. пособие. В 2 т. 3-е изд., испр. и доп. М.: МЕДпресс-информ, 2004. Т. I. 608 с.
17. Сукало А.В., Бовбель И.Э. Справочник по поликлинической педиатрии. Национальная академия наук Беларуси. Минск: Бел. навука, 2015. 313 с.
18. Рооз Р., Генцель-Боровичени О., Прокитте Г.М. Практические рекомендации: Пер. с нем. Медицинская литература, 2011. 592 с.
/35_2.jpg)

/35.jpg)