Резюме
Актуальність. Загоєння ран у ділянці грудини має свої особливості, що найбільш актуально, оскільки серединна стернотомія є основним оперативним доступом у кардіоторакальній хірургії. Локальні інфекційні ускладнення ран у цій зоні виникають у 0,4–6 % хворих. Мета — порівняльна оцінка ефективності двоетапного й одноетапного тактичного підходу до пластичного закриття ускладнених стернальних ран на основі активної хірургічної тактики і локального вакуумного дренування. Матеріали та методи. Нами узагальнені результати лікування 11 хворих з ускладненнями ран у ділянці грудини. 9 пацієнтів були прооперовані у відділеннях кардіохірургії, 1 військовослужбовець отримав мінно-вибухове поранення і 1 хвора — високовольтний електроопік. Результати. У всіх хворих ми використали активну хірургічну тактику. Вибір здійснювали залежно від характеру і глибини ураження тканин. Для прискорення очищення рани та підготовки її до пластичного закриття в 2-й групі застосовували терапію локальним негативним тиском. У нашій практиці ми частіше використовували розрідження 70–90 мм рт.ст. Застосування надмірного розрідження на поверхні середостіння потенційно небезпечне вентиляційними порушеннями. Активуються обмінні процеси, полегшується міграція фагоцитарних клітин, прискорюються грануляційні процеси, неоваскулогенез. Використання вакуум-терапії останнім часом сприяло оптимізації перебігу ранового процесу порівняно з пацієнтами 2-ї групи. Але щодо зменшення бактеріального обсіменіння статистично значущого поліпшення не відзначили. Вирішальне значення для вибору клаптя при закритті дефекту м’яких тканин мають знання кровопостачання донорської зони покривних тканин й анатомічної характеристики дефекту. Як правило, використовували комбіновану пластику дефекту за рахунок мобілізації великих грудних м’язів і місцевих ковзаючих або острівцевих шкірно-фасціальних клаптів. До моменту виписки повного загоєння рани передньої грудної стінки домоглися у 81,8 % хворих. Висновки. При використанні вакуум-терапії в пацієнтів з інфекційними ускладненнями стернальних ран знижується ризик виникнення рецидивів і скорочуються терміни лікування. Сьогодні існує необхідність проведення подальших досліджень для оптимізації вибору методу і термінів проведення реконструктивних міопластичних втручань.
Актуальность. Заживление ран в области грудины имеет свои особенности, что наиболее актуально, так как срединная стернотомия является основным оперативным доступом в кардиоторакальной хирургии. Локальные инфекционные осложнения ран в этой зоне возникают у 0,4–6 % больных. Цель — сравнительная оценка эффективности двухэтапного и одноэтапного тактического подхода к пластическому закрытию осложненных стернальных ран на основе активной хирургической тактики и локального вакуумного дренирования. Материалы и методы. Нами обобщены результаты лечения 11 больных с осложнениями ран в области грудины. 9 пациентов перенесли операции в отделениях кардиохирургии, 1 военнослужащий получил минно-взрывное ранение и 1 больная — высоковольтный электроожог. Результаты. У всех больных мы использовали активную хирургическую тактику. Выбор осуществляли в зависимости от характера и глубины поражения тканей. Для ускорения очищения раны и подготовки ее к пластическому закрытию во 2-й группе применяли терапию локальным отрицательным давлением. В нашей практике мы чаще использовали разрежение 70–90 мм рт.ст. Применение избыточного разрежения на поверхности средостения потенциально опасно вентиляционными нарушениями. Активируются обменные процессы, облегчается миграция фагоцитарных клеток, ускоряются грануляционные процессы, неоваскулогенез. Использование вакуум-терапии в последние годы способствовало оптимизации течения раневого процесса по сравнению с пациентами 2-й группы. Но в отношении уменьшения бактериальной обсемененности статистически значимого улучшения не отметили. Решающее значение для выбора лоскута при закрытии дефекта мягких тканей имеют знание кровоснабжения донорской зоны покровных тканей и анатомической характеристики дефекта. Как правило, использовали комбинированную пластику дефекта за счет мобилизации больших грудных мышц и местных скользящих или островковых кожно-фасциальных лоскутов. К моменту выписки полного заживления раны передней грудной стенки добились у 81,8 % больных. Выводы. При использовании вакуум-терапии у пациентов с инфекционными осложнениями стернальных ран снижается риск возникновения рецидивов и сокращаются сроки лечения. В настоящее время существует необходимость проведения дальнейших исследований для оптимизации выбора метода и сроков проведения реконструктивных миопластических вмешательств.
Background. The healing of wounds in the sternum has its own characteristics, which is most relevant, since the median sternotomy is the main operative approach in cardiothoracic surgery. Local infectious complications of wounds in this zone occur in 0.4–6 % of patients. The basic purpose is to evaluate the effectiveness of two-stage in comparison with the one-stage method of plastic closure of complicated sternal wounds based on the active surgical approach to their treatment and the use of local vacuum drainage. Materials and methods. The description of the early sternomediastinitis after cardiothoracic and trauma surgery in 11 patients. Results. Complication was the cause for using open method of management with negative pressure therapy in combination with antibacterial treatment. Foam sponge was used as absorbent material. Negative pressure of 70–90 mmHg was created using aspirator. The bandage was changed every 3–4 days. A rapid growth of granulating tissue, a significant reduction in the wound surface, and an improvement in the patient’s emotional state were noted. Discharge from the hospital in a satisfactory condition occurred on the 14th day after the beginning of the use of vacuum drainage system. The dependence of lipid peroxidation activation on the severity of exudative and destructive inflammation manifestations has been established, thereby suggesting the possibility of using the values of free radical oxidation as markers. The application of skin grafts or flaps were required due to complete wound closure with granulations with the formation of a full scab of the anterior thoracic wall. Conclusions. When using vacuum therapy in patients with infectious complications of sternal wounds, the risk of recurrence and the duration of treatment are reduced.
Введение
Заживление ран в области грудины имеет свои особенности, что наиболее актуально, так как срединная стернотомия является основным оперативным доступом в кардиоторакальной хирургии. Локальные инфекционные осложнения ран в этой зоне возникают у 0,4–6 % больных, проявляясь в виде несостоятельности швов грудины, медиастинита и остеомиелита с формированием свищей, развитием хондрита реберных хрящей и сепсиса [1]. Факторы риска развития гнойных осложнений делят на дооперационные (пол, возраст, сопутствующая патология), интраоперационные (асимметричная стернотомия, метод ушивания стернотомного доступа, продолжительность операции, использование внутренней грудной артерии, кровопотеря, использование аппарата искусственного кровообращения) и послеоперационные (нестабильность либо ишемия грудины, рестернотомия, наличие инородных тел, послеоперационные кровотечения и гематомы) [2]. Лечение таких больных требует комплексного подхода, включающего консервативные и оперативные мероприятия. Своевременное дренирование раны и ее очищение с последующим ушиванием являются базисом современной тактики, а анализ индивидуальных особенностей течения раневого процесса позволяет разработать лечебные мероприятия с учетом распространения процесса и стадии его развития [3].
Цель — сравнительная оценка эффективности двухэтапного и одноэтапного тактического подхода к пластическому закрытию осложненных стернальных ран на основе активной хирургической тактики и локального вакуумного дренирова–ния.
Материалы и методы
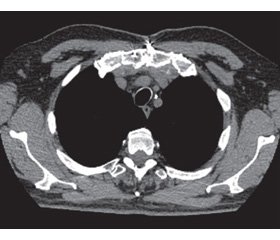
Нами обобщены результаты лечения 11 больных с осложнениями ран в области грудины, поступивших в ожоговое отделение после лечения в клиниках Донецка, Днепра, Киева, Краматорска. 9 пациентов перенесли операции в отделениях кардиохирургии, 1 военнослужащий 38 лет получил минно-взрывное ранение и 1 больная — высоковольтный электроожог. Возраст больных, оперированных по поводу кардиохирургических патологий, составил от 4 до 67 лет. У всех них были сопутствующая патология, осложненный кардиологический анамнез, у 3 пациентов — приобретенные пороки сердца, у 5 — стенокардия (у 3 больных — перенесенный в анамнезе инфаркт), у 1 пациентки инфаркт миокарда отмечен дважды. Один ребенок перенес операцию по поводу врожденного порока сердца. Сахарным диабетом второго типа страдали 2 больных. Среди кардиохирургических операций в 5 случаях выполнялось аортокоронарное шунтирование (рис. 1), использовалась внутренняя грудная артерия, в 3 случаях — операции на аортальном и в 1 — на митральном клапанах.
/62-1.jpg)
Средняя длительность лечения при первичной госпитализации составила 29,5 ± 12,6 дня, при повторной госпитализации — 32,5 ± 9,7 дня. У всех больных отмечались незажившие раны в области грудины, а структура осложнений была следующая: острый послеоперационный остеомиелит грудины, свищевая форма — у 7; острый послеоперационный стерномедиастинит — у 1; хронический послеоперационный остеомиелит грудины, свищевая форма — у 2; хронический остеомиелит ребер — у 1.
При повторной госпитализации у наблюдаемых больных (n = 3) установлены следующие клинические диагнозы: хронический послеоперационный стерномедиастинит (рис. 2) — у 2; хронический остеомиелит ребер — у 1, один из пациентов с остеомиелитом грудины и передних отрезков ребер госпитализирован трижды.
Подготовка ран к пластическому закрытию проводилась с использованием аппарата локального отрицательного давления «АГАТ-Днепр» — у 4 больных (1-я группа) и повязочным методом — у 7 больных (2-я группа). Для пластического закрытия раны нами использован как одноэтапный (2-я группа), так и двухэтапный подход (1-я группа).
Результаты и обсуждение
У всех больных мы использовали активную хирургическую тактику. Выбор осуществляли в зависимости от характера и глубины поражения тканей. Поверхностное инфекционное поражение тканей в области грудины (superficial sternal wound infection — SSWI) подразумевало нагноение мягких тканей в области фиксирующих грудину лигатур, остеомиелит грудины и ребер без распространения на клетчатку переднего средостения, поражение грудинно-реберного комплекса. Глубокое инфекционное поражение грудины (deep sternal wound infection) было представлено передним стерномедиастинитом с тотальной несостоятельностью швов грудины с флотацией ее краев, обширным гнойным поражением мягких тканей, грудины и реберно-ключичного комплекса.
Возбудителями инфекционного процесса в грудине и средостении являлись как грамположительные, так и грамотрицательные микроорганизмы. Наиболее часто встречались Staphylococcus epidermidis и Staphylococcus aureus, доля метициллинрезистентного Staphylococcus aureus при этом составляла более 16 %. Обращает на себя внимание большое число пациентов с Pseudomonas aeruginosa и Acinetobacter baumannii. Почти четверть всех больных в процессе лечения имели 1 антибиотикорезистентный микроорганизм или более. Проводили антибактериальную терапию с учетом чувствительности микрофлоры, местное лечение раны антисептиками (перевязки 2–3 раза в сутки) и затем мазевыми повязками.
При глубоком поражении удаление металлических лигатур выполняли только после санации переднего средостения. Это связано с тем, что при остром стерномедиастините крайне высок риск развития нестабильности грудинно-реберного комплекса с нарушением функции внешнего дыхания, что может привести к острой дыхательной недостаточности и декомпенсации витальных функций организма.
При переднем стерномедиастините возможности репарации затруднены из-за отсутствия хорошо кровоснабжаемых тканей, наличия открытой поврежденной губчатой кости, как правило, некротизированной по краям. Широко раскрывали гнойные полости, создавая оптимальные условия для оттока гнойного отделяемого, удаляли металлические лигатуры, свободно лежащие секвестры створок грудины, измененных реберных хрящей.
У пациентов с SSWI (n = 8) во время операции из вскрытых очагов некроза, гнойных затеков производили забор материала на исследование микрофлоры и чувствительности к антибактериальным препаратам. Одной из главных особенностей операции является хирургическая обработка раны с удалением инфицированных тканей единым блоком в пределах здоровых, так как высокая контаминация раны не позволяет произвести более экономную резекцию. При гнойном хондрите и поражении медиальной трети реберного хряща резецировали 2–3 см костной части, а при поражении латеральной трети хряща — не менее 5 см. При остеомиелите ребра ребро резецировали в пределах не менее 2–3 см от границы воспаленной надкостницы.
И только после этого решался вопрос о ликвидации дефекта в полости грудины и/или переднем средостении, а также при возможности стабилизации грудинно-реберного комплекса. Следует учитывать, что позднее закрытие раны грудной стенки и нестабильность грудной клетки приводят к выраженным нарушениям дыхания и гемодинамики, продолжению гнойного процесса в ране.
Для ускорения очищения раны и подготовки ее к пластическому закрытию во 2-й группе применяли терапию локальным отрицательным давлением (VAC-терапия) как одну из разновидностей активного дренажа, сочетающего преимущества открытого и закрытого ведения ран. Как и при открытом ведении, в данном случае имеется доступ для активной обработки раневой поверхности при смене повязки. Одновременно рана герметично закрыта, а равномерно распределенное отрицательное давление обеспечивает полное дренирование раневой поверхности с сохранением каркасности грудной стенки (рис. 3).
/63-2.jpg)
В нашей практике мы чаще использовали разрежение 70–90 мм рт.ст., продемонстрировавшее высокую эффективность. Применение избыточного разрежения на поверхности средостения потенциально опасно вентиляционными нарушениями. Эластичный пористый материал для заполнения полости раны позволяет равномерно распределять макро- и микронапряжение. Плотное прилегание повязки способствует равномерному распределению отрицательного давления по всей ране и эвакуации отделяемого. Вакуум облегчает сближение краев раны. Активируются обменные процессы, что выражается в уменьшении отека, более быстром очищении раневой поверхности, снижении бактериального загрязнения ткани, облегчении миграции фагоцитарных клеток, а расширение артериол позволяет ускорить грануляционные процессы, неоваскулогенез. Вакуумная санация раны позволила быстрее перейти к пластическому этапу лечения. Кроме того, создаваемое отрицательное давление уменьшает патологическую подвижность створок грудины относительно друг друга после удаления несостоятельных проволочных швов. Использование вакуум-терапии в последние годы способствовало оптимизации течения раневого процесса по сравнению с пациентами 2-й группы (табл. 1).
Показатели степени выраженности активации перекисного окисления липидов являются значимыми в оценке течения послеоперационного стерномедиастинита. Активность гнойного воспаления проявлялась в увеличении содержания гептанрастворимых диеновых конъюгатов и снижении содержания карбонилированных белков. Использование вакуум-терапии в последние годы способствовало оптимизации течения раневого процесса по сравнению с пациентами 2-й группы. Но в отношении уменьшения бактериальной обсемененности статистически значимого улучшения не отмечали: у 55 % больных добиться «чистоты» раны не удалось. При решении вопроса о выполнении реконструктивно-пластического этапа мы ориентировались на уровень содержания микробных тел в ране менее 103 КОЕ/г, однако зачастую были вынуждены выполнять пластический этап в первую очередь в целях быстрейшей стабилизации грудинно-реберного комплекса.
Решающее значение для выбора лоскута при закрытии дефекта мягких тканей имеет знание кровоснабжения донорской зоны покровных тканей и анатомической характеристики дефекта (площадь, глубина, структурный состав ткани, наличие инфекции в ране).
Как правило, использовали комбинированную пластику дефекта за счет мобилизации больших грудных мышц и местных скользящих или островковых кожно-фасциальных лоскутов. В 2 случаях использована и малая грудная мышца. Отсепаровывали края больших грудных мышц по периметру в латеральном направлении до уровня нормально кровоснабжаемых тканей и межреберных мышц и фиксировали рассасывающимися лигатурами к сохранившейся части ребер и грудины по всему периметру. Мобилизация в 2 случаях была проведена по типу «опрокидывающегося» мышечного лоскута (рис. 4).
Как особенность рубцеобразования престернальной зоны, особенно в условиях длительного хронического раневого воспаления, при способах свободной кожной пластики отмечаем склонность к образованию патологических форм кожного рубца (рис. 5).
К моменту выписки полного заживления раны передней грудной стенки добились у 81,8 % больных. Умерла 1 больная при явлениях прогрессирования гнойного стерномедиастинита и сепсиса.
Выводы
При использовании VAC-терапии у пациентов с инфекционными осложнениями стернальных ран снижается риск возникновения рецидивов и сокращаются сроки лечения. В настоящее время существует необходимость проведения дальнейших исследований, направленных на оптимизацию выбора метода и сроков проведения реконструктивных миопластических вмешательств.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.

/62-1.jpg)
/63-1.jpg)
/63-2.jpg)
/64-1.jpg)
/65-1.jpg)