Журнал «» 2(22) 2012
Вернуться к номеру
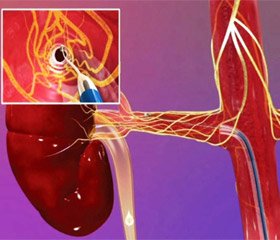
Ниркова денервація — інтервенційна терапія резистентної гіпертензії Позиційна стаття Європейського товариства гіпертензії
Авторы: Roland E. Schmiedera, Josep Redonb, Guido Grassic,k, Sverre E. Kjeldsend, Giuseppe Manciae, Krzysztof Narkiewiczf, Gianfranco Paratig, Luis Ruilopeh, Philippe van de Bornei, Costas Tsioufisj,
a University Hospital Erlangen, Nephrology and Hypertension, Erlangen, Germany,
b University of Valencia, Internal Medicine, Hypertension Unit, Valencia, Spain,
c Clinica Medica, Ospedale S. Gerardo dei Tintori, Monza (Milan), Italy,
d University of Oslo, Department of Cardiology at Ullevaal Hospital, Oslo, Norway,
e University of Milano-Bicocca, Department of Medicine, S. Gerardo Hospital, Monza, Italy,
f Medical University of Gdansk, Department of Hypertension and Diabetology, Gdansk, Poland,
g Department of Cardiology, S. Luca Hospital, Istituto Auxologico Italiano & Department of Clinical Medicine and Prevention, University of Milano-Bicocca, Milan, Italy,
h University Autonoma & Hypertension Unit, Hospital 12 de Octubre, Madrid, Spain,
i Department of Cardiology, Erasme Hospital, Brussels, Belgium,
j University of Athens, First Cardiology Clinic, Hippokration Hospital, Athens, Greece,
k Istituto di Ricerche a Carattere Ccientifico IRCCS Multimedica, Sesto san Giovanni (Milan), Italy
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Разделы: Справочник специалиста
Версия для печати
Експерти з Європейського товариства гіпертензії підготували цей документ з викладенням позиції для того, щоб узагальнити наявні дані, невирішені питання і надати практичні рекомендації із застосування черезшкірної транслюмінальної абляції ниркових нервів (ниркової денервації) як нової терапевтичної стратегії лікування резистентної артеріальної гіпертензії. Активація ниркової симпатичної системи та сенсорних аферентних сигналів до центральної нервової системи являє собою ціль для ниркової денервації. Клінічні дослідження підтвердили, що катетерна радіочастотна ниркова денервація приводить до зменшення активності ниркових еферентних симпатичних та аферентних сенсорних впливів і це супроводжується клінічно значимим зниженням систолічного та діастолічного артеріального тиску у хворих на резистентну артеріальну гіпертензію. Ця позиційна публікація має на меті сприяти кращому розумінню ефективності, безпеки, обмежень і проблем, що належить вирішити при проведенні ниркової денервації.
Глобальний тягар неконтрольованої артеріальної гіпертензії
Від артеріальної гіпертензії (АГ) сьогодні страждає близько 25 % дорослого населення світу. Її поширеність, за прогнозами, у 2025 році зросте до 1,5 млрд хворих на гіпертонічну хворобу [1]. Відповідно збільшаться витрати системи охорони здоров’я. Існує лінійна залежність між рівнем артеріального тиску (АТ) і величиною серцево-судинного ризику [2, 3]. Згідно з аналізом у світовому масштабі, 7 600 000 передчасних смертей (близько 13,5 % від загального числа смертей), 54 % інсультів і 47 % подій, викликаних ішемічною хворобою серця, виникає внаслідок високого АТ [4]. Найважливішим у цьому є те, що навіть помірне зниження АТ супроводжується достовірним зменшенням серцево-судинної захворюваності та смертності незалежно від початкового рівня АТ [5–8]. Незважаючи на адекватну антигіпертензивну терапію, цільовий рівень АТ не досягнуто у значної частини пацієнтів, особливо при так званій резистентній АГ.
Відповідно до настанов Європейського товариства гіпертензії (ESH)/Європейського товариства кардіологів (ESC) та Сьомої доповіді Об’єднаного національного комітету США з профілактики, діагностики, оцінки та лікування підвищеного артеріального тиску (JNC 7), резистентна АГ визначається як стійко підвищений АТ більше за цільовий рівень, незважаючи на одночасне використання трьох антигіпертензивних препаратів в адекватних дозах різних класів, включаючи діуретик [5, 6]. Точне поширення резистентної гіпертензії визначити важко, але залежно від чисельності населення та наявності так званих центрів лікування АГ вважають, що вона коливається від 5 до 30 % [9–12]. У разі неможливості досягти цільового рівня АТ, незважаючи на терапевтичні втручання, спостерігається прискорений розвиток уражень органів-мішеней, що обумовлює у таких пацієнтів високий ризик розвитку серцево-судинних подій [5, 6, 13].
Згідно з цими положеннями, розробка додаткових підходів до існуючого лікування резистентної гіпертензії, що складається зі зміни способу життя в поєднанні з комбінованою фармакотерапією, є пріоритетним клінічним завданням. Черезшкірна катетерна транслюмінальна ниркова абляція (відтепер — ниркова денервація (НДН)) за допомогою радіочастотної енергії — це новий розроблений підхід до забезпечення стійкого зниження АТ у пацієнтів з резистентною гіпертензією [14–17]. Минулого року інноваційний метод НДН поступово увійшов у клінічну практику в багатьох країнах для лікування резистентної АГ. Потенціал для його клінічного застосування ґрунтується на провідній ролі симпатичної гіперактивності для підтримки високих значень АТ.
Загальна та ниркова симпатична гіперактивність при артеріальній гіпертензії
Як було показано в численних дослідженнях, підвищення симпатичної активності характеризує всі фенотипи, характерні для гіпертензії, у тому числі при гіпертонічній хворобі [18–20], АГ «білого халата», маскованій АГ [18, 21], та асоціюється із будь-яким статусом щодо нічного зниження АТ: диперами, екстремальними диперами, нон-диперами або зворотними диперами [22]. Це також стосується і гіпертензії, викликаної вагітністю [23], деяких вторинних типів АГ [24], а також резистентної гіпертензії [25]. Найбільш виражено гіперактивність симпатичної нервової системи проявляється в нирках [26] і прогресивно зростає, паралельно до ступеня тяжкості АГ [25, 27, 28].
Симпатична іннервація нирок забезпечується за рахунок густої мережі постгангліонарних нейронів, що іннервують нирку [29, 30]. Аксони прегангліонарних нейронів виходять із грудного і поперекового симпатичних стовбурів і досягають пре- і паравертебральних симпатичних гангліїв. Ниркові постгангліонарні нерви йдуть упродовж ниркових артерій і ведуть до воріт (hilus) нирок. Після цього вони поділяються на більш дрібні пучки нервів упродовж кровоносних судин і проникають у кіркову та юкстамедулярну ділянки. Ниркова симпатична активація нервів збільшує продукцію норадреналіну і вивільнення його з нервових закінчень, що призводить до ниркової вазоконстрикції, підвищення секреції реніну, реабсорбції натрію і рідини; а наслідками ниркової вазоконстрикції є зниження ниркового кровотоку і швидкості клубочкової фільтрації [31].
Тіла клітин ниркових аферентних нервів знаходяться в гангліях спинного іпсилатерального кореня (T6-L4). Звідти висхідні сигнали проходять до серцево-судинного центру в центральній нервовій системі. Ниркові аферентні чутливі нерви реагують на розтягнення (механорецептори), ниркову ішемію, гіпоксію або інші подразники (хеморецептори), збільшуючи ниркову аферентну активність [32–34]. Електрична стимуляція аферентних ниркових нервів підвищує рівень АТ [35] й індукує мезентеріальну та м’язову вазоконстрикцію [35]. З іншого боку, аферентна ниркова денервація послаблює ці ефекти і затримує розвиток або запобігає виникненню гіпертензії на деяких моделях у тварин [36]. Загалом аферентні й еферентні волокна роблять важливий внесок у регуляцію системного судинного опору та контролю АТ [37].
Ренальна денервація при резистентній артеріальній гіпертензії
У минулому столітті хірургічне видалення селезінки (splanchnicectomy), що призводить до ниркової денервації, серед інших ефектів покращувало виживання хворих на гіпертонічну хворобу порівнянно з консервативною терапією на той момент [38], але інтерес до цієї інвазивної хірургічної техніки зник раптово зразу ж після впровадження ефективних антигіпертензивних препаратів.
НДН — це процедура черезшкірного малоінвазивного втручання, що характеризується коротким часом відновлення, а також відсутністю значних системних побічних ефектів. Дані про клінічну ефективність цієї процедури у хворих на гіпертонічну хворобу походять від програми клінічних випробувань Symplicity, що складається з групи досліджень, присвячених дослідженню ефективності НДН у лікуванні резистентної гіпертонії. Ці дослідження включають Symplicity HTN-1 (із продовженим спостереженням) та Symplicity HTN-2, результати яких були нещодавно опубліковані [15–17].
Дослідження Symplicity HTN-1 та результати продовженого спостереження
Ефективність
Це перший доказ правильності та безпечності концепції у людей: у дослідження було включено 50 пацієнтів (середній вік 58 ± 9 років) зі стійкою тяжкою резистентною гіпертензією (офісний АТ ≥ 160 мм рт.ст. при прийомі принаймні трьох або більше антигіпертензивних препаратів, у тому числі діуретика). У середньому початковий офісний САТ/ДАТ становив 177/101 мм рт.ст. на фоні прийому в середньому 5,1 антигіпертензивного препарату. НДН була досягнута за допомогою радіочастотної абляції спеціальним катетером (Symplicity, Ardian Inc., Пало-Альто, Каліфорнія, США) доступом через стегнову артерію. Офісний САТ/ДАТ після двосторонньої НДН знизився на 14/10, 21/10, 22/11, 24/11 і 27/17 мм рт.ст. на 1, 3, 6, 9 і 12-й місяць після процедури відповідно. У дев’яти пацієнтів дози препаратів було збільшено і у чотирьох пацієнтів — зменшено. Після незалежного перегляду даних визнано зазначений ефект процедури на рівень САТ/ДАТ. У невеликої частини хворих, в яких визначали викид норадреналіну нирками, було показано його зменшення на 47 %, що продемонструвало ефективність абляції ниркових симпатичних волокон. У більш довгостроковому спостереженні за 153 пацієнтами, у тому числі 45 пацієнтами з НДН у рамках дослідження Symplicity HTN-1 та більш великою групою нерандомізованих подібних пацієнтів, яким була виконана процедура НДН (середній вік — 57 років, середній офісний САТ/ДАТ — 176/98 мм рт.ст., незважаючи на прийом у середньому 5,1 антигіпертензивного засобу), офісний САТ/ДАТ значно знижувався на 20/10, 24/11, 25/11, 23/11, 26/14 і 32/14 мм рт.ст. на етапі 1, 3, 6, 12, 18 і 24-го місяця після процедури відповідно. Ці результати показують, що зниження АТ підтримується принаймні до 2 років після операції.
Безпека
Довгострокова безпечність процедури катетерної НДН була досліджена при тривалому спостереженні за групою хворих (n = 153) після закінчення дослідження Symplicity HTN-1. У цій групі у 97 % пацієнтів (149 із 153) не було ускладнень. Чотири гострих процедурні ускладнення включали три псевдоаневризми стегнової артерії та одну дисекцію ниркової артерії, але все обійшлося без подальших ускладнень. В одного пацієнта через 6 місяців після процедури за даними комп’ютерної томографічної (КТ), ангіографії виявлено прогресування існуючого стенозу в усті однієї ниркової артерії, який було успішно усунуто за допомогою стентування. Слід зазначити, що місце стенозу не було в ділянці, де проводилася абляція. Оцінка функції нирок показала, що протягом першого року спостереження рівень швидкості клубочкової фільтрації залишається стабільним, а після 2 років не було випадків подвоєння рівня креатиніну сироватки або випадків розвитку хронічного захворювання нирок на стадії 4 або 5 (хронічна ниркова недостатність).
Дослідження Symplicity HTN-2
Ефективність
У це багатоцентрове проспективне рандомізоване клінічне дослідження були включені пацієнти з резистентною АГ та рівнем офісного САТ і 160 мм рт.ст. (або Ј 150 мм рт.ст. для пацієнтів із цукровим діабетом 2-го типу) [17]. Учасники були рандомізовані на НДН відразу або після 6 місяців, без будь-яких змін у попередній схемі прийому антигіпертензивних препаратів. Первинною кінцевою точкою була зміна рівня АТ на етапі спостереження 6 місяців. Після первинного скринінгу зі 190 пацієнтів 106 були рандомізовані або на негайне проведення НДН (n = 52), або на затримку виконання процедури (контрольна група) (n = 54). Обидві групи мали схожі базові характеристики і режим прийому антигіпертензивних ліків, за винятком розрахункової величини швидкості клубочкової фільтрації. Офісний САТ/ДАТ у групі НДН знизився на 32/12 мм рт.ст. (базовий рівень — 178/96 мм рт.ст., р < 0,0001), тоді як ніяких змін у контрольній групі не відбулося. Різниця в рівні офісного САТ/ДАТ в обох групах через 6 місяців становила 33/11 мм рт.ст. (достовірність різниці — р < 0,0001). Після врахування ефекту збільшення доз антигіпертензивних препаратів ця різниця становила 31/11 мм рт.ст. (р < 0,0001). Амбулаторне моніторування АТ протягом 24 годин, що було виконане в обмеженої кількості пацієнтів з обох груп (n = 20), показало аналогічний, хоча і менш виражений, характер змін АТ через 6 місяців після НДН (–11/–7 мм рт.ст., p = 0,006 для рівня САТ, р = 0,014 для рівня ДАТ) порівняно з –3/–1 мм рт.ст. у контрольній групі. Різниця в рівні САТ/ДАТ при домашньому моніторуванні була 22/12 мм рт.ст. (р < 0,0001 порівняно з контролем). У результаті застосування НДН задовільний контроль АТ було досягнуто у 39 % або у 82 % випадків, коли контроль АТ був визначений як САТ менше 140 або менше 160 мм рт.ст. відповідно, тоді як аналогічні показники в контрольній групі становили 3 і 24 %. У десяти із 49 пацієнтів (20 %), яким було проведено НДН протягом наступних 6 місяців, було зменшено прийом антигіпертензивних засобів, тоді як у групі контролю — тільки у трьох із 51 (6 %, p = 0,04). При субаналізі даних показано, що після стандартизації усіх даних за прийомом антигіпертензивних засобів зниження АТ у хворих, яким було проведено процедуру НДН, становило 31/12 мм рт.ст. (p < 0,0001).
Безпека
У дослідженні Symplicity HTN-2 перипроцедурні ускладнення, які б вимагали лікування, були рідкими і складалися з однієї псевдоаневризми стегнової артерії, одного випадку зниження АТ після процедури, що вимагало зменьшення дози антигіпертензивних препаратів, одного випадку інфекції сечовивідних шляхів, одного випадку додаткової госпіталізації для оцінки парестезії і одного випадку болів у спині, що минули після 1 місяця лікування анальгетиками. У семи з 52 пацієнтів (13 %), які перенесли НДН, спостерігалася минуча брадикардія під час процедури, що у деяких із них вимагало застосування атропіну. Функція нирок, яку оцінювали за рівнем сироваткового креатиніну, розрахунковою швидкостістю клубочкової фільтрації та вмістом цистатину С, залишалася без змін у порівнянні з початковими даними в обох групах протягом 6 місяців. Упродовж 6 місяців при візуалізації ниркових судин було виявлено можливе прогресування основного атеросклеротичного ураження в одного пацієнта, що не потребувало додаткового лікування. Цікаві результати було отримано в іншому субдослідженні цього дослідження, що включало 37 хворих із резистентною АГ. Застосування НДН привело до зниження рівня САТ/ДАТ на піку виконання навантаження на 21/5 мм рт.ст. та 29/9 мм рт.ст. у період відновлення, в той час як частота серцевих скорочень та споживання кисню під час навантаження практично не змінилися [39].
Обмеження та відкриті питання
Слід підкреслити, що на початок 2012 року лише невеликій кількості хворих було проведено НДН, і термін подальшого спостереження досить короткий. Отже, ряд питань потребує подальшого з’ясування. Що стосується ефективності, в проведених дослідженнях не було групи фіктивного втручання, що тепер є частиною дослідження Symplicity HTN-3, яке в даний час проводиться в США, а також дослідження довгострокового ефекту ниркової симпатичної активації при гіпертензії, яке розпочате в країнах Європи та Канаді. Добове моніторування артеріального тиску було доступно тільки у невеликої (вибіркової) частини пацієнтів, і ступінь зниження АТ, який спостерігався при цьому, був значно меншим, ніж при офісному та домашньому вимірюванні [15, 17]. Таким чином, істинний антигіпертензивний ефект НДН, і зокрема ті компоненти прогнозу, що виходять не з офісного визначення АТ, ще належить визначити. Також повинна бути досліджена довгострокова тривалість антигіпертензивного ефекту після НДН, оскільки нервові волокна можуть регенерувати [40, 41]. Слід підкреслити, що при тривалому спостереженні в дослідженні Symplicity HTN-1 не спостерігалося ослаблення антигіпертензивного ефекту протягом 24 місяців, і це дозволяє припустити, що цього протягом періоду функціональної реіннервації не відбулося [16]. До того часу пацієнти з подвоєнням ниркових артерій, а також додатковими артеріями були виключені з дослідження, а також немає систематичних даних щодо ефекту односторонньої НДН [15, 17].
Відсутність перед процедурою маркерів, які б могли визначити добру реакцію на НДН (за винятком початкового рівня АТ), є ще одним важливим питанням для розгляду. Незважаючи на методологічні досягнення в оцінці адренергічної функції (отримані при виконанні мікронейрографії та визначенні органоспецифічного викиду норадреналіну), немає клінічної методики визначення успішності абляції ниркових симпатичних волокон під час процедури. Досі НДН проводилася у хворих із тяжкою резистентною АГ, і її ефекти при менш тяжких формах АГ невідомі. Так само невідомо, чи буде вплив на запобігання розвитку серцево-судинних ускладнень і чи зменшиться смертність.
У даний час проводяться подальші багатообіцяючі експериментальні дослідження щодо ниркової симпатичної денервації, що здійснюється різними методами, з використанням локальної доставки нейротоксичних препаратів, кріодеструкції, деструкції ультразвуком, а також клінічні випробування з використанням інших типів радіочастотних катетерів (наприклад, випробування з катетером у формі кошика (Ablation Induced Renal Sympathetic Denervation Trial study)) [42].
Перелік невирішених наукових проблем НДН:
— Рандомізовані сліпі дослідження.
— Використання добового моніторування АТ для оцінки антигіпертензивного ефекту.
— Порівняння ефективності і безпечності НДН при використанні різних процедур.
— Довгострокова оцінка ефективності та безпечності.
— Вплив на ризик розвитку серцево-судинних ускладнень та зниження смертності.
— Дослідження економічної доцільності НДН.
— Стандартизація та сертифікація НДН центрів.
Критерії відбору хворих для ниркової денервації
На підставі даних клінічних досліджень критеріями відбору хворих на АГ, яким показано проведення НДН, є наявність тяжкої резистентної до лікування АГ (при рівні офісного САТ не менше 160 мм рт.ст. (Ј 150 мм рт.ст. при цукровому діабеті 2-го типу)) принаймні трьома антигіпертензивними препаратами різних класів в адекватних дозах, у тому числі обов’язково — діуретиком, що відповідає АГ 2-го або 3-го ступеня [15–17].
Стан пацієнтів повинен бути оціненим фахівцем у галузі гіпертензії, який працює в спеціалізованому центрі (відділення) з певним досвідом (наприклад, у визнаних ESH-центрах досконалості). Пацієнти повинні пройти клінічне обстеження для підтвердження резистентності до лікування. Початковий крок — абсолютне виключення стану псевдорезистентності. Особливу увагу слід приділити виявленню неприхильності до терапії, яка часто присутня і не розпізнається, якщо строго не досліджується [6]. Збереження підвищеного офісного АТ, незважаючи на адекватне лікування, повинно бути підтверджено при домашньому і, найголовніше, добовому моніторуванні АТ, тому що не менше ніж у третини резистентних до лікування хворих АТ поза офісом є нормальним (фальшива резистентна АГ внаслідок феномену «білого халата») [43]. Після підтвердження істинної резистентної АГ слід ретельно дослідити пацієнта на предмет виявлення факторів способу життя, які сприяють резистентності, максимально їх корегувати та припинити або звести до мінімуму використання субстанцій (в тому числі ліків), які можуть підвищувати АТ, а також провести додаткові обстеження для виявлення вторинних причин АГ, тобто визначити ті умови, за яких контроль АТ може бути простішим при усуненні цих причинних факторів [5, 6]. Існують певні розбіжності щодо використання антагоністів альдостерону як необхідної умови для відбору пацієнтів. Уважають, що з його використанням може бути досягнуто зниження САТ до 25 мм рт.ст., але не всі пацієнти мають таку відповідь. У першому подвійному сліпому рандомізованому дослідженні зниження АТ при прийомі спіронолактону було досить помірним, довгострокова безпечність такої терапії є предметом непокоєння [44]. І нарешті, якщо АТ не контролюється, то пацієнт вважається кандидатом для проведення НДН.
Якщо це не зроблено до того, рекомендується візуалізація ниркової артерії (наприклад, комп’ютерна або магнітно-резонансна ангіографія), щоб точно оцінити анатомію ниркових артерій перед виконанням процедури НДН. Слід підкреслити, що пацієнти з резистентною АГ майже без винятку мають досвід прийому різних антигіпертензивних препаратів. Значна частина з них стверджує, що мають непереносимість деяких із них, і така непереносимість може бути пов’язана із типовими побічними ефектами даного компоненту, але також може бути пов’язана з психіатричними (психологічними) проблемами пацієнта або невдалими стосунками пацієнта з лікарем. Це є завданням для спеціаліста з гіпертензії: виявити істинну непереносимість препарату (наприклад, шляхом повторного пробного призначення непереносимих препаратів), оскільки тільки в цьому випадку процедура НДН може бути виправданою.
Наступні критерії виключення повинні бути впроваджені для того, щоб безпечно провести процедуру НДН [15–17]: попередні втручання на ниркових артеріях (балонна ангіопластика та стентування), ознаки атеросклерозу ниркової артерії (визначаються як стеноз ниркової артерій > 50 %), наявність кількох головних ниркових артерії в нирці або головної ниркової артерії діаметром менше 4 мм або завдовжки менше 20 мм, а також величини клубочкової фільтрації < 45 мл/хв/1,73 м2. Пацієнти повинні знаходитися в стабільному клінічному стані (НДН не є елементом невідкладної допомоги), за винятком тих, які нещодавно перенесли інфаркт міокарда, нестабільну стенокардію або інсульт протягом останніх 3–6 місяців.
Якщо пацієнт відповідає всім критеріям відбору для НДН, процедуру може бути заплановано. Втручання повинні виконуватися інтервенційними кардіологами та радіологами, які пройшли навчання для проведення даного конкретного втручання і мають право лікувати такі можливі ускладнення, як розшарування ниркової артерії.
Практичні рекомендації щодо проведення НДН у клінічній практиці
Перший крок
Виключити:
— псевдорезистентність із використанням добового та домашнього моніторування АТ;
— вторинну АГ;
— причини, які сприяють підтримці високого АТ і можуть бути усунені (обструктивне апное сну, надмірне споживання солі, підвищення АТ препаратами, ожиріння).
Другий крок
Оптимізація антигіпертензивної терапії: принаймні три (або краще чотири) переносимих препарати, включаючи діуретики та антагоністи альдостерону (якщо клінічно можливо, після повторної оцінки функції нирок і потенційного ризик гіперкаліємії) та перевірка ефективності контролю АТ із використанням добового моніторингу АТ до призначення НДН.
Третій крок
Переглянути анатомічні протипоказання через невирішені питання безпеки (уникати проведення НДН в разі множинних ниркових артерій, основної ниркової артерії діаметром менше 4 мм або основної ниркової артерії довжиною менше 20 мм, при значному стенозі ниркових артерій після попередньої ангіопластики та стентування ниркових артерій). Крім того, швидкість клубочкової фільтрації повинна бути > 45 мл/хв/1,73 м2.
Загальні
— Виконуйте процедуру в центрах, які мають досвід лікування резистентної АГ, наприклад визнаних ESH центрах досконалості.
— Використовуйте пристрої, які продемонстрували ефективність і безпечність у клінічних дослідженнях.
Перспективи
Ниркова денервація може мати позитивний ефект і при інших станах, що характеризуються надмірною активністю симпатичної нервової системи, і у даний час проводиться вивчення її ефективності в кількох клінічних дослідженнях. Поки ці результати не опубліковані, ми повинні використовувати процедуру НДН для терапії пацієнтів із резистентною АГ, ретельно дотримуючись вищезазначених критеріїв відбору в спеціалізованих центрах лікування гіпертензії (у тому числі визнаних ESH-центрах досконалості). Таким чином, в Європі НДН повинні виконуватися у центрах, що мають досвід лікування резистентної АГ, а процедуру проводи добре навчені лікарі-інтервенціоністи.
Подяка та конфлікт інтересів
Установа RES (Університетська лікарня Ерланген, Німеччина) отримала підтримку відряджень, консалтинг і платню за лекції від Medtronic. Установа RES (Університетська лікарня Ерланген, Німеччина) отримувала гранти від компанії Medtronic. Інших конфліктів інтересів авторів для оголошення немає.
Стаття вперше надрукована:
Journal of Hypertension. — 2012 May. — 30, № 5. — Р. 837-841
Перекладздійсненозапідтримки
ВГО «Проти гіпертензії»
Науковий редактор перекладу Ю. Сіренко
1. Kearney P.M., Whelton M., Reynolds K., Muntner P., Whelton P.K., He J. Global burden of hypertension: analysis of worldwide data // Lancet. 2005; 365: 217-223.
2. Turnbull F., Neal B., Ninomiya T., Algert C., Arima H., Barzi F. et al. Effects of different regimens to lower blood pressure on major cardiovascular events in older and younger adults: meta-analysis of randomised trials // BMJ. 2008; 336: 1121-1123.
3. Lewington S., Clarke R., Qizilbash N., Peto R., Collins R. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies // Lancet. 2002; 360: 1903-1913.
4. Lawes C.M., Vander Hoorn S., Rodgers A. Global burden of blood pressure-related disease, 2001 // Lancet. 2008; 371: 1513-1518.
5. Mancia G., Laurent S., Agabiti-Rosei E., Ambrosioni E., Burnier M., Caulfield M.J. et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document // J. Hypertens. 2009; 27: 2121-2158.
6. Mancia G., De Backer G., Dominiczak A., Cifkova R., Fagard R., Germano G. et al. 2007 Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // J. Hypertens. 2007; 25: 1105-1187.
7. Zhang Y., Zhang X., Liu L., Zanchetti A. Is a systolic blood pressure target < 140 mm Hg indicated in all hypertensives? Subgroup analyses of findings from the randomized FEVER trial // Eur. Heart. J. 2011; 32: 1500-1508.
8. Czernichow S., Zanchetti A., Turnbull F., Barzi F., Ninomiya T., Kengne A.P. et al. The effects of blood pressure reduction and of different blood pressure-lowering regimens on major cardiovascular events according to baseline blood pressure: meta-analysis of randomized trials // J. Hypertens. 2011; 29: 4-16.
9. Prugger C., Keil U., Wellmann J., de Bacquer D., de Backer G., Ambrosio G.B. et al. Blood pressure control and knowledge of target blood pressure in coronary patients across Europe: results from the EUROASPIRE III survey // J. Hypertens. 2011; 29: 1641-1648.
10. Calhoun D.A., Jones D., Textor S., Goff D.C., Murphy T.P., Toto R.D. et al. Resistant hypertension: diagnosis, evaluation, and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research // Hypertension. 2008; 51: 1403-1419.
11. De la Sierra A., Segura J., Banegas J.R., Gorostidi M., de la Cruz J.J., Armario P. et al. Clinical features of 8295 patients with resistant hypertension classified on the basis of ambulatory blood pressure monitoring // Hypertension. 2011; 57: 898-902.
12. Egan B.M., Zhao Y., Axon R.N., Brzezinski W.A., Ferdinand K.C. Uncontrolled and apparent treatment resistant hypertension in the United States, 1988 to 2008 // Circulation. 2011; 124: 1046-1058.
13. Cuspidi C., Macca G., Sampieri L., Michev I., Salerno M., Fusi V. et al. High prevalence of cardiac and extracardiac target organ damage in refractory hypertension // J. Hypertens. 2001; 19: 2063-2070.
14. Schlaich M.P., Sobotka P.A., Krum H., Whitbourn R., Walton A., Esler M.D. Renal denervation as a therapeutic approach for hypertension: novel implications for an old concept // Hypertension. 2009; 54: 1195-1201.
15. Krum H., Schlaich M, Whitbourn R., Sobotka P.A., Sadowski J., Bartus K. et al. Catheter-based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof-of-principle cohort study // Lancet. 2009; 373: 1275-1281.
16. Simplicity HTN-1 Investigators 2011. Catheter-based renal sympathetic denervation for resistant hypertension: durability of blood pressure reduction out to 24 months // Hypertension. 2011; 57: 911-917.
17. Simplicity HTN-2 Investigators, Esler M.D., Krum H., Sobotka P.A., Schlaich M.P., Schmieder R.E., Bohm M. Renal sympathetic denervation in patients with treatment-resistant hypertension (The Symplicity HTN-2 Trial): a randomised controlled trial // Lancet. 2010; 376: 1903-1909.
18. Grassi G. Assessment of sympathetic cardiovascular drive in human hypertension: achievements and perspectives // Hypertension. 2009; 54: 690-697.
19. Grassi G., Seravalle G., Bertinieri G., Turri C., Dell’Oro R., Stella M.L. et al. Sympathetic and reflex alterations in systo-diastolic and systolic hypertension of the elderly // J. Hypertens. 2000; 18: 587-593.
20. Flaa A., Eide I.K., Kjeldsen S.E., Rostrup M. Sympathoadrenal stress reactivity is a predictor of future blood pressure: an 18-year followup study // Hypertension. 2008; 52: 336-341.
21. Grassi G., Seravalle G., Trevano F.Q., Dell’oro R., Bolla G., Cuspidi C. et al. Neurogenic abnormalities in masked hypertension // Hypertension. 2007; 50: 537-542.
22. Grassi G., Seravalle G., Quarti-Trevano F., Dell’Oro R., Bombelli M., Cuspidi C. et al. Adrenergic, metabolic, and reflex abnormalities in reverse and extreme dipper hypertensives // Hypertension. 2008; 52: 925-931.
23. Schobel H.P., Fischer T., Heuszer K., Geiger H., Schmieder R.E. Preeclampsia: a state of sympathetic overactivity // N. Engl. Med. 1996; 335: 1480-1485.
24. Schlaich M.P., Socratous F., Hennebry S., Eikelis N., Lambert E.A., Straznicky N. et al. Sympathetic activation in chronic renal failure // J. Am. Soc. Nephrol. 2009; 20: 933-939.
25. Tsioufis C., Kordalis A., Flessas D., Anastasopoulos I., Tsiachris D., Papademetriou V. et al. Pathophysiology of resistant hypertension: the role of sympathetic nervous system // Int. J. Hypertens. 2011; 2011: 642-416.
26. Esler M., Lambert G., Jennings G. Regional norepinephrine turnover in human hypertension // Clin. Exp. Hypertens A. 1989; 11 (Suppl. 1): 75-89.
27. Anderson E.A., Sinkey C.A., Lawton W.J., Mark A.L. Elevated sympathetic nerve activity in borderline hypertensive humans. Evidence from direct intraneural recordings // Hypertension. 1989; 14: 177-183.
28. Grassi G., Cattaneo B.M., Seravalle G., Lanfranchi A., Mancia G. Baroreflex control of sympathetic nerve activity in essential and secondary hypertension // Hypertension. 1998; 31: 68-72.
29. Barajas L., Liu L., Powers K. Anatomy of the renal innervation: intrarenal aspects and ganglia of origin // Can. J. Physiol. Pharmacol. 1992; 70: 735-749.
30. Luff S.E., Hengstberger S.G., McLachlan E.M., Anderson W.P. Distribution of sympathetic neuroeffector junctions in the juxtaglomerular region of the rabbit kidney // J. Auton. Nerv. Syst. 1992; 40: 239-253.
31. DiBona G.F., Esler M. Translational medicine: the antihypertensive effect of renal denervation // Am. J. Physiol. Regul. Integr. Comp. Physiol. 2010; 298: R245-R253.
32. Ditting T., Freisinger W., Siegel K., Fiedler C., Small L., Neuhuber W. et al. Tonic postganglionic sympathetic inhibition induced by afferent renal nerves? // Hypertension. 2012; 59: 467-476.
33. Stella A., Zanchetti A. Functional role of renal afferents // Physiol. Rev. 1991; 71: 659-682.
34. Hausberg M., Kosch M., Harmelink P., Barenbrock M., Hohage H., Kisters K. et al. Sympathetic nerve activity in end-stage renal disease // Circulation. 2002; 106: 1974-1979.
35. Calaresu F.R., Stella A., Zanchetti A. Haemodynamic responses and renin release during stimulation of afferent renal nerves in the cat // J. Physiol. 1976; 255: 687-700.
36. DiBona G.F., Kopp U.C. Neural control of renal function // Physiol. Rev. 1997; 77: 75-197.
37. Doumas M., Papademetriou V., Douma S., Faselis C., Tsioufis K., Gkaliagkousi E. et al. Benefits from treatment and control of patients with resistant hypertension // Int. J. Hypertens. 2010; 2011: 318-549.
38. Smithwick R.H., Thompson J.E. Splanchnicectomy for essential hypertension; results in 1266 cases // JAMA. 1953; 152: 1501-1504.
39. Ukena C., Mahfoud F., Kindermann I., Barth C., Lenski M., Kindermann M. et al. Cardiorespiratory response to exercise after renal sympathetic denervation in patients with resistant hypertension // J. Am. Coll. Cardiol. 2011; 58: 1176-1182.
40. Hansen J.M., Abildgaard U., Fogh-Andersen N., Kanstrup I.L., Bratholm P., Plum I. et al. The transplanted human kidney does not achieve functional reinnervation // Clin. Sci (Lond). 1994; 87: 13-20.
41. Gazdar A.F., Dammin G.J. Neural degeneration and regeneration in human renal transplants // N. Engl. J. Med. 1970; 283: 222-224.
42. Safety and Efficacy Study of Renal Artery Ablation in Resistant Hypertension Patients (ARSENAL). ClinicalTrialsgov. NCT01438229.
43. Banegas J.R., Messerli F.H., Waeber B., Rodriguez-Artalejo F., de la Sierra A., Segura J. et al. Discrepancies between office and ambulatory blood pressure: clinical implications // Am. J. Med. 2009; 122: 1136-1141.
44. Vaclavik J., Sedlak R., Plachy M., Navratil K., Plasek J., Jarkovsky J. et al. Addition of spironolactone in patients with resistant arterial hypertension (ASPIRANT): a randomized, double-blind, placebo-controlled trial // Hypertension. 2011; 57: 1069-1075.