Журнал "Гастроэнтерология" 1 (47) 2013
Вернуться к номеру
Изменения экспрессии MUC2, MUC3, MUC4, TFF3 в слизистой оболочке толстого кишечника у больных неспецифическим язвенным колитом
Авторы: Дорофеев А.Э., Василенко И.В., Рассохина О.А. - Донецкий национальный медицинский университет им. М. Горького
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
Целью данной работы была оценка изменений экспрессии муцинов (MUC2, MUC3, MUC4) и трефоилового пептида (TFF3) слизистого барьера кишечника у больных неспецифическим язвенным колитом (НЯК). Было обследовано 49 больных с левосторонним НЯК в стадии обострения. Всем больным НЯК было проведено эндоскопическое исследование с биопсией слизистой оболочки толстой кишки и морфологическим исследованием биоптата, определением экспрессии MUC2, MUC3, MUC4, TFF3. Изменения слизистого барьера кишечника у больных НЯК отображают нарушение процессов слизеобразования, экспрессии муцинов и их свойств, а также тяжесть течения НЯК
Метою цієї роботи була оцінка змін експресії муцинів (MUC2, MUC3, MUC4) і трефоїлового пептиду (TFF3) слизового бар’єру кишечника у хворих на неспецифічний виразковий коліт (НВК). Було обстежено 49 хворих із лівобічним НВК у стадії загострення. Усім хворим на НВК було проведено ендоскопічне дослідження з біопсією слизової оболонки товстої кишки та морфологічним дослідженням біоптату, визначенням експресії MUC2, MUC3, MUC4, TFF3. Зміни слизового бар’єру кишечника у хворих на НВК відображають порушення процесів слизоутворення, експресії муцинів та їх властивостей і тяжкість перебігу НВК.
The aim of this study was to evaluate the changes in expression of mucins (MUC2, MUC 3, MUC 4) and trefoil peptide (TFF3) of colonic mucus barrier in patients with ulcerative colitis (UC). 49 patients with left-side UC in the acute stage were examined. All patients underwent endoscopic examination of colonic mucosa with biopsy and morphological study of biopsy sample, determination of expression of MUC2, MUC3, MUC4, TFF3. Changes in colonic mucus barrier of patients with UC indicate disorder in mucus production, expression of mucins and their properties, as well as severity
of UC.
неспецифический язвенный колит, слизистый барьер толстого кишечника.
неспецифічний виразковий коліт, слизовий бар’єр товстого кишечника.
ulcerative colitis, colonic mucus barrier.
Введение
Протективная функция слизистого барьера толстого кишечника во многом определяется уровнем экспрессии эпителиальных муцинов и их свойствами. Целью данной работы была оценка влияния изменений экспрессии муцинов (MUC2, MUC3, MUC4) и трефоилового пептида (TFF3) на состояние слизистого барьера толстого кишечника у больных неспецифическим язвенным колитом (НЯК). Было обследовано 49 больных НЯК, выполнено эндоскопическое исследование с биопсией слизистой оболочки толстой кишки (СОТК) и морфологическим исследованием биоптата. У всех больных НЯК выявлено снижение числа бокаловидных клеток, при этом степень их уменьшения коррелировала с тяжестью НЯК, снижение уровня экспрессии секреторного (MUC2) и мембраносвязанных (MUC3, MUC4) муцинов. Отмечалась высокая экспрессия TFF3. Следовательно, для больных НЯК характерно снижение защитного слизистого барьера за счет уменьшения MUC2 и MUC3. Выявленные изменения коррелировали со степенью тяжести НЯК. Наблюдается нарушение взаимодействия муцинов и трефоилового фактора, что снижает протективные свойства муцинов и регенераторный потенциал слизистой оболочки толстого кишечника у больных НЯК.
Актуальность
Защитная функция слизистого барьера толстого кишечника определяется балансом клеточного и гуморального иммунитета, оптимальным соотношением облигатной и факультативной флоры, количеством и свойствами толстокишечной слизи. Уровень экспрессии и степень гликозилирования муцинов характеризуют состоятельность протективной функции муцинов. Эпителиальные муцины — это большая группа секретируемых, а также трансмембранных гликопротеинов, богатых серином, треонином и пролином, связанных большим числом олигосахаридных цепей. На сегодняшний день идентифицировано более 20 муцинов, большинство генов локализуются на хромосоме 11.pq15,5 [1, 2]. Муцины подразделяются на 2 класса соединений: секреторные (MUC2, MUC5AC, MUC5В, MUC6) и трансмембранные муцины (MUC1, MUC4, MUC13, MUC16, MUC17) [1, 3]. Муцины активно экспрессируются эпителием желудочно-кишечного тракта и формируют высокомолекулярный вязко-эластический слой, являющийся протективным барьером между поверхностью слизистой оболочки и полостным содержимым желудочно-кишечного тракта, представляющий собой питательную среду для жизнедеятельности комменсальных бактерий кишечника [2, 3]. Изменения вязко-эластических свойств слизи формируются при взаимодействии муцинов с микроорганизмами, электролитами, белками и пищевыми компонентами. В условиях развития воспалительного процесса муцины претерпевают характерные преобразования: сульфатирование снижается, а сиалирование увеличивается, что отражает снижение резистентности муцина к бактериальному разрушению и способствует повышению проницаемости слизистого барьера кишечника [1, 2, 4].
Согласно современным представлениям, в тонком кишечнике, слепой кишке и проксимальных и дистальных отделах толстого кишечника преимущественно экспрессируются MUC2, MUC4, MUC3 и MUC17, при этом в неизмененной слизистой оболочке желудочно-кишечного тракта их локализация совпадает с распределением трефоиловых пептидов. Трефоиловые факторы (TFF1–3) наряду с муцинами играют важную роль в формировании гастроинтестинального барьера и выполняют протективную и регенераторную функции [4, 5]. TFF синтезируются и секретируются муцинпродуцирующими клетками и тесно связаны с муцинами. Однако молекулярные механизмы взаимодействия муцинов и трефоиловых пептидов, а также многообразие их свойств еще недостаточно хорошо изучены [3, 4]. Считается, что в отличие от TFF1 и TFF2 только TFF3 экспрессируется колоноцитами [4, 5]. Все три трефоиловых фактора обеспечивают процессы миграции клеток, участвуют в полимеризации муцинов, способствуя повышению защитной функции эпителия [5, 6]. Изменения слизистого барьера кишечника при неспецифическом язвенном колите могут характеризоваться изменением экспрессии муцинов и трефоиловых пептидов и приводить к снижению защитных свойств мукозного слоя слизистой оболочки кишечника, что стимулирует клетки иммунной системы, способствует поддержанию воспаления в толстом кишечнике при НЯК.
Целью данной работы была оценка влияния изменений экспрессии муцинов (MUC2, MUC3, MUC4) и трефоилового пептида (TFF3) на состояние слизистого барьера толстого кишечника у больных НЯК.
Материалы и методы
Было обследовано 49 больных левосторонним НЯК в стадии обострения, среди которых было 24 мужчины и 25 женщин. Средний возраст больных составлял (38,3 ± 9,2) года. Помимо общеклинических методов обследования всем больным НЯК было проведено эндоскопическое исследование с биопсией слизистой оболочки толстой кишки и морфологическим исследованием биоптата. Фиксация биоптата слизистой толстой кишки проводилась в 4% растворе нейтрального формалина на одни сутки с последующей заливкой в парафин. Гистохимическую идентификацию муцинов (MUC2, MUC3, MUC4) и TFF3 проводили в биоптатах, фиксированных в 10% нейтральном забуференном формалине (рН 7,2–7,4) в течение 18–24 часов, заливали в парафин по общепринятой методике [1, 6]. Для характеристики слизеобразования проводилась PAS-реакция, с помощью которой выявляли гликопротеиды, гликолипиды и гликоген. Другие срезы окрашивали альциановым синим при значениях рН 1,0 и 2,5. При рН 1,0 сульфатные группы углеводов приобретают достаточный заряд для связывания положительно заряженных молекул красителя. При рН 2,5 окрашивали как сульфатные, так и карбоксильные группы углеводов, которые входят в состав сиаловых, глюкуроновой и индуроновой кислот. С помощью этой методики определяли сульфатированные и несульфатированные протеогликаны и гликопротеины [4, 6].
Иммуногистохимическое исследование муцинов (MUC2, MUC3, MUC4) и трефоилового пептида (TFF3) выполняли на парафиновых срезах. Демаскировку антигенов проводили в цитратном буфере (рН = 6,0) при кипячении на водяной бане в течение 1 часа. В качестве первичных антител использовали мышиные моноклональные антитела (USBiological, США), а также систему визуализации KP-500 (Diagnostic Biosystems, США). При просмотре препаратов на светооптическом уровне антигенпозитивные клетки идентифицировали по их коричневому окрашиванию.
Все обследованные больные получали базисную терапию препаратами 5-аминосалициловой кислоты в течение 30 дней в сочетании с ферментными препаратами и пробиотиками. Эндоскопическое и морфологическое исследования проводились у больных НЯК до начала терапии и после ее окончания.
Результаты
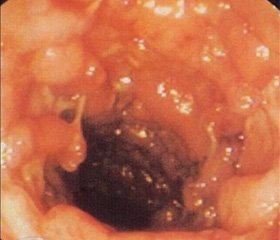
Клиника НЯК была типичной и характеризовалась нарушениями стула, поносами от 4 до 10 раз в день с примесью крови и слизи, тенезмами, ночными дефекациями, вздутиями кишечника, болевым, астеноневротическим синдромами. Среди обследованных больных НЯК у 25 (62,5 %) пациентов было выявлено среднетяжелое течение, а у 15 (37,5 %) диагностировано легкое течение НЯК. При эндоскопическом исследовании у всех больных НЯК до терапии выявляли гиперемию СОТК с изменением сосудистого рисунка, отечность слизистой толстой кишки с «зернистостью» — грануляциями мембранной поверхности слизистой оболочки, рассеивающими отраженный свет. Эрозии или язвы, повышенная ранимость СОТК, примеси слизи, фибрина, гноя обнаружены практически у всех больных, и степень выраженности этих изменений коррелировала со степенью тяжести НЯК.
До терапии у всех больных НЯК выявлено снижение числа бокаловидных клеток, при этом степень их уменьшения коррелировала с тяжестью НЯК и варьировала от незначительного уменьшения количества бокаловидных клеток с преобладанием клеток с мелкими, незрелыми вакуолями у больных НЯК легкой степени до выраженного снижения и иногда полного отсутствия бокаловидных клеток у пациентов со среднетяжелым течением НЯК. Выявлены истончение, дистрофия поверхностного эпителия с перестройкой крипт, кроме того, у всех больных обнаруживались дефекты поверхностного эпителия — от микроэрозий до глубоких язв, заполненных некротическими массами. На этом фоне у всех больных НЯК выявлена усиленная воспалительная клеточная инфильтрация слизистой оболочки толстой кишки, интенсивность которой колебалась от умеренной до выраженной.
В воспалительном клеточном инфильтрате у больных НЯК чаще преобладали лимфоциты — 24 (80 %) больных, плазмоциты преобладали у 18 (60 %) пациентов, а макрофаги — у 14 (46,7 %) больных. Нейтрофилы обнаруживались в инфильтрате у 18 (60 %) больных НЯК, при этом активные сегментоядерные лейкоциты, содержащие гликоген, обнаружены у 13 (43,3 %) пациентов. Более чем у половины больных НЯК выявлялись внутриэпителиальные лимфоциты, что свидетельствует об активности воспалительного процесса.
Помимо изменений клеточного состава слизистой оболочки толстой кишки у больных НЯК выявлены нарушения слизеобразования. У всех больных выявлено уменьшение количества внутриклеточной и внеклеточной слизи с изменением ее свойств. При проведении PAS-реакции, окрашивании альциановым синим рН 2,5 и рН 1,0 интенсивность окрашивания у всех больных НЯК была ниже нормы (P < 0,01), что свидетельствует об изменениях состава толстокишечной слизи, уменьшении в ней гликозамингликанов и гликопротеинов.
Уровень экспрессии секреторного (MUC2) и мембраносвязанных (MUC3, MUC4) муцинов у всех пациентов с НЯК был низким, при этом наиболее выраженным было снижение MUC2 и MUC3, проявляющееся негомогенностью окрашивания вакуолей бокаловидных клеток вплоть до его полного отсутствия, что свидетельствует о значительном снижении секреторной активности СОТК, снижении ее протективной функции при НЯК. При этом отмечалось интенсивное окрашивание муцинов в цитоплазме вокруг вакуолей и умеренное — в базальных отделах клеток эпителия, что может отражать высокую интенсивность метаболических процессов в эпителиальных клетках кишечника. В то же время низкая экспрессия MUC2 и MUC3 в поверхностном эпителии, выявленная у большинства обследованных пациентов с НЯК, может характеризовать неэффективность репаративных процессов слизистой оболочки при обострении заболевания (рис. 1а).
У 29 (59,2 %) обследованных больных НЯК отмечалось окрашивание клеток стромы от слабой до высокой экспрессии как MUC2, так и MUC3, что свидетельствует об активности митоза и процессов дифференцировки эпителиальных клеток стромы в бокаловидные экзокриноциты. Эти изменения могут индуцироваться высокой интенсивностью воспалительного процесса в толстом кишечнике и носить компенсаторный характер (рис. 1б). Экспрессия секреторных муцинов индуцируется провоспалительными цитокинами: TNF-а, INF-у, IL-6. Поэтому ее отсутствие в вакуолях бокаловидных клеток и появление в строме свидетельствует также о локализации воспалительного процесса в собственной пластинке СОТК, характерной для НЯК. В то же время хроническое воспаление, вызванное бактериальными инфекциями (энтеропатогенная и гемолизирующая E.coli, Salmonella enteritidis, Clostridium difficile и др.), ассоциируется с повышенной экспрессией секреторных муцинов в поверхностных отделах, ограничивая проникновение микроорганизмов в глубь слизистой оболочки кишечника, что может являться дополнительным дифференциально-диагностическим критерием.
Уровень MUC4 был низким у большинства больных НЯК, однако снижался в меньшей степени по сравнению с MUC2 и MUC3 (рис. 1в). В то же время у трети обследованных больных экспрессия MUC4 была высокой.
Избыточная активация трансмембранных муцинов приводит к стимуляции ядерного фактора транскрипции (NF-kB) и канонического ингибитора ядерного фактора кВ киназы в (IKK-в), ассоциирующихся с неоплазией, индуцированной хроническим воспалением, что может объяснять высокую частоту малигнизации при длительном течении НЯК.
Экспрессия TFF3 в слизистой оболочке толстого кишечника у больных НЯК в целом по группе была высокой в отличие от секреторных муцинов, что свидетельствует о нарушении регуляторного влияния трефоиловых пептидов на экспрессию и протективные свойства муцинов.
При этом локализация TFF3 также характеризовалась неравномерностью: в большей степени экспрессия наблюдалась в базальных отделах клеток крипт, умеренная — в вакуолях бокаловидных клеток (рис. 1г). В некоторых случаях отмечалась выраженная поверхностная локализация TFF3 в сочетании с отсутствием или низкой экспрессией MUC2 и MUC3, что, вероятно, отражает истощение секреторной функции бокаловидных клеток при сохранении стимулирующего влияния TFF3 на муцинообразование в ответ на воспаление.
Следовательно, для больных НЯК характерно снижение защитного слизистого барьера как за счет уменьшения разреженного (MUC2 и MUC3), так и за счет плотного слоя муцинов, сформированного в большей степени мембрановстроенными муцинами (MUC3 и MUC4). Наблюдается нарушение взаимодействия муцинов и трефоилового фактора, что снижает протективные свойства муцинов и регенераторный потенциал слизистой оболочки толстого кишечника у больных НЯК. Это приводит к уменьшению толщины и вязкости мукозного слоя СОТК, снижению колонизационной резистентности вследствие отсутствия питательного субстрата для жизнедеятельности облигатной флоры. Уменьшение толщины слизистого слоя способствует снижению как гуморального (IgA), так и клеточного компонентов защитного барьера, локализованных в мукозном геле, повышению проницаемости кишечного барьера для различных токсинов, микроорганизмов, бактериальных полисахаридов, индуцирующих и поддерживающих иммунный воспалительный ответ в кишечнике.
Степень выраженности выявленных изменений экспрессии муцинов варьировала в зависимости от степени тяжести НЯК. Так, у пациентов со слабой активностью НЯК отмечались значительные нарушения экспрессии MUC2, который не определялся у 90 % больных. MUC3 был выявлен только у 20 % пациентов. В то же время умеренная экспрессия MUC4 отмечалась более чем у половины больных — 62 %, а высокая — у 38,5 % пациентов, что, вероятно, свидетельствует о компенсаторном увеличении синтеза мембраноассоциированного муцина (MUC4) на фоне снижения общей секреторной активности. Отмечалась высокая экспрессия TFF3 у 70 % больных с легкой степенью тяжести НЯК, в то же время у 15 % обследованных TFF3 не определялся.
Достоверных отличий экспрессии MUC2 и MUC3 между группами больных с легкой и средней степенью тяжести НЯК выявлено не было. У пациентов с умеренной степенью тяжести НЯК экспрессия секреторного MUC2 выявлялась только у 30 %, а мембраносвязанного MUC3 — у 35 % больных, при этом выраженность экспрессии муцинов была минимальной. В то же время более выраженные нарушения экспрессии MUC4 были выявлены у больных со средней степенью тяжести НЯК: отсутствие MUC4 наблюдалось у 28 % больных, низкая экспрессия — у 38 % и умеренная — у 34 % больных НЯК. В этой группе также преобладали пациенты с выраженной экспрессией TFF3.
У 100 % больных НЯК тяжелой степени отмечалось абсолютное отсутствие экспрессии MUC2 и MUC3 в бокаловидных клетках, экспрессия MUC4 отмечалась у 70 % больных, однако была низкой, что свидетельствует о наиболее выраженных изменениях синтеза и секреции муцинов у этой группы пациентов. Стимулирующее влияние провоспалительных цитокинов на экспрессию и секрецию муцинов, вероятно, нивелировалось длительным течением заболевания и истощением компенсаторных механизмов защиты слизистого слоя кишечника у обследованных больных НЯК. Уровень TFF3 был низким у 30 % обследованных, высокая экспрессия сохранялась у 70 % больных НЯК с высокой активностью воспалительного процесса в толстом кишечнике.
Таким образом, наиболее выраженные нарушения экспрессии муцинов наблюдались у больных НЯК тяжелой степени с выраженной активностью воспалительного процесса в толстом кишечнике. Значительное снижение секреторных и трансмембранных муцинов отмечалось при средней степени тяжести НЯК. Повышение экспрессии муцинов наблюдается в фазе ремиссии НЯК, что отражалось на уровне MUC4 в группе больных с минимальной активностью заболевания (легкая степень тяжести НЯК). Степень выраженности нарушений экспрессии муцинов коррелировала с активностью воспалительного процесса в толстом кишечнике у больных НЯК, отражала эффективность компенсаторных процессов в зависимости от стадии заболевания.
1. Intestinal barrier dysfunction in inflammatory bowel diseases / M.A. McGuckin, R. Eri, L.A. Simms et al. // Inflamm. Bowel Dis. — 2009. — № 15. — Р. 100-113.
2. Role of intestinal mucins in innate host defense mechanisms against pathogens / Р. Dharmni, V. Srivatava, V. Kissoon-Singh et al. // J. Innate Immun. — 2009. — № 1. — Р. 123-135.
3. Perez-Vilar J. Mucin granule intraluminal organization / J. Perez-Vilar // Am. J. Respir. Cell Mol. Biol. — 2008. — № 36(2). — Р. 183-190.
4. Kim Y.S. Intestinal goblet cells and mucins in health and disease: recent insights and progress / Y.S. Kim, S.B. Ho // Curr. Gastroenterol. Rep. — 2010. — № 12. — P. 319-330.
5. Linden S.K. Mucin dynamics in intestinal bacterial infection / S.K. Linden, T.H.J. Florin, M.A. McGuckin // PLoS ONE. — 2008. — V. 3(12). — P. 3952-3966.
6. MUC1, MUC2, MUC4, and MUC5AC expression in salivary gland mucoepidermoid carcinoma: diagnostic and prognostic implications / A. Handra-Luca, G. Lamas, J.C. Bertrand et al. // Am. J. Surg. Pathol. — 2005. — № 29. — Р. 881-889.

/082/082.jpg)