Журнал «» 5 (31) 2013
Вернуться к номеру
Оцінка антигіпертензивної ефективності та впливу на жорсткість артерій раміприлу (Рамізес), призначеного у вигляді монотерапії або в комбінації з амлодипіном (Аладин), у пацієнтів з м’якою та помірною артеріальною гіпертензією
Авторы: Радченко Г.Д., Торбас О.О., Доброход Г.С., Сіренко Ю.М., Поліщук С.А. - ДУ «ННЦ «Інститут кардіології ім. акад. М.Д. Стражеска» НАМН України», м. Київ
Рубрики: Семейная медицина/Терапия, Кардиология
Разделы: Справочник специалиста
Версия для печати
Метою дослідження було оцінити антигіпертензивну ефективність та вплив раміприлу (препарат Рамізес компанії ВАТ «Фармак», Україна) у вигляді монотерапії або в комбінації з амлодипіном (препарат Аладин компанії ВАТ «Фармак», Україна) на центральний артеріальний тиск (АТ) та швидкість поширення пульсової хвилі по артеріях еластичного (ШППХе) та м’язового (ШППХм) типів у пацієнтів із м’якою та помірною артеріальною гіпертензією (АГ).
У дослідження було включено 37 пацієнтів із м’якою та помірною АГ (середній вік — 53,40 ± 2,35 року). Усім пацієнтам на початку дослідження та на етапах лікування проводили такі дослідження: вимірювання маси тіла та зросту, вимірювання офісного систолічного АТ (САТ), діастолічного (ДАТ) та частоти серцевих скорочень, добове моніторування АТ, визначення швидкості поширення пульсової хвилі по артеріях еластичного та м’язового типів, центрального САТ, біохімічне дослідження крові, ЕКГ. Після рандомізації призначали раміприл у дозі 10 мг. Якщо рівень АТ через 1 місяць лікування був більшим за цільовий, то додавали амлодипін 5 мг, дозу якого збільшували до 10 мг при неефективності терапії на 2-му місяці лікування. Тривалість лікування становила 3 місяці.
За даними офісного вимірювання АТ тримісячне лікування ефективно знижувало офісний САТ/ДАТ із 152,7 ± 3,6/92,7 ± 2,2 мм рт.ст. до 133,0 ± 1,9/80,9 ± 1,6 мм рт.ст. Цільовий офісний АТ було досягнуто на монотерапії у 21 (56,8 %) та на комбінованій терапії у 36 (97,3 %) пацієнтів. Середнє зниження середньодобового САТ/ДАТ становило 14,1 ± 0,9/5,1 ± 0,2 мм рт.ст., дСАТ/дДАТ — 14,8 ± 0,4/7,4 ± 0,3 мм рт.ст. та нСАТ/нДАТ — 11,5 ± 0,3/3,2 ± 0,1 мм рт.ст. Цільового середньодобового САТ та ДАТ було досягнуто у 17 (45,9 %) на монотерапії раміприлом та у 29 (78,4 %) пацієнтів на комбінації раміприл + амлодипін. Позитивний вплив призначеної терапії підтверджувався достовірним зниженням варіабельності дСАТ, Макс.САТ, Макс. ДАТ, індексів навантаження часом та площею для 24САТ, дСАТ, нСАТ, 24ДАТ, дДАТ та нПАТ. Лікування супроводжувалося достовірним зниженням центрального САТ з 129,5 ± 2,2 мм рт.ст. до 118,5 ± 1,5 мм рт.ст. та покращенням пружно-еластичних властивостей артерій еластичного типу, що проявлялося достовірним зменшенням ШППХе, ШППХм та індексу приросту. Частота побічних реакцій становила 5,4 % (2,7 % на монотерапії).
Целью исследования было оценить антигипертензивную эффективность и влияние рамиприла (препарат Рамизес компании ОАО «Фармак», Украина) в виде монотерапии или в комбинации с амлодипином (препарат Аладин компании ОАО «Фармак», Украина) на центральное артериальное давление и скорость распространения пульсовой волны по артериям эластического (СРПВэ) и мышечного типов (СРПВм) у пациентов с мягкой и умеренной артериальной гипертензией (АГ).
В исследование было включено 37 пациентов с мягкой и умеренной АГ (средний возраст — 53,40 ± 2,35 года). Всем пациентам исходно и на этапах наблюдения проводили исследования: измерение массы тела и роста, измерение офисного систолического АД (САД), диастолического (ДАД), частоты сердечных сокращений, суточное мониторирование АД, определение СРПВэ и СРПВм, центрального САД, биохимическое исследование крови, ЭКГ. После рандомизации назначали рамиприл 10 мг/сут. Если уровень АД через 1 месяц был выше целевого, то добавляли амлодипин 5 мг/сут, дозу которого увеличивали до 10 мг при неэффективности терапии на 2-м месяце лечения. Длительность терапии составила 3 месяца.
По данным офисного измерения АД трехмесячное лечение эффективно снижало офисный САД/ДАД с 152,7 ± 3,6/
92,7 ± 2,2 мм рт.ст. до 133,0 ± 1,9/80,9 ± 1,6 мм рт.ст. Целевой офисный АД был достигнут на монотерапии у 21 (56,8 %) и на комбинированной терапии у 36 (97,3 %) пациентов. Среднее снижение среднесуточного САД/ДАД составило 14,1 ± 0,9/
5,1 ± 0,2 мм рт.ст., дСАД/дДАД — 14,8 ± 0,4/7,4 ± 0,3 мм рт.ст. и нСАД/нДАД — 11,5 ± 0,3/3,2 ± 0,1 мм рт.ст. Целевые среднесуточные САД и ДАД были достигнуты у 17 (45,9 %) на монотерапии рамиприлом и у 29 (78,4 %) пациентов на комбинации рамиприл + амлодипин. Позитивное влияние назначенной терапии подтверждалось достоверным снижением вариабельности дСАД, Макс.САД, Макс.ДАД, индексов нагрузки временем и площадью для 24САД, дСАД, нСАД, 24ДАД, дДАД и нПАД. Лечение сопровождалось достоверным снижением центрального САД с 129,5 ± 2,2 мм рт.ст. до 118,5 ± 1,5 мм рт.ст. и улучшением упруго-эластических свойств артерий эластического типа, что проявлялось достоверным снижением СРПВэ, СРПВм и индекса прироста. Частота побочных реакций составила 5,4 % (на монотерапии — 2,7 %).
The aim of study was to evaluate of antihypertensive effectiveness and influence on arterial stiffness of ramipril (Ramizes manufactured by Farmak JSC, Ukraine) as monotherapy or in combination with amlodipine (Aladin by by Farmak JSC, Ukraine) on central blood pressure (BP) and pulse ware velocity (PWVe) in elastic and muscular arteries (PWVm) in patients with mild-to-moderate arterial hypertension (AH).
There were included 37 patients with mild-to-moderate AH (mean age — 53.40 ± 2.35 years). All patients at baseline and at the stages of observation conducted studies : measurement of weight and height, the measurement of office systolic BP (SBP), diastolic (DBP), heart rate, 24-hour BP monitoring, identification and PWVe and PWVm, central BP, biochemical blood analysis, ECG. After randomization, patients were administered ramipril 10 mg/day. If BP level in 1 month was higher than the target one, then added amlodipine 5 mg/day, the dose of which was increased to 10 mg for treatment failure on the 2nd month of treatment. The duration of therapy was 3 months.
According to the office BP measurement, three-month treatment effectively reduced the office SBP/DBP from
152.7 ± 3.6/92.7 ± 2.2 mmHg to 133.0 ± 1.9/80.9 ± 1.6 mmHg. The target office BP level was achieved in 21 (56.8 %) patients on montherapy and in 36 (97.3 %) on combination therapy. The mean lowering of daily average SBP/DBP was 14.1 ± 0.9/5.1 ± 0.2 mmHg, dSBP/dDBP — 14.8 ± 0.4/
7.4 ± 0.3 mmHg and nSBP/nDBP — 11.5 ± 0.3/
3.2 ± 0.1 mmHg. The target daily average SBP and DBP were achieved in 17 (45.9 %) patients on monotherapy and in 29 (78.4 %) on combination ramipril + amlodipine. Positive antihypertensive effects were confirmed by significant reduction in variability of dSBP, maxSBP, maxDBP, time load and pressure indices 24SBP, dSBP, nSBP, 24DBP, dDBP and nDBP. Treatment was associated with a significant decrease of central SBP from 129.5 ± 2.2 mmHg to 118.5 ± 1.5 mmHg and improvment of for arteries of elastic type, that mainifested in recudtion of PWVe, PWVm and aortic index. Adverse reactions rate was 5.4 % (on combination — 2.7 %).
антигіпертензивна ефективність, центральний артеріальний тиск, жорсткість артерій, раміприл.
антигипертензивная эффективность, центральное артериальное давление, жесткость артерий, рамиприл.
антигипертензивная эффективность, центральное артериальное давление, жесткость артерий, рамиприл.
Інгібітори ангіотензинперетворюючого ферменту (АПФ) широко увійшли в практику лікування артеріальної гіпертензії (АГ), серцевої недостатності, дисфункції лівого шлуночка, нефропатій та цукрового діабету [2, 4, 5, 13, 21, 28, 33, 37, 45]. Препарат раміприл, що належить до даного класу, все ще вважається новим для ринку України, незважаючи на те, що патент на виробництво раміприлу було одержано в 1991 році, а вже в кінці 90х з’явилися результати дослідження НОРЕ, що дозволило FDA зареєструвати раміприл для лікування пацієнтів високого ризику виникнення серцевосудинних ускладнень у 2000 році [14, 19, 46]. На теперішній час існує чи не найбільша серед інгібіторів АПФ кількість багатоцентрових досліджень щодо ефективності раміприлу при різній серцевосудинній патології [6, 11, 12, 14, 24, 26, 27–32, 43, 44, 46, 47 55, 56]. Практично немає станів у кардіології, при яких би за відсутності протипоказань не можна було би призначати цей препарат.
З огляду на останні рекомендації з лікування АГ у більшої половини хворих доцільним є призначення комбінованої антигіпертензивної терапії [33]. Як правило, це пацієнти з рівнем артеріального тиску (АТ) 160/100 мм рт.ст. і вище або з високим ризиком виникнення серцевосудинних ускладнень. Найбільш популярною до недавнього часу була комбінація інгібітори АПФ + діуретик. Але два великих дослідження ACCOMPLISH і ASCOT продемонстрували переваги іншої комбінації — інгібітор АПФ + антагоніст кальцію (АК) [22, 23, 25, 34, 35, 57]. Причому якщо раніше вважалося, що з АК краще призначати недигідропіридинові, то тепер після цих та кількох інших (VALUE, ALLHAT) досліджень хвалебні слова звучать у бік саме дигідропіридинових. Причинами більшої ефективності в попередженні серцевосудинних ускладнень у дослідженні ASCOT комбінації амлодипін + інгібітор АПФ називають такі: комбінація сприяє більш жорсткому контролю артеріального тиску — краще знижується центральний АТ, краще контролюється нічний АТ, зменшується варіабельність АТ; сумується позивний органопротекторний ефект інгібіторів АПФ та АК; зменшується кількість побічних реакцій та, відповідно, покращується прихильність хворих до терапії.
Дуже цікавим залишається вивчення впливу різних препаратів та їх комбінацій на центральний АТ та пружноеластичні властивості артерій. У дослідженні ASCOT показано, що існує різниця між препаратами у ступені зниження центрального АТ при однаковому зниженні офісного АТ [57]. За даними останнього метааналізу, всі класи антигіпертензивних препаратів зменшують жорсткість аорти при однаковому довготривалому зниженні АТ, але деякі препарати (інгібітори АПФ та сартани) роблять це значно раніше, що може вплинути на прогноз [39]. В Україні подібних досліджень мало, особливо з препаратами вітчизняного виробництва. Тому метою нашого дослідження було: оцінити антигіпертензивну ефективність та вплив раміприлу (препарат Рамізес компанії ВАТ «Фармак», Україна) у вигляді монотерапії або в комбінації з дигідропіридиновим АК амлодипіном (препарат Аладин компанії ВАТ «Фармак», Україна) на центральний АТ та швидкість поширення пульсової хвилі по артеріях еластичного та м’язового типів у пацієнтів із м’якою та помірною АГ.
Матеріали та методи
Матеріали. У дослідження було включено 39 пацієнтів із м’якою та помірною АГ. Проте дві пацієнтки відмовилися від участі в дослідженні через особисті причини і не прийшли на повторні обстеження. Тому в остаточний аналіз було включено лише 37 хворих. Критеріями включення були: вік понад 18 років, рівень АТ 140–179/90–109 мм рт.ст., згода пацієнта на участь у дослідженні, відсутність критеріїв виключення.
Критеріями виключення були: ангіоневротичний набряк в анамнезі, гіперкаліємія (> 5,5 ммоль/л) або гіпокаліємія (< 3,5 ммоль/л), стенотичне двостороннє ураження судин нирок, гостра серцева недостатність, порушення серцевого ритму (хронічна фібриляція передсердь, часта екстрасистолічна аритмія, шлуночкова або надшлуночкова тахікардія, тахікардія (частота серцевих скорочень (ЧСС) понад 100 уд/хв), порушення атріовентрикулярної провідності, або синусова брадикардія, або синдром слабкості синусового вузла, наявність вад серця, вагітність або лактація, злоякісний перебіг АГ, рівень АТ 180/110 мм рт.ст. і більше, вторинна артеріальна гіпертензія, виражена артеріальна гіпотонія (систолічний АТ (САТ) нижче 90 мм рт.ст.), бронхіальна астма, декомпенсовані захворювання печінки (рівень аспартатамінотрансферази (АСТ), аланінамінотрансферази (АЛТ) вище верхньої границі норми у 3 рази), гостра або хронічна ниркова недостатність (рівень креатиніну сироватки крові 133 мкмоль/л), серцева недостатність вища за II функціональний клас (згідно з НьюЙоркською класифікацією), інфаркт міокарда в анамнезі, гостре порушення мозкового кровообігу в анамнезі у строк 6 місяців до скринінгу, наявність стенокардії напруги більше ІІ класу або вазоспастичної стенокардії, інфекційні та онкологічні захворювання, стани, що супроводжуються ендогенною депресією (чи наявністю депресивних станів у сім’ї), цукровий діабет, ожиріння, індекс маси тіла > 35 кг/м2, виражені захворювання периферичних судин, синдром Рейно, стан після хірургічного втручання (менше одного місяця), прийом стероїдних та нестероїдних протизапальних засобів, контрацептивів, значні психічні розлади, неможливість відмінити попередню антигіпертензивну терапію, участь в іншому дослідженні.
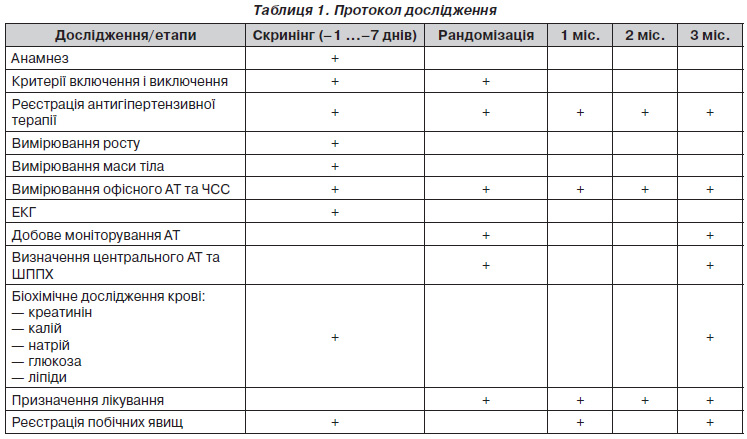
Протокол дослідження наведений у табл. 1. Усім пацієнтам на початку дослідження та на етапах лікування проводили такі дослідження: вимірювання маси тіла та зросту, вимірювання офісного САТ, діастолічного АТ (ДАТ) та ЧСС, добове моніторування АТ (ДМАТ), визначення швидкості поширення пульсової хвилі по артеріям еластичного (ШППХе) та м’язового (ШППХм) типів, визначення центрального САТ, біохімічне дослідження крові (визначення рівнів калію, натрію, креатиніну, АЛТ, АСТ, глюкози, загального холестерину, тригліцеридів), ехокардіографія (ЕКГ).
Вимірювання САТ та ДАТ проводили на початку дослідження, після семиденної (в разі необхідності) відміни всіх антигіпертензивних препаратів та на етапах спостереження. Вимірювали АТ у положенні сидячи тричі з інтервалом 1–2 хвилини. Визначали середнє з трьох вимірів. ЧСС визначали після другого вимірювання.
Індекс маси тіла (ІМТ) визначали за формулою:
ІМТ = маса тіла/(ріст)2, кг/м2.
Реєстрацію ЕКГ проводили на шестиканальному самописці «Юнікард» (Україна). Визначали наявність загальноприйнятих ознак гіпертрофії лівого шлуночка (індекс Соколова (SV1 + RV5/RV6 > 35 мм), вольтажний індекс Корнела (R aVL + S V3 > 28 мм у чоловіків та > 20 мм — у жінок), індекс тривалості Корнела (вольтаж помножити на тривалість) > 2400 мм · мс, індекс Ромхілта — Естес > 5 балів) та порушення ритму [2].
ДМАТ проводили на портативному апараті АВРМ04 (Meditech, Угорщина). При цьому вивчали такі показники: середньодобовий (24), денний (д), нічний (н) та максимальний (Макс.) САТ і ДАТ, ЧСС. При комп’ютерному аналізі ДМАТ для САТ і ДАТ розраховували індекс навантаження часом (Час.Ін.), що характеризує часове перевантаження тиском впродовж доби і визначається як відсоток вимірів АТ, що перевищує 140/90 мм рт.ст. удень і 120/80 мм рт.ст. уночі. Також визначали індекс навантаження площею (Ін.Пл.), що є площею між кривою підвищеного АТ та лінією границі норми, а також варіант (Вар.) обчислювали як стандартне відхилення величини АТ. Крім того, за допомогою програмного забезпечення вираховували добовий індекс (ДІ) — відсоток зниження нічного АТ порівняно з денним. ДМАТ проводили в такому режимі: у денний час — кожні 15 хв, уночі (з 22:00 до 6:00) — кожні 30 хв. Хворі вели звичайний спосіб життя, зі звичайними побутовими фізичними і психоемоційними навантаженнями [52].
ШППХ та центральний АТ визначалися на апараті SphygmocorPVx (AtCor Medical Pty Ltd, Австралія), з’єднаному з персональним комп’ютером, що дозволяє проводити аналіз пульсової хвилі та визначати ШППХе та ШППХм. П’єзодатчики встановлювали на загальній правій артерії, на стегновій артерії та на радіальній артерії правого передпліччя під візуальним (на моніторі) та автоматичним контролем якості, що здійснювався за відповідної програми приладу. Час запізнювання пульсової хвилі та ШППХ, центральний АТ визначалися автоматично за допомогою програмного забезпечення приладу після введення величини відстані між датчиками, що вимірювалася сантиметровою смужкою. Для оцінки пружноеластичних властивостей артерій еластичного типу ШППХ визначали на сегменті «сонна артерія — стегнова артерія», для оцінки пружноеластичних властивостей артерій м’язового типу — на сегменті «сонна артерія — радіальна артерія». Окрім ШППХ, визначали також центральний АТ за допомогою програмного забезпечення приладу на основі артеріального тиску на плечовій артерії та формі отриманої пульсової хвилі у висхідній аорті (формула визначена виробником та проведена стандартизація при інтрааортальному вимірюванні артеріального тиску).
Біохімічні аналізи виконувалися на автоматичному фотометрі Livia (Сormay, Польща) в лабораторії ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» АМН України. Визначали рівень креатиніну, електролітів (калію та натрію), глюкози, загального ХС, тригліцеридів (ТГ), сироватки крові. Кліренс креатиніну, що відображає ШКФ, визначали розрахунково за формулою Cockroft — Gault. Проводили також загальноклінічні дослідження крові та сечі.
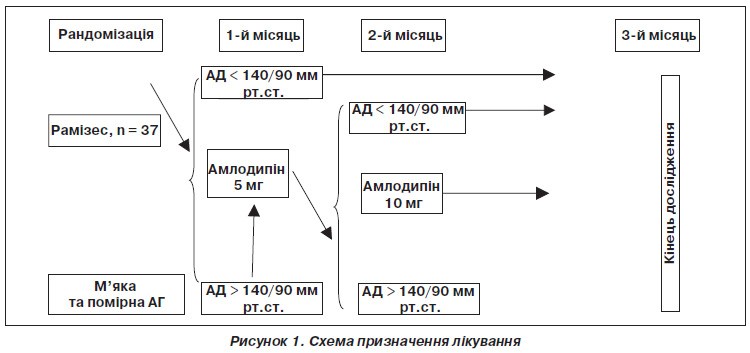
Лікування. Якщо пацієнти не приймали ліки на момент скринінгу, то в день рандомізації пацієнтам призначали раміприл (препарат Рамізес, компанія ВАТ «Фармак», Україна) у дозі 10 мг. Перший прийом ліків відбувався в офісі лікарядослідника. Оцінку антигіпертензивної ефективності проводили через місяць лікування. Якщо рівень АТ через 1 місяць лікування становив більше ніж 140/90 мм рт.ст., то до лікування основним препаратом додавали амлодипін 5 мг (препарат Аладин, компанії ВАТ «Фармак», Україна), дозу якого збільшували до 10 мг при неефективності терапії на 2му місяці лікування. Схема лікування наведена на рис. 1.
Якщо пацієнт до включення в дослідження отримував антигіпертензивні препарати, то рандомізації передував період відміни, що становив 7 днів. У кінці періоду відміни оцінювали повторно критерії включення в дослідження. Якщо пацієнт відповідав критеріям включення і не мав критеріїв виключення, то відбувалася рандомізація пацієнта за наведеною вище схемою. Тривалість лікування становила 3 місяці.
Супутнє лікування включало модифікацію способу життя, прийом статинів та ацетилсаліцилової кислоти.
Статистична обробка. Статистичну обробку результатів проводили після створення баз даних у системах Microsoft Excel. Середні показники обстежених пацієнтів визначали за допомогою пакету аналізу в системі Microsoft Excel. Усі інші статистичні розрахунки проводили за допомогою програми SPSS 13.0. Порівняння динаміки показників на етапах лікування проводили за допомогою парного двовідбіркового tтесту для середніх.
Результати дослідження та їх обговорення
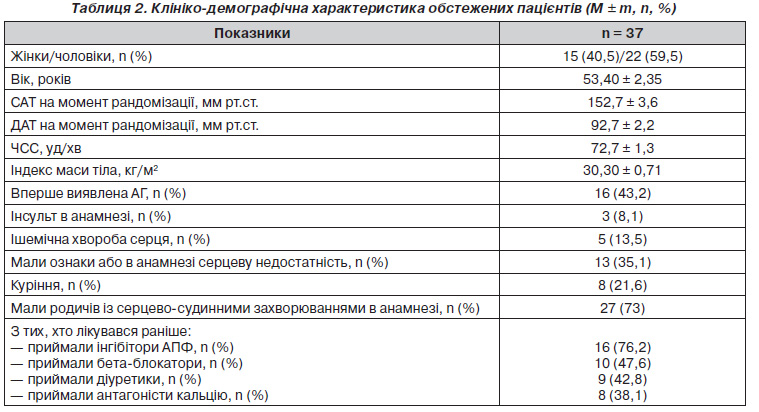
Характеристика включених у дослідження пацієнтів подана в табл. 2. Як видно з табл. 2, середній вік становив 53,40 ± 2,35 року, чоловіки були в більшості (59,5 %), середній рівень АТ відповідав критеріям включення, більшість хворих мали надлишкову масу тіла або ожиріння. Раніше лікувалися лише 56,8 % пацієнтів. З них найчастіше отримували інгібітори АПФ 76,2 % пацієнтів.
Ефективність терапії за даними офісного вимірювання АТ. Динаміка офісного АТ і ЧСС наведена на рис. 2. Як видно з рис. 2, на першому місяці прийому раміприлу спостерігалося вірогідне зниження офісних САТ/ДАТ із 152,7 ± 3,6/92,7 ± 2,2 мм рт.ст. до 142,2 ± 2,3/84,2 ± 1,6 мм рт.ст. (Р < 0,02), що продовжували знижуватися після додавання амлодипіну до 135,0 ± 2,2/82,9 ± 1,5 мм рт.ст. (Р < 0,001 порівняно з початком, Р < 0,05 порівняно з етапом 1 місяць) та 133,0 ± 1,9/80,9 ± 1,6 мм рт.ст. (Р < 0,001 порівняно з початком, Р < 0,005 — порівняно з етапом 1 місяць) відповідно на етапах 2 та 3 місяці. Середнє зниження САТ/ДАТ в обстежених хворих становило 10,8 ± 0,9/8,8 ± 1,2 мм рт.ст. на монотерапії раміприлом та 19,8 ± 0,8/11,9 ± 1,0 мм рт.ст. при комбінації з амлодипіном. Цільовий офісний АТ було досягнуто на монотерапії у 21 (56,8 %) пацієнта. Додатково амлодипін у дозах 5 та 10 мг відповідно призначався 16 (43,2 %) та 6 (16,2 %) обстеженим. На комбінованій терапії цільовий АТ досягався у 31 (83,8 %) та 36 (97,3 %) осіб відповідно на етапах 2 та 3 місяці лікування.
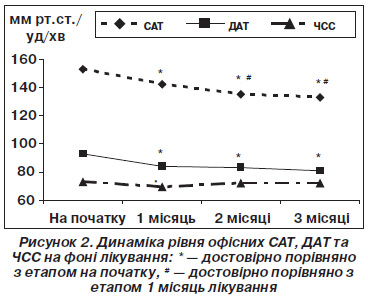
Офісна ЧСС достовірно зменшилася на етапі 1 місяць монотерапії раміприлом, що підтверджує дані про те, що інгібітори АПФ мають симпатолітичні властивості. На етапах 2 та 3 місяці спостереження офісна ЧСС достовірно не відрізнялася від початкової, що, ймовірно було пов’язано з призначенням амлодипіну, який, як відомо, сприяє активації симпатоадреналової системи.
За даними метааналізу Cochrane Collaboration2008 [18], у який увійшли результати 92 досліджень із вивчення ефективності монотерапії різними інгібіторами АПФ у 12954 пациентів із середнім віком 54,4 року, середнім рівнем АТ 157,1/101,2 мм рт.ст. та середньою тривалістю спостереження 6,2 тижня, середнє зниження САТ/ДАТ на раміприлі становило 6,29/4,14 мм рт.ст. Ця величина вираховувалася як різниця між зниженням АТ на фоні прийому препарату та на фоні плацебо. На фоні плацебо АТ, як правило, знижується на 3,2/3,7 мм рт.ст. Тобто якщо цей показник додати до отриманих 6,29/4,14 мм рт.ст., то можна сказати, що в середньому в групі хворих, які отримують раміприл, АТ знижується на 9,49/7,84 мм рт.ст., що є порівнянним із результатами нашого дослідження — 10,8 ± 0,9/8,8 ± 1,2 мм рт.ст.
Таким чином, призначене лікування раміприлом 10 мг/добу у вигляді монотерапії або комбінації з амлодипіном 5–10 мг/добу було ефективним щодо зниження офісного АТ у пацієнтів із м’якою та помірною АГ.
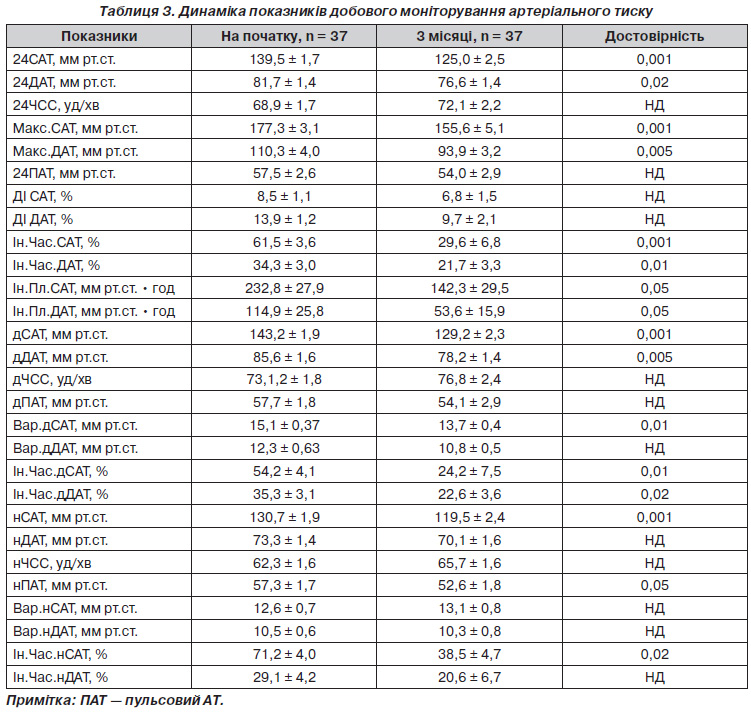
Ефективність за даними ДМАТ. Динаміка 24САТ/24ДАТ та середньодобових ЧСС (24ЧСС) наведена в табл. 3. Як видно з табл. 3, спостерігалося достовірне зниження середньодобових, денних та нічних САТ і ДАТ. Середнє зниження 24САТ/24ДАТ, дСАТ/дДАТ та нСАТ/нДАТ відповідно становило 14,1 ± 0,9/5,1 ± 0,2 мм рт.ст., 14,8 ± 0,4/7,4 ± 0,3 мм рт.ст. та 11,5 ± 0,3/3,2 ± 0,1 мм рт.ст. Цільовий середньодобовий САТ та ДАТ було досягнуто у 17 (45,9 %) на монотерапії раміприлом та у 29 (78,4 %) пацієнтів на комбінації раміприл + амлодипін. ЧСС, визначена при ДМАТ, достовірно не змінилася.
Ефективність терапії за даними ДМАТ була дещо нижчою, ніж за даними офісного вимірювання, що є порівнянним із даними літератури, згідно з якими частота досягнення цільового АТ за даними офісного вимірювання завжди вища, ніж при ДМАТ, адже офісне вимірювання — це лише частинка, яка характеризує підвищений протягом доби АТ [52].
Позитивний вплив терапії підтверджується динамікою інших показників ДМАТ (табл. 3). Так, достовірно знизилися варіабельність дСАТ, Макс.САТ, Макс.ДАТ, Час.Ін. для 24САТ, дСАТ, нСАТ, 24ДАТ, дДАТ, Ін.Пл.24САТ, Ін.Пл.24ДАТ. Окрім того, достовірно зменшився нПАТ, що може непрямо свідчити про покращення пружноеластичних властивостей аорти. Зниження варіабельності дСАТ можна вважати позитивною рисою антигіпертензивного лікування. В останні роки з’явилося багато публікацій, що свідчать про те, що різним впливом препаратів на варіабельність АТ можна частково пояснити різницю у прогнозі. Вважається, що дигідропіридинові АК є найбільш ефективними у зниженні варіабельності [42, 51].
Таким чином, призначене лікування раміприлом у вигляді монотерапії або ж у комбінації з амлодипіном супроводжується позитивною динамікою показників ДМАТ.
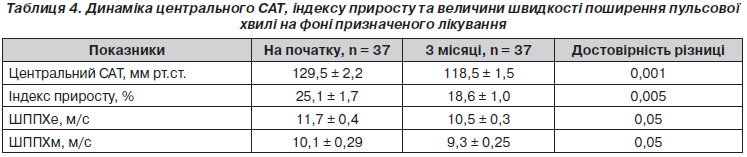
Вплив призначеного лікування на центральний АТ та жорсткість артерій наведений у табл. 4.
Як видно з табл. 4, на початку дослідження центральний САТ був значно меншим за рівень офісного САТ, але вищим за нормальні показники для центрального АТ 120–125 мм рт.ст. [53, 54]. На фоні лікування спостерігалося достовірне зниження цСАТ.
Показники, що характеризують пружноеластичні властивості артерій обох типів, також достовірно зменшилися під впливом призначеної терапії, що було наслідком як ефективного зниження АТ (зменшення АТ зменшує тиск розтягування), так і, можливо, позитивних структурних змін у стінках артерій. У попередніх наших дослідженнях було показано, що ШППХе достовірно зменшується під впливом будьякого ефективного щодо зниження АТ лікування, але для цього повинен минути певний час — мінімум 6 місяців [1]. У даному дослідженні ми отримали позитивні результати вже на 3му місяці терапії. Можливо, це пов’язано з більш легкою категорією включених у дослідження хворих — м’яка та помірна АГ без значних ускладнень (лише 3 пацієнти перенесли інсульт та 5 мали ішемічну хворобу без інфаркту міокарда в анамнезі) та цукрового діабету. У хворих із більш тяжкою АГ та супутніми станами потрібно більше часу для структурних змін у стінках артерій; зниження АТ в них не сильно зменшує тиск розтягування. Окрім того, не виключно, що застосування саме раміприлу у вигляді монотерапії або ж у комбінації з амлодипіном сприяло більш швидкому покращенню еластичності артерій, що раніше було показано в ряді досліджень [7, 8, 41].
Індекс приросту достовірно зменшився, що підтверджує позитивну дію терапії на центральний АТ. Це могло бути наслідком зменшення як жорсткості артерій, так і периферичного опору на фоні застосування вазодилататорів — інгібітора АПФ та АК.
Таким чином, отримані дані свідчать, що лікування раміприлом у вигляді монотерапії або ж в комбінації з амлодипіном призводить до достовірного зниження центрального САТ, індексу приросту та покращення пружноеластичних властивостей артерій обох типів.
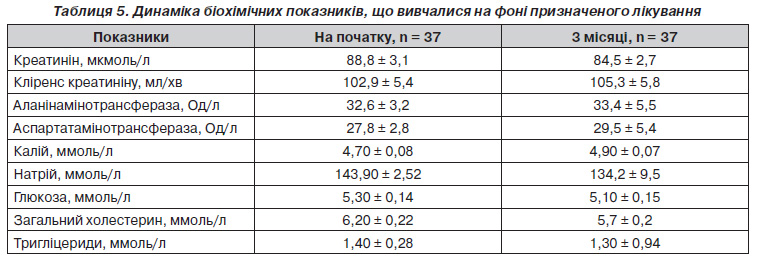
Влив призначеного лікування на біохімічні показники наведено в табл. 5.
Як видно з табл. 5, під впливом призначеної терапії достовірних змін показників, що вивчалися, не відбулося.
Таким чином, лікування на основі раміприлу було метаболічно нейтральним.
Оцінка переносимості. Призначене лікування добре переносилося хворими. Побічні реакції у вигляді кашлю виникли в однієї пацієнтки (2,7 %), у вигляді периферичних набряків — в одного пацієнта (2,7 %), якому було призначено амлодипін (6,3 % серед хворих, яким призначали амлодипін). Кашель виник на 3му місяці спостереження, а набряки на гомілках були незначними, тому пацієнти не виключалися з дослідження. Таким чином, частота побічних реакцій становила 5,4 %.
Згідно з офіційною інформацією та даними рандомізованих досліджень частота виникнення периферичних набряків на фоні монотерапії амлодипіном у середньому становить 8,3 % [20, 15–17, 38, 40]. Це менше, ніж у нашому дослідженні. В інших дослідженнях також продемонстровано меншу частоту набряків при комбінації амлодипіну з інгібіторами АПФ. Одним із пояснень цього є те, що при раціональному комбінуванні окремі компоненти нівелюють побічну дію один одного. Набряки на фоні АК пов’язані з його вираженим периферичним вазодилатуючим ефектом. Місцем прикладання є прекапілярні судини. При цьому притік крові збільшується, а відтік не змінюється. При додаванні інгібіторів АПФ відбувається додаткове розширення посткапілярних судин, що зменшує внутрішньокапілярний тиск [9, 10, 16], і вірогідність виникнення набряків також зменшується.
Частота виникнення кашлю у нашому дослідженні становила 2,7 %, що менше, ніж в інших дослідженнях за участю раміприлу, — 3–7,3 % [31, 32, 44, 46–48]. Загальна кількість побічних явищ у нашому дослідженні була також дуже низькою. В інших дослідженнях вона коливалася від 31 до 6,2 % [5, 6, 11, 14, 19, 24, 26, 27, 29–31, 32, 36, 43–50, 56]. Найбільш часто серед побічних реакцій, за даними літератури, зустрічається кашель, слабкість, запаморочення/гіпотензія, гастроінтестинальні порушення, головний біль. Серед пацієнтів — жителів США з АГ при короткостроковому лікуванні раміприлом головний біль відмічався у 5,4 %, запаморочення — у 2,2 %, кашель — у 3 %, слабкість — у 2 %, імпотенція — у 0,4 %, що, за винятком слабкості, не відрізнялося від плацебо [21]. У більшості випадків ці побічні дії були слабкої вираженості та не потребували відміни препарату. У дослідженні HOPE припинили лікування 32,6 % пацієнтів на раміприлі та 30,7 % на плацебо [14, 46]. Основними причинами цього були: кашель (7,3 проти 1,8 % у групі плацебо), гіпотензія/запаморочення (1,9 проти 1,5 % у групі плацебо), ангіоневротичний набряк (0,4 проти 0,2 % у групі плацебо), неконтрольована гіпертензія (2,3 проти 3,9 % у групі плацебо), розвиток клінічно значущих подій (6,7 проти 9 % у групі плацебо). Малу кількість побічних явищ у нашому дослідженні можна пояснити тим, що більшість пацієнтів, які отримували раміприл, мали вже досвід застосування інгібіторів АПФ і, відповідно, було відомо, що вони добре переносили дані препарати. Цим же, частково, можна пояснити малу кількість побічних реакцій у вигляді кашлю. Окрім того, можливо, саме комбінування з амлодипіном також цьому сприяло. Адже в дослідженнях із використанням комбінації периндоприл + амлодипін також було показано, що частота кашлю була меншою, ніж при застосуванні периндоприлу у вигляді монотерапії [3].
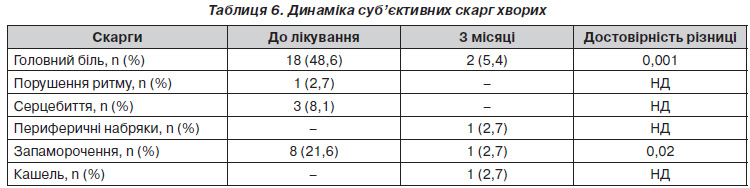
Динаміка cуб’єктивних скарг хворих, які були включені в дослідження, наведена в табл. 6. Як видно з табл. 6, на фоні лікування достовірно зменшилася частка хворих із такими скаргами, як головний біль та запаморочення.
Таким чином, лікування раміприлом у вигляді монотерапії або в комбінації з амлодипіном добре переносилися хворими протягом 3 місяців.
Таким чином, у нашому досліджені комбіноване тримісячне лікування на основі раміприлу у вигляді монотерапії або в комбінації із амлодипіном дозволило ефективно знизити офісний, добовий та центральний АТ, що супроводжувалося зменшенням жорсткості артерій, суттєво не впливало на показники вуглеводного та ліпідного обмінів та добре переносилося хворими з м’якою та помірною неускладненою АГ.
Висновки
1. За даними офісного вимірювання АТ тримісячне лікування на основі раміприлу у вигляді монотерапії або ж у комбінації з амлодипіном ефективно знижувало офісний САТ/ДАТ зі 152,7 ± 3,6/92,7 ± 2,2 мм рт.ст. до 133,0 ± 1,9/80,9 ± 1,6 мм рт.ст. Цільовий офісний АТ було досягнуто на монотерапії у 21 (56,8 %) та на комбінованій терапії у 36 (97,3 %) пацієнтів.
2. На фоні призначеної терапії середнє зниження середньодобового САТ/ДАТ становило 14,1 ± 0,9/5,1 ± 0,2 мм рт.ст., дСАТ/дДАТ — 14,8 ± 0,4/7,4 ± 0,3 мм рт.ст. та нСАТ/нДАТ — 11,5 ± 0,3/3,2 ± 0,1 мм рт.ст. Цільового середньодобового САТ та ДАТ було досягнуто у 17 (45,9 %) на монотерапії раміприлом та у 29 (78,4 %) пацієнтів на комбінації раміприл + амлодипін. ЧСС, визначена при ДМАТ, достовірно не змінилася.
3. Позитивний вплив призначеної терапії підтверджувався достовірним зниженням варіабельності дСАТ, Макс.САТ, Макс.ДАТ, Час.Ін. для 24САТ, дСАТ, нСАТ, 24ДАТ, дДАТ, Ін.Пл.24САТ, Ін.Пл.24ДАТ та нПАТ.
4. Лікування на основі раміприлу у вигляді монотерапії або ж у комбінації з амлодипіном супроводжувалося достовірним зниженням центрального САТ з 129,5 ± 2,2 до 118,5 ± 1,5 мм рт.ст. та покращенням пружноеластичних властивостей артерій еластичного типу, що проявлялося достовірним зменшенням ШППХе, ШППХм та індексу приросту.
5. Призначена терапія на основі раміприлу у вигляді монотерапії або ж у комбінації з амлодипіном добре переносилось хворими, призводячи до виникнення м’яких побічних реакцій, які не потребували відміни препаратів, лише у 5,4 % (2,7 % на монотерапії) хворих, та була метаболічно нейтральною.
1. Кушнір С.М. Діагностика ураження артеріальних судин у хворих на гіпертонічну хворобу та обгрунтування медикаментозної корекції: Автореф. дис... канд. мед. наук. — К.: Інвасервіс, 2010. — 24 с.
2. Сіренко Ю.М. Артеріальна гіпертензія. — Київ: Моріон, 2002. — 203 с.
3. Сиренко Ю.Н., Радченко А.Д., Дзяк Г.В. и др. Результаты открытого исследования по оценке антигиПЕРтензивной эффективноСти и ПЕреносимости БиПрестариума у пациентов с АГ, вновь диагностированной или не КонТролИроВАнной предыдущей терапией (Первичные результаты исследования ПЕРСПЕКТИВА) // Артериальная гипертензия. — 2010. — № 4. — С. 719.
4. 2007 Guidelines for the Management of Arterial Hypertension. The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and the European Society of Cardiology (ESC) // J. Hypertens. — 2007. — 11051187.
5. Abuissa H., O’Keefe J., Bell D. et al. ACE Inhibitors or ARBs for Prevention of Type 2 Diabetes: A metaanalysis of randomized clinical trials // J. Am. Coll Cardiol. — 2005. — Vol. 45. — P. 10A.
6. AgabitiRosei E., Ambrosioni E., Dal Palu C. et al. ACE inhibitor ramipril is more effective than betablocker atenolol in reducing left ventricular mass in hypertension. Results of the RACE (ramipril cardioprotective evaluation) study // J. Hypertens. — 1995. — Vol. 13. — P. 13251334.
7. Ahimastos A., Natoli A., Lawler A. et al. Ramipril Reduces LargeArtery Stiffness in Peripheral Arterial Disease and Promotes Elastogenic Remodeling in Cell Culture // Hypertension. — 2005. — Vol. 45. — P. 11941199.
8. Ahimastos A.A., Dart A.M., Lawler A., Blombery P.A., Kingwell B.A. Reduced arterial stiffness may contribute to angiotensinconverting enzyme inhibitor induced improvements in walking time in peripheral arterial disease patients // J. Hypertens. — 2008. — Vol. 26. — P. 10371042.
9. Bahl V., Jadhav U., Thacker H. Management of Hypertension with the Fixed Combination of Perindopril and Amlodipine in Daily Clinical Practice // Am. J. Cardivas. Drugs. — 2009. — Vol. 9. — P. 135142.
10. Bertrand M., Ferrari R., Remme W., Simoons M., Deckers J., on behalf of the EUROPA Investigators. Synergistic effect of perindopril and calcium channel blockers in revention of cardiac events and death in coronary artery disease patients: analysis from the EUROPA study // Am. Heart J. — 2010. — Vol. 159. — P. 795802.
11. Bosch J., Yusuf S., Pogue J. et al. Use of ramipril in preventing stroke: double blind randomized trial // BMJ. — 2002. — Vol. 324. — P. 699702.
12. Breyer Lewis J., Berl T., Bain R. et al. Effect of intensive blood pressure control on course of type 1 diabetic nephropathy // Am. J. Kidney Dis. — 1999. — Vol. 34. — P. 8098173.
13. Brown N., Vaughan D. Angiotensinconverting enzyme inhibitors // Circulation. — 1998. — Vol. 97. — P. 14111420.
14. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICROHOPE substudy. Heart Outcomes Prevention Evaluation Study Investigators // Lancet. — 2000. — Vol. 355. — P. 253259.
15. Fogari R., Malamani G., Zoppi A. et al. Effect on the development of ankle edema of adding delapril to manidipine in patients with mild to moderate essential hypertension: a threeway crossover study // Clin. Ther. — 2007. — Vol. 29. — P. 413418.
16. Fogari R., Malamani G.D., Zoppi A. et al. Effect of benazepril addition to amlodipine on ankle oedema and subcutaneous tissue pressure in hypertensive patients // J. Hum. Hypertens. — 2003. — Vol. 17. — P. 207212.
17. Fogari R., Mugellini A., Derosa G. Efficacy and tolerability of candesartan cilexetil/hydrochlorothiazide and amlodipine in patients with poorly controlled mildtomoderate essential hypertension // Journal of ReninAngiotensinAldosterone System. — 2007. — Vol. 8. — P. 139144.
18. Heran B.S., Wong M.M., Heran I.K., Wright J.M. Blood pressure lowering efficacy of angiotensin converting enzyme (ACE) inhibitors for primary hypertension // The Cochrane Collaboration. Cochrane database of Systematic Reviews. — 2008. — Issue 4. Art.No.:CD003823.DOI:10.1002/14651858.CD003823. pub2.
19. HOPE study. Design, results and clinical implications of the landmark study. — Hampshire: Euromed Communications Haslemere, 2000. — 22 p.
20. http: // www.rxlist.com/norvascdrug.htm
21. Hypertension Disease Management Guide. — NJ: Tomson PDR, 2003. — 709 p.
22. Jamerson K.A., Bakris G.L., Wun C.C. et al. Rationale and design of the avoiding cardiovascular vents through combination therapy in patients living with systolic hypertension (ACCOMPLISH) trial: the first randomized controlled trial to compare the clinical utcome effects of firstline combination therapies in hypertension // Am. J. Hypertens. — 2004. — Vol. 17. — P. 793801.
23. Jamerson K., Bakris G.L., Dahlf B. et al. Exceptional early blood pressure control rates: the ACCOMPLISH trial // Blood Press. — 2007. — Vol. 16(2). — P. 8086.
24. Kaplan N. on behalf of the Clinical Altace RealWord Efficacy (CARE) Investigators. The CARE Study: a postmarketing evaluation of ramipril in 11 100 patients // Clin. Ther. — 1993. — Vol. 18. — P. 658670.
25. Kenneth J., Weber M., Bakris J., Dahlöf B., Pitt B., Shi V., Hester A., Gupte J., Gatlin M., Velazquez E. for the ACCOMPLISH Trial Investigators. Benazepril plus Amlodipine or Hydrochlorothiazide for Hypertension in HighRisk Patients // N. Engl. J. Med. — 2008. — Vol. 359. — P. 24172428.
26. KjollerHansen L., Steffensen R., Grade P. The angiotensinconverting enzyme inhibition post revascularization study (APRES) // J. Am. Coll. Cardiol. — 2000. — Vol. 35. — Р. 881888.
27. Koenign M. on behalf of the Multicentre Study Group. Ramipril vs lisinopril in treatment of mild to moderate primary hypertension — randomized doubleblind multicentre trial // Drug Invest. — 1992. — Vol. 4. — P. 450457.
28. Lewis E.J., Hunsiker L.G., Bain R.P., Rohde R.D. The effect of ACE inhibition on diabetic nephropathy. The Collaborative Study Group. // N. Engl. J. Med. — 1994. — Vol. 329. — P. 14561462.
29. Lievre M. Ramiprilinduced regression of left ventricular hypertrophy in treated hypertensive individuals // Hypertension. — 1995. — Vol. 25. — P. 9297.
30. Linz W. Ramipril prevents left ventricular hypertrophy with myocardial fibrosis without blood pressure reduction: a one year study in rats // Br. J. Pharmacol. — 1992. — Vol. 102. — P. 970975.
31. Lonn E., Yusuf S., Dzavik V. et al. SECURE Investigators. Effects of ramipril and vitamin E on atherosclerosis: the study to evaluate carotid ultrasound changes in patients treated with ramipril and vitamin E // Circulation. — 2001. — Vol. 103. — P. 919925.
32. MacMahon S., Sharpe N., Gamble G. et al. Prevention of atherosclerosis with ramipril Trial2 // J. Am. Coll Cardiol. — 2000. — Vol. 36. — P. 438443.
33. Mancia G., Laurent S., AgabitiRosei E. et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document // Journal of Hypertension. — 2009. — Vol. 27.
34. Manisty C., Zambanini A., Parker K. et al. on behalf of the AngloScandinavian Cardiac Jutcome Trial Investigators. Differences in the Magnitude of Wave Reflection Account for Differential Effects of Amlodipine — Versus AtenololBased Regimens on Central Blood Pressure An AngloScandinavian Cardiac Outcome Trial Substudy // Hypertension. — 2009. — Vol. 54. — P. 724730.
35. Matsui Y., Eguchi K., O’Rourke M. et al. Differential Effects Between a Calcium Channel Blocker and a Diuretic When Used in Combination With Angiotensin II Receptor Blocker on Central Aortic Pressure in Hypertensive Patients // Hypertension. — 2009. — Vol. 54. — P. 716723.
36. Moser M., Basile J., Miller E.R., Ferdinand K.C. Roundtable Discussion: Hypertension, Renal Disease and Diabetes // J. Clin. Hypertension. — 2002. — Vol. 4. — P. 113119.
37. National Kidney Foundation. Clinical Practice Guidelines for Chronic Kidney Disease: Evaluation, Classification and Stratification. Executive Summary. — New York, 2002. — 94 p.
38. Neutel J., Germino F., Smith D.Comparison of Monotherapy with Irbesartan 150 mg or Amlodipine 5 mg for Treatment of MildtoModerate Hypertension // Journal of ReninAngiotensinAldosterone System. — 2005. — Vol. 6. — P. 8489.
39. Ong K., Delerme S., Pannier B., Safar M. et al. Aortic stiffness is reduced beyond blood pressure lowering by shortterm and longterm antihypertensive treatment: a metaanalysis of individual data in 294 patients // J. Hypertens. — 2011. — Vol. 29. — P. 10341042.
40. Opie L.H., Schall R. Old antihypertensives and new diabetes // J. Hypertens. — 2004. — Vol. 22. — P. 14531458.
41. Rahman S., Ismail A.A., Ismail S.B., Naing N.N., Abdul Rahman A.R. Effect of rosiglitazone/ramipril on preclinical vasculopathy in newly diagnosed, untreated diabetes and IGT patients: 1year randomised, doubleblind, placebocontrolled study // Eur. J. Clin. Pharmacol. — 2007. — Vol. 63. — P. 73341.
42. Rothwell P., Howard S., Dolan E. et al. Prognostic significance of visittovisit variability, maximum systolic blood pressure, and episodic hypertension // Lancet. — 2010. — Vol. 375. — P. 895905.
43. Ruggenenti P., Perna A., Gherardi G. et al. Chronic proteinuric nephropathies: outcomes and response to treatment in a prospective cohort of 352 patients with different patterns of renal injury // Am. J. Kidney. Dis. — 2000. — Vol. 35. — P. 11551165.
44. Ruggenenti P., Perna A., Remuzzi G. ACE inhibitors to prevent endstage renal disease: when to start and why possibly never to stop: a post hoc analysis of the REIN trial results. Ramipril Efficacy in Nephropathy // J. Am. Soc. Nephrol. — 2001. — Vol. 12. — P. 28322837.
45. Schoolwerth A.C., Sica D.A., Ballerman B.J., Wilcox C.S. Renal Considerations in Angiotensin Converting Enzyme Inhibitor Therapy. AHA Scientific Statement // Circulation. — 2001. — Vol. 104. — P. 19851991.
46. Sleight P., Yusuf S., Pogue J. et al. Heart Outcomes Prevention Evaluation (HOPE) Study. Bloodpressure reduction and cardiovascular risk in HOPE study // Lancet. — 2001. — Vol. 358. — P. 21302131.
47. The Acute Infarction Ramipril Efficacy (AIRE) Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction: AIRE Extension (AIREX) study // Lancet. — 1997. — Vol. 349. — P.14931497.
48. The heart outcomes prevention evaluation study investigators. Effects of an angiotensinconvertingenzyme inhibitor, ramipril, on cardiovascular events in high risk patients // N. England J. Med. — 2000. — Vol. 342. — P. 145153.
49. Third joint task force of European and other Societies on Crdiovascular prevention in clinical practice. // European Heart Journal. — 2003. — Vol. 24. — P. 16011610.
50. Trivadi H., Pang M. Discrepancy in epidemiology of nondiabetic chronic renal insufficiency and endstage renal disease in black and white Americans: the third National Health and Nutrition Examination Survey and United States Renal data System // Am. J. Nephrol. — 2003. — Vol. 23. — P. 448457.
51. Webb A., Fischer U., DPhil Z., Rothwel P. Effects of antihypertensivedrug class on interindividual variation in blood pressure and risk of stroke: a systematic review and metaanalysis // Lancet. — 2010. — 375. — 90615.
52. White W. Blood pressure monitoring in Cardiovascular Medicine and Therapeutics. — N. Jersy: Humana Press, 2001. — 308 p.
53. Wilkinson I., Franklin S., Hall I. et al. Pressure Amplification Explains Why Pulse Pressure is unrelated to risk in young subjects // Hypertens. — 2001. — Vol. 38. — P. 14611466.
54. Wilkinson I., Ian R., Hall I., MacCallum H. et al. PulseWave Analysis Clinical Evaluation of a Noninvasive, Widely Applicable Method for Assessing Endothelial Function // Arterioscler. Thromb. Vasc. Biol. — 2002. — Vol. 22. — P. 147152.
55. Wright J.T. Jr., Bakris G., Greene T. et al. African American Study of Kidney Disease and Hypertension Study Group. Effect of blood pressure lowering and antihypertensive drug class on progression of hypertensive kidney disease: results from the AASK trial // JAMA. — 2002. — Vol. 288. — P. 24212431.
56. Wright J.T. Jr., Douglas J.G., Rahman M. Prevention of cardiovascular disease in hypertensive patients with normal renal function // Am. J. Kidney Dis. — 1998. — Vol. 32. — P. S66S79.
57. Zambanini A., Parker K. et al. on behalf of the AngloScandinavian Cardiac Jutcome Trial Investigators. Differences in the Magnitude of Wave Reflection Account for Differential Effects of Amlodipine — Versus AtenololBased Regimens on Central Blood Pressure An AngloScandinavian Cardiac Outcome Trial Substudy // Hypertension. — 2009. — Vol. 54. — P. 724730.