Журнал «Здоровье ребенка» 5 (56) 2014
Вернуться к номеру
Современные возможности и перспективы использования пробиотиков группы самоэлиминирующихся антагонистов в терапии инфекционных заболеваний
Авторы: Псахис И.Б., Маковская Т.Е. - Государственное предприятие «Научно-технический инженерный центр проблем водоочистки и водосбережения (НТИЦ «Водообработка») Физико-химического института им. А.В. Богатского; Национальной академии наук Украины»; Главный военно-медицинский клинический центр «ГВКГ»
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
В статье рассматривается вопрос применения пробиотиков в современной клинике инфекционных болезней. Уделено внимание таким препаратам, как Биоспорин и Субалин, исследованию культур микроорганизмов, полученных из различного отделяемого у 34 992 пациентов, и чувствительности микроорганизмов к этим препаратам.
У статті розглядається питання застосування пробіотиків у сучасній педіатрії. Приділена увага таким препаратам, як Біоспорин і Субалін, дослідженню культур мікроорганізмів, отриманих з різного виділюваного у 34 992 пацієнтів, і чутливості мікроорганізмів до цих препаратів.
The article discusses the use of probiotics in modern pediatrics. Attention is given to drugs such as Biosporin and Subalin, research of microorganisms cultures obtained from various discharge in 34,992 patients, and the sensitivity of microorganisms to these drugs.
пробиотики, микроорганизмы, штамм, чувствительность.
пробіотики, мікроорганізми, штам, чутливість.
probiotics, microorganisms, strain, sensitivity.
Статья опубликована на с. 134-138
Способность спорообразующих бактерий оказывать антагонистическое по отношению к патогенной и условно-патогенной флоре и пробиотическое действие привела к разработкам на их основе препаратов, отнесенных к группе самоэлиминирующихся антагонистов (СЭА) [3].
На сегодняшний день в мире создано более полусотни таких лекарственных средств. Хотя большинство бактерий, обладающих пробиотическими свойствами, являются представителями семейств Lactobacillus и Bifidobacterium, все чаще в качестве пробиотиков стали использоваться и спорообразующие бактерии из рода Bacillus [2]. В настоящее время в мире выпускается и реализуется огромное количество лекарственных средств, биологически активных добавок и продуктов функционального питания, которые содержат не только молочнокислые, но и спорообразующие бактерии пробиотического действия [8]. Этот вопрос является актуальным, если принимать во внимание тот факт, что целесообразность искусственного заселения нормальной микрофлоры остается дискутабельной темой в научном мире.
C учетом данных об антагонистическом действии спорообразующих бактерий по отношению к представителям патогенной флоры нами было принято решение изучить in vitro действие препаратов на основе B.subtilis на различные штаммы микроорганизмов: Staphylococcus aureus, Staphylococcus haemolyticus, Enterobacter aerogenes, рода Streptococcus, Escherichia coli, Proteus mirabilis, Proteus vulgaris, грибы рода Candida, Pseudomonas aeruginosa. Данные микроорганизмы наиболее часто выделяются из различного клинического материала (урогенитальное отделяемое, моча, кал, отделяемое из глаз и ушей, отделяемое из носа и зева, эякулят, секрет предстательной железы, содержимое акне, отделяемое из ран, мокрота). Выявление чувствительности вышеуказанных микроорганизмов к различным лекарственным средствам, оказывающим антагонистическое действие по отношению к ним, играет важную роль в лечении ряда заболеваний.
В качестве эталонных препаратов были выбраны Биоспорин и Субалин (препараты, содержащие различные штаммы В.subtilis). Наш выбор основан на том, что бациллы, содержащиеся в этих лекарственных препаратах, выделяют антибиотикоподобные вещества, так называемые бактериоцины и микоцины [3]. Bacillus subtilis выделяют в просвет кишечника субтилизин и ферменты, которые помогают разрушать и выводить эндотоксины патогенной и условно–патогенной флоры. Кроме того, ферменты Bacillus subtilis принимают участие в процессе пристеночного пищеварения [3]. Дипиколиновая кислота, также выделяемая Bacillus subtilis, является, с одной стороны, дополнительным фактором эрадикации патогенной и условно–патогенной флоры, с другой стороны, способствует росту собственной нормофлоры [3].
Кроме того, наш выбор связан и с полученными нами ранее данными. На базе микробиологической лаборатории ГП «НТИЦ “Водообработка” ФХИ им. А.В. Богатского НАН Украины» с 2000 по 2003 год были проведены исследования воды реки Днестр на всех этапах очистки, а также была исследована вода, прошедшая дополнительную очистку и озонирование на водоочистных сооружениях. Интересно, что в реке и на всех этапах очистки были обнаружены бактерии рода Bacillus. Виды бактерий рода Bacillus (Bacillus cereus 17а, В.cereus 25, В.cereus 26, B.coagulans 21а, B.laterosporus 17а, B.subtilis) являются непатогенными денитрифицирующими бактериями, и, кроме того, они проявляют, как уже говорилось ранее, антагонистическую активность по отношению к большинству условно-патогенных бактерий. Штаммы этих бактерий снижали количество представителей условно-патогенной флоры рода Enterobacteriacae, Pseudomonas, Staphylococcus и грибов рода Candida, которые обнаруживаются на механических и угольных фильтрах в любых установках очистки воды и по истечении времени начинают попадать в воду, повторно загрязняя ее.
Оба исследуемых лекарственных средства принадлежат к группе самоэлиминирующихся антагонистов, но содержат разные штаммы бацилл и имеют некоторые отличия в своем механизме действия.
Так, препарат Биоспорин содержит 2 представителей рода Bacillus — штаммы Bacillus subtilis УКМ В-5007 и Bacillus licheniformis УКМ-5514 и характеризуется достаточно выраженным антибактериальным действием. Данное свойство и определяет сферу применения препарата — преимущественно терапия острых кишечных инфекций бактериальной природы, лечение дисбактериоза [10].
Субалин же содержит только штамм Bacillus subtilis УКМ В-5020. При этом данный штамм представляет собой модифицированный микроорганизм, который обладает способностью самостоятельно продуцировать альфа-интерферон, что обусловливает наличие противовирусного и иммуномодулирующего действия. Соответственно, сферой применения данного препарата является терапия инфекций вирусной и смешанной (вирусно-бактериальной) природы [11].
Нас заинтересовал вопрос, как эти отличия будут проявляться в отношении действия препаратов на одних и тех же представителей патогенной и условно-патогенной флоры.
Материалы и методы
С января 2012 по март 2014 г. нами были проведены анализы различного отделяемого у 34 992 обследуемых. Использовались плотные дифференциально-диагностические среды Эндо, Плоскирева, Сабуро, 5% кровяной агар, желточно-солевой агар для выделения и видовой идентификации микроорганизмов. При идентификации бактерий использовались общепринятые классические дифференциально-диагностические среды, системы индикаторные бумажные. Определение видовой принадлежности микроорганизмов проводилось в соответствии с классификацией Bergy (9-е издание «Определителя бактерий Берги», 1984) [4]. Во время идентификации изолированных организмов наряду с общеприменяемыми методами использовали стандартизированные системы АРИ 20Е, АPI STAPH (bio Merieux S.A., France) для идентификации энтеробактерий и стафилококков.
Определение чувствительности микроорганизмов к Субалину и Биоспорину проводили следующим образом:
1. Выделенные и определенные до вида культуры микроорганизмов засевали на среду Мюллер — Хинтона и Сабуро на чашки Петри диаметром 60 мм [9].
2. Субалин и Биоспорин разводили стерильной водой (5 мл воды на 1 флакон препарата) согласно инструкции.
3. Стерильные бумажные диски пропитывали 0,01 мл суспензии культуры пробиотического штамма (109 КОЕ/мл) и наносили на среду с бактериальной культурой.
4. Далее определяли зоны задержки роста микроорганизмов, используя аттестованную линейку. Зоны задержки роста оцениваются следующим образом: > 15 мм — чувствительность микроорганизмов к Cубалину и Биоспорину, 5–15 мм — умеренная чувствительность, < 5 мм — устойчивость микроорганизмов к препаратам. Данные определены в нашей лаборатории статистическим методом.
Следует обратить внимание на хранение разведенного препарата. Разведенный препарат хранению не подлежит!
Результаты и их обсуждение
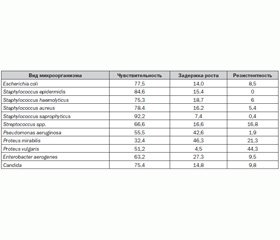
На протяжении 2 лет мы изучали культуры микроорганизмов, полученных из различного отделяемого (урогенитальное отделяемое (10 145 образцов), моча (8321), кал (5323), отделяемое из глаз (1253) и ушей (898), отделяемое из носа и зева (7221), эякулят (152), секрет предстательной железы (429), содержимое акне (993), отделяемое из ран (129), мокрота (128)). Чувствительность микроорганизмов к Субалину приведена в табл. 1.
Как видно из табл. 1, Субалин оказывает литическое действие на большинство видов микроорганизмов. Наибольшее его воздействие отмечено на бактерии рода Staphylococcus (S.aureus (78,4 %), S.epidermidis (84,6 %), S.haemolyticus (75,3 %), S.saprophyticus (92,2 %)). Также отмечается высокая чувствительность бактерий рода Enterobacteriacae (E.coli (77,5 %), E.aerogenes (63,2 %)) и грибов рода Сandida (75,4 %). Несколько меньшую чувствительность демонстрируют Proteus mirabilis (32,4 %), Proteus vulgaris (51,2 %) и Pseudomonas aeruginosa (55,5 %). Однако, на наш взгляд, это связано с тем, что данные микроорганизмы из–за ряда своих биологических свойств проявляют высокую устойчивость ко всем антибактериальным препаратам и бактериологическим фагам, которые получили широкое применение в медицинской практике в последние годы.
Чувствительность микроорганизмов к Биоспорину приведена в табл. 2.
Согласно табл. 2, Биоспорин обладает высокой литической активностью к бактериям рода Staphylococcus (S.aureus (69,3 %), S.epidermidis (88,4 %), S.haemolyticus (72,1 %), S.saprophyticus (87,9 %)). Чувствительность бактерий рода Enterobacteriacae (E.coli (81,2 %), E.aerogenes (71,5 %)) немного выше, чем чувствительность этих же бактерий к Субалину. Чувствительность грибов рода Сandida (44,3 %) и Pseudomonas aeruginosa (32,2 %) значительно ниже, чем к Субалину (75,4 и 55,5 % соответственно).
Следует отметить, что Субалин и Биоспорин проявляют высокую литическую активность даже к штаммам с высокой резистентностью к антибиотикам.
В табл. 3 приведена сравнительная характеристика чувствительности микроорганизмов к наиболее часто применяемым антибиотикам и антимикотикам, а также к исследуемым Субалину и Биоспорину.
Как видно из табл. 3, гатифлоксацин более активен, чем Субалин и Биоспорин, в отношении E.coli (88,1 %), Streptococcus spp. (73,3 %), E.aerogenes (78,9 %), однако в остальных случаях Субалин и Биоспорин показывают более высокую литическую активность. Следует отметить, что при этом Субалин и Биоспорин не оказывают токсического действия, свойственного гатифлоксацину.
При этом Субалин и Биоспорин, в отличие от антибактериальных препаратов, демонстрируют выраженное противогрибковое действие (рис. 1), что позволяет оказывать воздействие на патогенную и условно-патогенную флору, не используя дополнительно противогрибковые препараты. Это, в свою очередь, позволяет уменьшить токсическое воздействие вышеуказанных препаратов на организм.
По своему воздействию на грибы рода Сandida Биоспорин и Субалин выигрывают даже в сравнении с популярным в последние годы противогрибковым препаратом интраконазолом (рис. 2).
Интересным является также наблюдение эффективности широко применяемого на протяжении долгих лет антибиотика цефтриаксона в сравнении с исследуемыми препаратами. Как видно из табл. 3, Субалин и Биоспорин выигрывают по способности подавления УПФ.
Полученные данные позволяют утверждать, что препараты СЭА (Субалин и Биоспорин) демонстрируют выраженную антагонистическую активность по отношению к ряду патогенных и условно–патогенных микроорганизмов. При этом спектр ее отличается. Так, Субалин более активен в отношении стафило- и стрептококковой флоры. С учетом того факта, что именно эти возбудители чаще всего являются причиной возникновения заболеваний кожи, лор-органов, а также органов дыхания [12], можно говорить о хороших перспективах использования Субалина именно в этих направлениях.
Что касается Биоспорина, то максимальный эффект препарата был выявлен относительно Е.соli и E.aerogenes, которые занимают ведущее место среди причин возникновения бактериальных кишечных инфекций, а также заболеваний мочеполовой сферы [13].
Полученные в результате исследования данные позволяют сделать следующие выводы:
1. Субалин и Биоспорин демонстрируют высокую антагонистическую активность по отношению к представителям патогенной и условно-патогенной флоры.
2. По отношению к ряду возбудителей Субалин и Биоспорин демонстрируют сопоставимую и в ряде случаев более выраженную активность, чем традиционно применяемые антибактериальные и противогрибковые препараты.
3. Спектр антагонистической активности двух исследуемых препаратов отличается, что связано в первую очередь с различиями используемых штаммов микроорганизмов, а соответственно, и с оказываемыми этими препаратами эффектами. Выявленные отличия позволяют говорить о возможности дифференцированного использования Субалина и Биоспорина в терапии тех или иных заболеваний.
4. Разработанная нами методика произведения посевов для определения чувствительности различных представителей патогенной и условно-патогенной флоры к исследуемым препаратам имеет широкие перспективы внедрения в рутинную практику. Это дает возможность использовать вышеуказанные лекарственные средства в качестве альтернативы традиционным антибактериальным и противогрибковым препаратам либо в схемах комбинированной терапии. Это особенно актуально, учитывая имеющиеся в настоящий момент высокие показатели резистентности к различным антибактериальным и противогрибковым средствам, а также высокий профиль безопасности Субалина и Биоспорина.
1. Проблемы водоснабжения города Одессы // Качество воды и здоровье человека. Сборник научных статей. — 1999. — С. 203–204.
2. Похиленко В.Д., Перелыгин В.В. Пробиотики на основе спорообразующих бактерий и их безопасность // Химическая и биологическая безопасность. — 2007. — № 2–3. — С. 20–41.
3. Бакулина Л.Ф., Перминова Н.Г., Тимофеев И.В. и др. Пробиотики на основе спорообразующих микроорганизмов рода Bacillus и их использование в ветеринарии // Биотехнология. — 2001. — № 2. — С. 4–56.
4. Bergey’s manual of systematic bacteriology / Ed. P.H.A. Sneat, N.S. Mair, M.E. Sharpe, J.G. Holt. — Baltimore etc: Williams and Wilkins, 1984. — Vol. 2. — P. 1105–1139.
5. Reiling H.E., Zuber H. Energy production of Bacillus stearothermophilus by denitrification processes // Experimentia. — 1980. — Vol. 36, № 12. — P. 1457–1459.
6. Засыпка Л.И., Маляренко Л.А., Псахис И.Б., Иваница В.А. Микробиологическая оценка качества воды реки Днестр в течение 1999–2001 гг. // Вестник Одесского национального университета. — 2001. — Т. 6, № 4. — С. 116–119.
7. Псахис І. Б., Псахіс Б.Й., Іваниця В.О. Деклараційний патент на корисну модель № 13081 «Спосіб доочищення питної води від нітритів». — 2004.
8. Брусникина Н.Ф., Залесских Н.В., Быкова С.А., Власнеко М.А. Характеристика условно-патогенных микроорганизмов при острах и хронических заболеваниях кишечника // Республиканский сборник научных трудов / Под ред. И.Н. Блохиной, К.Л. Соколовой. — Горький: Мед. ин-т, 1988. — С. 41–43.
9. Визначення чутливості мікроорганізмів до антибактеріальних препаратів: Методичні вказівки Мв 9.9.5-143-2007 / МОЗ України. — К. — 2007. — 80 с.
10. Легеза К.Н., Чаплинский В.Я., Сорокулова И.Б., Якимова С.В., Грицаенко А.М. Применение Биоспорина при лечении кишечных инфекций // Современная педиатрия. — 2013. — № 5 (53). — С. 172–174.
11. Сорокулова И.Б., Рыбалко С.Л., Руденко А.А., Берестовая Т.Г., Легеза К.Н., Подгорский В.С., Курищук К.В. Субалин. Принципиально новый подход к лечению бактериальных и вирусных инфекций. — К., 2010.
12. Перцева Т.А., Бонцевич Р.А. Клиническое значение возбудителей инфекций дыхательных путей. Конспект врача клинициста и микробиолога // Клиническая иммунология. Аллергология. Инфектология. — 2006. — № 4.
13. Ильина Н.А., Карпеева Е.А., Гусева И.Т. // Современные наукоемкие технологии. — 2008. — № 9. — С. 60–62.

/136/136.jpg)
/137/137.jpg)
/137/137_2.jpg)