Журнал «Актуальная инфектология» 4 (5) 2014
Вернуться к номеру
Особенности общего реактивного потенциала организма у детей раннего возраста при БЦЖ-лимфаденитах
Авторы: Бобровицкая А.И., Голубова Т.Ф., Суходольская В.В., Захарова Л.А. — Донецкий национальный медицинский университет им. М. Горького; НИИ детской курортологии и физиотерапии, г. Евпатория
Рубрики: Акушерство и гинекология
Разделы: Клинические исследования
Версия для печати
Цель: интегральная оценка состояния здоровья детей раннего возраста с БЦЖ-индуцированными регионарными лимфаденитами.
Материал и методы. Работа выполнена на академической базе детских инфекционных отделений Донецкой области и Донецкого областного лабораторного центра Госсанэпидслужбы Украины. Сделан сравнительный анализ осложнений БЦЖ-вакцинаций в виде регионарных лимфаденитов за 3 года. Оценка иммунного статуса проводилась на основе комплексного изучения показателей общего реактивного потенциала организма путем изучения качественно-количественной характеристики гемограмм.
Результаты. В Донецкой области за 3 года вакцинировано БЦЖ-вакциной (Дания) 19 078 детей и БЦЖ-вакциной (Россия) — 14 328, из них у 210 детей развились осложнения: 143 (0,74 %) ребенка были привиты БЦЖ-вакциной (Дания) и 67 (0,36 %) — БЦЖ-вакциной (Россия). Клинические формы осложнений в некоторой степени определялись характером БЦЖ-вакцины. При использовании БЦЖ-вакцины (Дания) среди осложнений в виде лимфаденитов различной локализации в 2,2 раза чаще встречались инфильтративные формы, а также отмечалось наличие свищей (5,7 %) по сравнению с детьми, вакцинированными БЦЖ-вакциной (Россия). Помимо этого, в 3 раза чаще встречались очень редкие осложнения — 10 против 3,3 %. Это язва средней трети левого плеча; грудино-ключичное сочетание БЦЖ-ассоц., дест.+ МБТ(–), впервые диагностированный туберкулез (ВДТБ), вторичный туберкулез легких (ВТЛ); тубостит правого бедра; тубостит нижней трети правого бедра; тубостит 4/3 правой бедренной кости; тубостит левого коленного сустава при вакцинации БЦЖ-вакциной (Дания). При вакцинации БЦЖ-вакциной (Россия) наблюдались только ВДТБ, тубостит и ВДТБ, двойничный гонит, Д+, МБТ(+).
Особенности общего реактивного потенциала организма при БЦЖ-вакцинации определяются более выраженной степенью активности воспаления у детей раннего возраста, а также снижением способности организма отвечать на антигенный раздражитель и выраженным риском прорыва барьера на пути инфекции — возможностью генерализации инфекции у детей первого года жизни на фоне нормальной аллергической настроенности организма.
Выводы. При использовании БЦЖ-вакцины российского производства наблюдается менее выраженная перегрузка кровотока продуктами интоксикации и воспаления, более выраженная способность организма отвечать на антигенный раздражитель и отсутствие риска генерализации инфекции, особенно у детей первого года жизни, по сравнению с БЦЖ-вакциной датского производства. Для вакцинации новорожденных против туберкулеза целесообразно использовать более очищенную, с высокой иммуногенностью и наименее реактогенную БЦЖ-вакцину российского производства. Несмотря на наличие осложнений при использовании БЦЖ-вакцины, защита организма от развития генерализованных форм туберкулеза у детей раннего возраста возможна путем вакцинации в периоде новорожденности.
Мета: інтегральна оцінка стану здоров’я дітей раннього віку з БЦЖ-індукованими регіонарними лімфаденітами.
Матеріал і методи. Робота виконана на академічній базі дитячих інфекційних відділень Донецької області та Донецького обласного лабораторного центру Держсанепідслужби України. Зроблено порівняльний аналіз ускладнень БЦЖ-вакцинацій у вигляді регіонарних лімфаденітів за 3 роки. Оцінка імунного статусу проводилася на основі комплексного вивчення показників загального реактивного потенціалу організму шляхом вивчення якісно-кількісної характеристики гемограм.
Результати. У Донецькій області за 3 роки вакциновано БЦЖ-вакциною (Данія) 19 078 дітей і БЦЖ-вакциною (Росія) — 14 328, з них у 210 дітей розвинулися ускладнення: 143 (0,74 %) дитини були щеплені БЦЖ-вакциною (Данія) і 67 (0,36 %) — БЦЖ-вакциною (Росія). Клінічні форми ускладнень деякою мірою визначалися характером БЦЖ-вакцини. При використанні БЦЖ-вакцини (Данія) серед ускладнень у вигляді лімфаденітів різної локалізації в 2,2 раза частіше зустрічалися інфільтративні форми, а також зазначалася наявність свищів (5,7 %) порівняно з дітьми, вакцинованими БЦЖ-вакциною (Росія). Крім того, в 3 рази частіше зустрічалися дуже рідкісні ускладнення — 10 проти 3,3 %. Це виразка середньої третини лівого плеча; грудино-ключичне поєднання БЦЖ-асоц., дест.+ МБТ (–), вперше діагностований туберкульоз (ВДТБ), вторинний туберкульоз легенів (ВТЛ); тубостит правого стегна; тубостит нижньої третини правого стегна; тубостит 4/3 правої стегнової кістки; тубостит лівого колінного суглоба при вакцинації БЦЖ-вакциною (Данія). При вакцинації БЦЖ-вакциною (Росія) спостерігалися тільки ВДТБ, тубостит і ВДТБ, двойнічний гоніт, Д+, МБТ(+). Особливості загального реактивного потенціалу організму при БЦЖ-вакцинації характеризуються більш вираженим ступенем активності запалення в дітей раннього віку, а також зниженням здатності організму відповідати на антигенний подразник і вираженим ризиком прориву бар’єру на шляху інфекції — можливістю генералізації інфекції в дітей першого року життя на тлі нормальної алергічної налаштованості організму.
Висновки. При використанні БЦЖ-вакцини російського виробництва спостерігається менш виражене перевантаження кровотоку продуктами інтоксикації та запалення, більш виражена здатність організму відповідати на антигенний подразник і відсутність ризику генералізації інфекції, особливо в дітей першого року життя, порівняно з БЦЖ-вакциною данського виробництва. Для вакцинації новонароджених проти туберкульозу доцільно використовувати більш очищену, з високою iмуногеннiстю і найменшою реактогенністю БЦЖ-вакцину російського виробництва. Незважаючи на наявність ускладнень при використанні БЦЖ-вакцини, захист організму від розвитку генералізованих форм туберкульозу в дітей раннього віку можливий шляхом вакцинації в періоді новонародженості.
Objective: integrated health assessment of infants with BCG-induced regional lymphadenitis.
Material and Methods. The work was carried out on the academic basis of pediatric infectious departments of Donetsk region and Donetsk regional laboratory center of State sanitary and epidemiological service of Ukraine. Comparative analysis of complications of BCG vaccinations in the form of regional lymphadenitis for 3 years is carried out. Evaluation of immune status was based on a comprehensive study of indicators of general reactive potential of the organism by studying the qualitative-quantitative characteristics of hemogram.
Results. In Donetsk region for 3 years 19,078 children were vaccinated with BCG vaccine (Denmark) and 14,328 — with BCG vaccine (Russia), of whom 210 children developed complications: 143 (0.74 %) children were vaccinated with BCG vaccine (Denmark) and 67 (0.36 %) — with Russian BCG vaccine. Clinical forms of complications to some extent were determined by the nature of the BCG vaccine. When using the BCG vaccine (Denmark), infiltrative forms were 2.2 times more common among the complications in the form of lymphadenitis of various localization, and the presence of a fistula (5.7 %) were detected compared with children vaccinated with BCG vaccine (Russia). In addition, very rare complications were 3 times more frequent — 10 versus 3.3 %. They are: plague is the middle third of the left shoulder; sternoclavicular combination of BCG assoc., dest.+ MBT(–), newly diagnosed tuberculosis (NDT), secondary pulmonary tuberculosis; tuberculous osteitis of the right hip; tuberculous osteitis of the lower third of the right hip; tuberculous osteitis of the 4/3 of the right femur; tuberculous osteitis of the left knee joint with BCG vaccine (Denmark). When BCG vaccine (Russia) was used, we detected only NDT, tuberculous osteitis and NDT, onitis, D+, MBT(+). Features of general reactive potential of the organism at BCG vaccination are determined by more significant degree of inflammatory activity in young children, as well as by a decrease in the body’s ability to respond to antigenic stimulus and a pronounced risk of breaking a barrier to infection — the possibility of generalization of infection in infants on the background of normal allergic disposition of the body.
Conclusions. When using BCG vaccine of Russian production, there is far less significant overload of blood flow by products of intoxication and inflammation, more pronounced body’s ability to respond to antigenic stimulus generalization and no risk of infection, especially in infants, compared with Danish BCG vaccine. For vaccination of infants against tuberculosis, it is advisable to use more refined, with high immunogenicity and less reactogenic BCG vaccine of Russian production. Despite the presence of complications when using BCG vaccine, protection of the body from the development of generalized forms of tuberculosis in young children is possible by vaccination in the neonatal period.
Статья опубликована на с. 59-63
Одной из актуальных проблем в настоящее время является заболеваемость туберкулезом. Украина вместе со странами СНГ относится к территориям с высоким уровнем заболеваемости туберкулезом — более 30 случаев на 100 тыс. населения. Особенно неблагоприятная ситуация по туберкулезу в юго-восточном регионе Украины. За период 2005–2011 гг. заболеваемость различными формами туберкулеза колебалась в пределах 84,1 случая на 100 тыс. населения (2005 г.) против 67,2 (2011 г.). Заболеваемость туберкулезом детей в возрасте 0 мес. — 14 лет включительно составила 9,3–8,0 (2011 г.) случая на 100 тыс. детского населения, смертность — 25,3–16,6, а годовой риск инфицирования туберкулезом детей оценивается в 0,5–2,0 % (Фещенко Ю.И., 2012). Анализ случаев неблагоприятных исходов при туберкулезе у детей Донецкой области позволил определить, что среди умерших 80 % составили непривитые дети (Беломеря Т.А., Коломойцева А.Н., Кириллова Т.А., 2011).
Ведущим и обязательным профилактическим мероприятием по контролю над туберкулезом в Украине признана первичная профилактика в виде БЦЖ-вакцинации, которая не предотвращает первичное инфицирование и реактивацию латентной легочной инфекции — основного источника бациллярного распространения туберкулеза среди населения. Однако она единственный существующий в настоящее время препарат, который используется для иммунизации детей против туберкулеза и обеспечивает защиту от туберкулезного менингита (64 %), диссеминированной формы туберкулеза (78 %), летальных исходов (65 %) у детей раннего возраста (Митинская Л.А., 2001; WHO, 2010).
В настоящее время БЦЖ-вакцинацией охвачено около 100 млн детей. Эффективность вакцины БЦЖ доказана длительностью ее использования в практическом здравоохранении — более 90 лет — и способностью предотвращать генерализацию инфекции путем развития локального специфического процесса, безопасного для здоровья детей. Однако вакцина БЦЖ — живая культура. Поэтому она может быть причиной развития осложнений. Большинство осложнений после БЦЖ-вакцинации проявляются поражением регионарных лимфатических узлов (подмышечных, надключичных, подключичных, шейных) с развитием специфического воспаления, характеризующегося наличием казеозного некроза. В ответ на БЦЖ-вакцинацию возможно развитие нежелательных тяжелых реакций, зачастую системного характера, связанных с генерализацией инфекции: БЦЖ-остеомие-лит, генерализованная лимфаденопатия, диссеминированная БЦЖ-инфекция, туберкулезная волчанка, частота которых колеблется от 0,004 до 2,5 % случаев.
В Украине частота осложнений БЦЖ-вакцинации за последние годы увеличилась в 10–100 раз по сравнению с частотой во время предыдущей эпидемии (1946–1990 гг.) и составила в отдельных регионах 1,5–2,0 %. Однако риск развития подобных осложнений значительно меньше по сравнению с риском заболевания туберкулезом невакцинированных детей.
Среди многочисленных причин непредвиденных реакций детского организма на БЦЖ-вакцинацию и развития серьезных осложнений основными являются: эпидемиологические — неконтролируемая группа детей, рожденных от ВИЧ-положительных матерей и снятых с учета по достижении 18 месяцев; снижение селективного давления контагиозных инфекционных болезней на человека; генетические — отсутствие скрининга процесса полиморфизации генов и накопление генных (точечных) мутаций; игнорирование в детском организме иммунологических феноменов — антигенного импритинга и антителозависимого усиления инфекции.
При развитии осложнений БЦЖ-вакцинации важную роль играет состояние иммунной системы у детей. Скрытые изменения иммунного статуса у детей раннего возраста клинически могут ничем не проявляться. Поэтому такие дети не имеют противопоказаний к БЦЖ-вакцинации.
Таким образом, вышеизложенное требует нового подхода (дифференцированного) к БЦЖ-вакцинации детей раннего возраста.
Целью работы явилась интегральная оценка состояния здоровья детей раннего возраста с БЦЖ-индуцированными регионарными лимфаденитами.
Материалы и методы
Под наблюдением находилось 210 детей раннего возраста, имеющих осложнения БЦЖ-вакцинации в виде регионарных лимфаденитов. Среди них городских детей было 185 (88,1 %), сельских — 25 (11,9 %). Половой состав вакцинированных новорожденных, имеющих осложнения, характеризовался наличием детей мужского пола — 53,1 % и женского — 46,9 %. При отягощенной беременности и от патологических родов родилось 19,4 % новорожденных. Доношенные дети составили 95,3 %, недоношенные — 4,7 %. Фоновые заболевания выявлены у 52,3 % детей: последствия кесарева сечения (13,2 %), ОРВИ (9,6 %), анемия (8,5 %), атопический дерматит (14,2 %), перинатальное поражение ЦНС (19,2 %), недоношенность I степени и тимомегалия (по 5,9 %), гнойно-воспалительные заболевания и внутриутробные инфекции (ВУИ) (по 6,1 %), кефалогематома (2,5 %), гемолитическая болезнь (3,1 %), геморрагическая болезнь (1,5 %), врожденный порок сердца (1,7 %).
Оценка иммунного статуса проводилась на основе комплексного изучения показателей общего реактивного потенциала организма путем изучения качественно-количественной характеристики гемограмм по методике Н.П. Мель (1990). Изучали нагрузочно-эритроцитарный коэффициент (НЭК), клеточно-фагоцитарный потенциал (КФП), иммуно-лимфоцитарный потенциал (ИЛП), а также аллергическую настроенность организма (АНО).
Нагрузочно-эритроцитарный коэффициент — относительный показатель, позволяющий судить о напряженности эритропоэза, уровне гемоглобина и опосредованно — о кислородной обеспеченности организма, а также об элиминации углекислого газа и глубине воспалительного процесса. Выведение коэффициента и учет НЭК базируются на предположении, что при метаболических нарушениях, связанных с перегрузкой кровотока продуктами интоксикации, воспаления, адсорбцией их на эритроцитах и утяжелением, гемоглобин будет хуже справляться со своими адсорбционно-транспортными функциями. При благоприятных условиях НЭК невелик, а при неблагоприятных — высок за счет роста СОЭ и/или падения уровня гемоглобина. Высокие показатели НЭК позволяют судить о степени активности инфекционно-воспалительного процесса и необходимости противовоспалительной терапии.
Клеточно-фагоцитарный потенциал обеспечивается кооперирующим взаимодействием клеток крови, обладающих фагоцитарной функцией. Из числа клеточных элементов белой крови фагоцитарной активностью обладают палочкоядерные и сегментоядерные нейтрофилы и моноциты. Она зависит от их удельного веса в общей массе лейкоцитов. Оценка условного коэффициента проводилась по принципу: чем меньше оказывается КФП, тем больше выражен риск прорыва этого барьера на пути инфекции.
Иммунно-лимфоцитарный потенциал. Большую роль в обеспечении специфического иммунного ответа на внедрение возбудителя инфекционного заболевания играют лимфоциты. Определение их количества и отношение удельного веса к общей массе лейкоцитов может помочь в определении способности организма отвечать на антигенное раздражение.
Аллергическая настроенность организма. Количество эозинофилов — один из показателей иммунограммы, наиболее чувствительный к наличию воспалительного процесса в организме. Сразу после внедрения инфекции содержание в кровотоке эозинофилов, как правило, резко сокращается, практически до полного исчезновения. В начале выздоровления, перед кризом, число эозинофилов повышается до значений, существенно превышающих норму, и сохраняется даже в периоде ремиссии заболевания. В формировании аллергии принимают участие многие клеточные элементы, наиболее постоянно — эозинофилы, базофилы, нейтрофилы. В процессе сенсибилизации и реализации аллергических реакций, определяющих общую аллергическую настроенность организма, их состояние отражает абсолютное количество и удельный вес в общей массе лейкоцитов.
Обсуждение и результаты
В Донецкой области в течение 3 лет вакцинировано БЦЖ производства Дании 19 078 детей и производства России — 14 328, из них осложнения развились у 210 детей: 143 (0,74 %) ребенка были привиты БЦЖ-вакциной Дании и 67 (0,36 %) — БЦЖ-вакциной России. В условиях родильного отделения городских и районных больниц вакцинированы на 3–5-й день жизни 192 (91,4 %) новорожденных, позже 7-го дня жизни — 12 (5,7 %), из них по 1 ребенку на 17-й день жизни, 48-й, спустя 3, 4 и 9 месяцев, 2 г. 1 мес. жизни. Пролонгация вакцинации у 18 детей определялась перинатальным поражением ЦНС (12), морфофункциональной незрелостью (4), недоношенностью 4-й степени (2). Интервал развития осложнений от момента вакцинации БЦЖ в среднем составил 160,66 ± 36,80 дня. Однако при использовании БЦЖ-вакцины (Россия) он был более длительным и составил в среднем 219,83 ± 56,30 дня против 131,11 ± 45,20 дня для БЦЖ-вакцины (Дания), что свидетельствует об участии других факторов, а возможно, о менее выраженной иммуногенности БЦЖ-вакцины (Россия). Осложнения, как правило, развивались в первом полугодии жизни у 72,6 % детей, во втором — у 19,6 %, позже — у 7,8 %.
Клинические формы осложнений в некоторой степени определялись характером БЦЖ-вакцины. При использовании БЦЖ-вакцины (Дания) среди осложнений в виде лимфаденитов различной локализации в 2,2 раза чаще встречались инфильтративные формы, а также отмечалось наличие свищей (5,7 %) по сравнению с детьми, вакцинированными БЦЖ-вакциной (Россия). Помимо этого, у детей, вакцинированных БЦЖ-вакциной (Дания) в 3 раза чаще встречались и очень редкие осложнения по сравнению с детьми, вакцинированными БЦЖ-вакциной (Россия) — 10 % случаев против 3,3 %. Это язва средней трети левого плеча; грудино-ключичное сочетание БЦЖ-ассоц., дестр.+, МБТ(–), ВДТБ, ВТЛ; тубостит правого бедра; тубостит нижней трети правого бедра; тубостит 4/3 правой бедренной кости; тубгонит левого коленного сустава при вакцинации БЦЖ-вакциной (Дания). При вакцинации БЦЖ-вакциной (Россия) только ВДТБ, тубостит и ВДТБ, двойничный гонит, Д+, МБТ(+).
После развития осложнения обращаемость за медицинской помощью была хуже у детей, вакцинированных БЦЖ-вакциной российского производства, по сравнению с детьми, вакцинированными БЦЖ-вакциной (Дания) — через 27,5 ± 2,5 дня против 10,3 ± 2,7. Значительно более поздняя обращаемость выявлена только у 3 детей, вакцинированных БЦЖ-вакциной (Россия), — на 185-й день, 362-й и 128-й от начала вакцинации. Данные дети имели фоновые заболевания в виде атопического дерматита, перинатального поражения ЦНС, синдрома нейрорефлекторной возбудимости и ВУИ в сочетании с атопическим дерматитом.
Особенности общего реактивного потенциала организма детей в зависимости от возраста и БЦЖ-вакцины различных стран представлены в табл. 1 и 2.
Согласно данным табл. 1 и 2, у детей первого года жизни НЭК превышал физиологический уровень на 38 и 30 %; КФП — на 24,4 и 29,9 %; ИЛП — на 11,3 и 16,2 %. У детей второго и третьего года жизни НЭК сохранялся в физиологических пределах; КФП превышал физиологический уровень на 39,4 и 60,6 %; ИЛП — на 22,6 и 38,8 %. Независимо от возраста АНО сохранялось на физиологическом уровне статистически достоверно (р < 0,5). Это свидетельствует о более выраженной перегрузке кровотока продуктами интоксикации и воспаления у детей раннего возраста, особенно при вакцинации БЦЖ (Дания). Повышение КФП и ИЛП при вакцинации БЦЖ (Россия) отражает более выраженную способность организма отвечать на антигенный раздражитель и уменьшение риска генерализации инфекции, особенно у детей первого года жизни, при сохранении аллергической настроенности организма на физиологическом уровне.
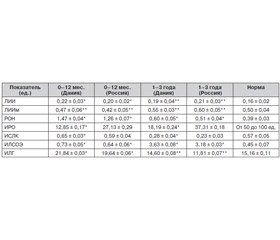
Для контроля течения осложнений БЦЖ-вакцинации, появления неспецифических осложнений и эффективости проводимого лечения у детей раннего возраста определяли ряд индексов на основании расширенного общего анализа крови (табл. 3).
Согласно табл. 3, у детей первого года жизни по сравнению с физиологическим уровнем увеличены: ЛИИ — в 1,3 раза (Дания) и 1,2 (Россия); РОН — в 3,9 и 3,02; ИЛСОЭ — в 1,6 и 1,4; ИЛГ — в 1,4 и 1,3 раза соответственно. У детей 2-го и 3-го года жизни РОН увеличен в 1,5 и 1,4 раза; ИЛСОЭ — в 8,0 и 7,0; ИСКЛ отсутствует (р < 0,05). Сохраняются на физиологическом уровне у детей раннего возраста показатели ЛИИм, ИРО и ИЛГ. Данные индексы у детей раннего возраста при БЦЖ-индуцированных регионарных лимфаденитах, в частности ЛИИм, отражают отсутствие тканевой деградации; РОН указывает на декомпенсирование эндогенной интоксикации. Однако ИРО свидетельствует о возможности развития осложнений; ИСКЛ — об активном воспалительном процессе и нарушении иммунологической реактивности организма. ИЛСОЭ позволяет утверждать, что интоксикация связана с инфекционным процессом. На основании ИЛГ можно предположить, что воспалительный процесс имеет асептический характер у детей первого года жизни (р < 0,05).
Выводы
1. При использовании БЦЖ-вакцины российского производства наблюдается менее выраженная перегрузка кровотока продуктами интоксикации и воспаления, более выраженная способность организма отвечать на антигенный раздражитель и отсутствие риска генерализации инфекции, особенно у детей первого года жизни, по сравнению с БЦЖ-вакциной датского производства.
2. Для вакцинации новорожденных против туберкулеза целесообразно использовать более очищенную, с высокой иммуногенностью и наименее реактогенную БЦЖ-вакцину российского производства.
3. Несмотря на наличие осложнений при использовании БЦЖ-вакцины, защита организма от развития генерализованных форм туберкулеза у детей раннего возраста возможна путем вакцинации в периоде новорожденности.
1. Костроміна В.П. БЦЖ-вакцинація у дітей та можливі ускладнення // Здоров’я України. — 2008. № 4 (1). — С. 54–55.
2. Чернишова Л.І. Імунопрофілактика: сучасні досягнення та проблеми // Перинатология и педиатрия. — 2007. — № 3 (31). — С. 7–11.
3. WHO Vaccine — Preventable Diseases: Vonitoring System 2001 Global Summary. — Geneva: WHO, 2001. — 330 p.
4. Vaccine and Biologicals Annual Report. — Geneva, 2000. — 215 p.

/62/62.jpg)