Журнал «Здоровье ребенка» 1 (60) 2015
Вернуться к номеру
Гастроінтестинальна форма харчової алергії у дітей — актуальна проблема сучасності
Авторы: Охотнікова О.М. — Національна медична академія післядипломної освіти імені П.Л. Шупика; Гладуш Ю.І., Бондаренко Л.В. — Національна дитяча спеціалізована лікарня «ОХМАТДИТ», м. Київ;
Мелліна К.В., Федушка Г.М., Підвишенна Т.В., Боровик Ю.Р. — Національна медична академія післядипломної освіти імені П.Л. Шупика; Українська Т.Л., Підгірна Н.В., Шестакова О.С., Зарудна О.Ф., Грищенко О.М. — Національна дитяча спеціалізована лікарня «ОХМАТДИТ», м. Київ
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Мета: визначення особливостей гастроінтестинальної алергії у дітей з алергічною і соматичною патологією.
Пацієнти і методи. Обстежено 106 дітей: основна група — 60 пацієнтів з алергією, група порівняння — 46 дітей суто з патологією органів травлення. Проведено клінічні, лабораторні (загальний імуноглобулін Е) та ендоскопічні й морфологічні дослідження.
Результати. Причиною харчової алергії частіше були білки коров’ячого молока, цитрусові, шоколад, полуниці. Шлунково-кишкові симптоми при алергії проявлялись больовим і диспептичним синдромами (нудота, печія), порушенням випорожнення. У 28 % хворих абдоміналгія була відсутня. Еозинофілія крові виявлена у 61,7 % дітей. Ендоскопічно рухова функція характеризувалась порушенням моторики шлунка, стравоходу або дванадцятипалої кишки, переважно рефлюксами. Незмикання кардії було діагностично значущим (χ2(1) = 14,095, φ = 0,374) для харчової алергії. Візуальні особливості слизової оболонки (лімфоїдна гіперплазія, наліт за типом «манної крупи») верхніх відділів травного тракту не мали значущого зв’язку у хворих основної і порівнюваної груп (χ2 не вище критичного значення). Відзначались випадки поєднання бронхіальної астми, алергічного риніту і харчової алергії з нормальним рівнем IgE, що зумовлено не-IgE-залежними реакціями.
Висновки. Ендоскопічне й морфологічне дослідження варто застосовувати в диференціальній діагностиці алергічних і неалергічних уражень слизової оболонки травного тракту.
Цель: определение особенностей гастроинтестинальной аллергии у детей с аллергической и соматической патологией.
Пациенты и методы. Обследовано 106 детей: основная группа — 60 пациентов с аллергией, группа сравнения — 46 детей только с патологией пищеварительного тракта. Проведены клинические, лабораторные (общий иммуноглобулин Е), эндоскопическое и морфологическое исследования.
Результаты. Причиной пищевой аллергии чаще были белки коровьего молока, цитрусовые, шоколад, клубника. Желудочно-кишечные симптомы при аллергии проявлялись болевым и диспептическим синдромами (тошнота, изжога), нарушениями стула. У 28 % больных абдоминалгия отсутствовала. Эозинофилия крови выявлена у 61,7 % детей. Эндоскопически двигательная функция характеризовалась нарушением моторики желудка, пищевода или двенадцатиперстной кишки, преимущественно рефлюксами. Несмыкание кардии было диагностически значимым (χ2(1) = 14,095, φ = 0,374) для пищевой аллергии. Визуальные особенности слизистой (лимфоидная гиперплазия, налет типа «манной крупы») верхних отделов пищеварительного тракта не имели значимой связи у больных основной и сравниваемой групп (χ2 не выше критического значения). Отмечались случаи сочетания бронхиальной астмы, аллергического ринита и пищевой аллергии с нормальным уровнем IgE, что обусловлено не-IgE-зависимыми реакциями.
Выводы. Эндоскопическое и морфологическое исследование следует использовать в дифференциальной диагностике аллергических и неаллергических поражений слизистой оболочки пищеварительного тракта.
Objective: to determine the characteristics of gastrointestinal allergy in children with allergic and somatic pathology.
Patients and Methods. 106 children were examined: study group — 60 patients with an allergy, comparison group — 46 children with digestive diseases alone. Clinical, laboratory (total immunoglobulin E) and endoscopic morphological methods were used.
Results. Cow’s milk proteins, citrus fruits, chocolate, strawberry were the most frequent causes of food allergies. Gastrointestinal symptoms in allergy manifested by pain and dyspeptic syndrome (nausea, heartburn), altered bowel elimination. 28 % of patients hadn’t abdominalgia. Blood eosinophilia has been detected in 61.7 % of children. Endoscopically, motor function was characterized by dysmotility of the stomach, esophagus or duodenum, in most cases by refluxes. Incompetence of cardia was diagnostically significant (χ2(1) = 14.095, φ = 0.374) in food allergies. Visual features of the mucous membrane (lymphoid hyperplasia, multiple small white patches) of the upper gastrointestinal tract had no significant correlation in patients from study and comparison groups (χ2 not higher than the critical value). Cases of the combination of bronchial asthma, allergic rhinitis and food allergy with normal IgE level were detected, which is caused by not-IgE-dependent reactions.
Conclusions. Endoscopic and morphological study should be applied in the differential diagnosis of allergic and non-allergic lesions of the mucous membrane of the alimentary canal.
гастроінтестинальна алергія, ендоскопія, біопсія, імуноглобулін Е.
гастроинтестинальная аллергия, эндоскопия, биопсия, иммуноглобулин Е.
gastrointestinal allergy, endoscopy, biopsy, immunoglobulin E.
Статья опубликована на с. 29-35
Вступ
У наш час винятково актуальними постають питання діагностики різноманітних клінічних проявів, що розвиваються на харчові продукти, причому переважно в дитячому віці [6, 9]. Харчова алергія (ХА) — це небажана реакція на їжу з доведеним iмуноопосередкованим механізмом за рахунок як IgE-залежних, так і IgE-незалежних реакцій та їх комбінації [3, 4, 13], що клінічно проявляється шкірним, респіраторним і гастроінтестинальним синдромами [12]. Її важлива клінічна особливість — рецидивний, затяжний і хронічний перебіг, що створює загрозу для швидкої еволюції алергічного «маршу» [10, 11]. Поширеність ХА у дітей коливається в межах 6–8 % [4, 6, 14–16], проте справжня її частота залишається невідомою, оскільки в наш час вивчені лише найуживанiші харчові продукти [5]. Погіршення якості життя хворого, тісний зв’язок із хронічними хворобами шлунково-кишкового тракту (ШКТ), ензимопатiями, іншими алергічними та соматичними хворобами, а також розмаїття харчових алергенів і варiантiв алергічної відповіді роблять проблему ХА дуже актуальною [11].
Генетичнi фактори відіграють важливу роль у схильності до розвитку алергічних хвороб у людини, у тому числі i до ХА. Можливо, саме через дефект в алерген-специфiчнiй клiтиннiй відповіді не розвивається толерантнiсть до їжі у дітей, які це успадкували [15]. Наявність атопічного дерматиту, бронхіальної астми чи алергічного риніту в родичів є суттєвим фактором ризику розвитку цих захворювань.
Етіологічно значущими алергенами харчових продуктів є білки, що здатні викликати у генетично схильних дітей складну активацію Th2-хелперів і продукцію специфічних IgE-антитіл чи проникати через бар’єр травного каналу і вступати в контакт з імунними клітинами органів і тканин [1]. Найпоширенiшими харчовими алергенами у дітей є коров’яче молоко, курячі яйця, риба i продукти моря, м’ясо (особливо холодної обробки) [6–8, 18–20].
Важливим залишається питання взаємозв’язку харчової алергії та атопічного дерматиту. Провiдна роль у механізмах виникнення харчової алергії належить порушенню морфофункцiонального стану органів травлення [3, 6, 9]. Діти з функціональними порушеннями кишечника схильні до розвитку харчової алергії, оскільки шлунково-кишковий тракт має свою імунну систему, яка містить 80 % В-клітин. Разом із тим шкіра теж є імунним органом, у якому ініціація імунної відповіді здійснюється в асоційованій зі шкірою лімфоїдній тканині. Нормальна перистальтика сприяє елімінації мікроорганізмів та алергенів, зменшуючи можливість їх адгезії на епітелій. Розвитку алергічної реакцiї значно сприяє велика поверхня слизової оболонки травного каналу, її постiйний безпосереднiй контакт з алергеном i фонова гастроентерологiчна патологiя, що полегшує антигенну пенетрацiю кишкового епiтелiю [4, 6, 8, 12]. Кишкова мікробіота бере участь в імунному дозріванні організму дитини, що веде до Th2-поляризованої алергічної відповіді й підвищення продукції інтерлейкінів IL-4, IL-5, IL-13 і алерген-специфічних IgE-антитіл. Водночас імунне запалення з еозинофільною інфільтрацією тканин призводить до стійкого порушення кількісного й видового складу мікробіоти.
Гастроiнтестинальнi симптоми харчової алергії в дітей грудного віку (диспептичні явища, кишкові кольки) виникають у період введення прикорму [2, 9, 12]. У вiцi понад 6 років більше ніж у половини дітей вже діагностуються хронічні захворювання органів травлення [2], зв’язок розвитку яких із харчовою алергією залишається нерозпізнаним.
Метою дослідження було поліпшення ефективностi ранньої дiагностики гастроiнтестинальної харчової алергії у дітей різного вiку.
Матеріали та методи дослідження
Обстежено 60 дiтей вiком вiд 1,5 до 17 рокiв на базi Національної дитячої спеціалізованої лікарні «ОХМАТДИТ», із них 25 дiвчаток і 35 хлопчикiв (основна група). До дослідження залучено дітей зі скаргами з боку ШКТ та алергiчними хворобами, такими як бронхiальна астма, алергiчний ринiт, атопiчний дерматит, харчова алергiя. Групу порівняння становили 46 дiтей із патологією ШКТ (гастродуоденiт, виразкова хвороба, дискінезія жовчовивідних шляхів) без алергічних проявів.
Методи дослідження: збiр детального анамнезу хвороби й життя, загальний аналiз кровi і сечі, бiохiмiчний аналiз кровi, фіброезофагогастродуоденоскопія (ФЕГДС), бioпсiя слизової оболонки, pH-метрiя шлункового соку, визначення загального IgE в сироватцi кровi, ультразвукове дослідження органів черевної порожнини. До включення дітей у дослідження була отримана письмова поінформована згода батьків обстежених дітей.
Результати дослідження та їх аналіз
За даними сімейного анамнезу (рис. 1), у родичів дітей основної групи переважали алергiчнi захворювання (30 проти 2,2 % у дітей без алергічної патології), а в родичів дітей групи порівняння — захворювання ШКТ (24 проти 5 % у дітей із ХА). У батьків дітей з алергiєю відзначено більш високу частоту супутньої патології з перевагою алергiчних хвороб: алергічний риніт — 32,5 ± 12,0 %, бронхіальна астма — 47,5 ± 13,0 %, атопічний дерматит — 45 ± 13 %, ангіонабряк (набряк Квінке) — 10,0 ± 7,7 %, кропив’янка — 15,0 ± 9,2 %, медикаментозна алергія — 7,5 ± 6,8 %. Отже, сімейний анамнез дає вагому підставу для підозри на спадкову схильність алергічної патології ШКТ у хворих з алергічною патологією.
На підставі вивчення харчового анамнезу обстежених дітей, що наведено на рис. 2, найчастіше ХА спричиняють білки коров’ячого молока, цитрусові, шоколад і полуниці, горіхи та ін.
/31/31.jpg)
Що стосується клінічних проявів, перш за все скарг з боку ШКТ, то, як свідчать дані табл. 1, вони були однаковими в дітей обох порівнюваних груп, варто лише вiдмітити, що на неприємний запах із рота, вiдрижку повiтрям, печiю, а також астено-невротичні проблеми (головний бiль, швидку втомлюваність) скаржились дiти старшого вiку (пiсля 10 рокiв).
Аналогiчна ситуацiя спостерігалась i при аналiзi даних об’єктивного обстеження. У хворих обох груп при пальпацiї живота виявлялась болючість різного ступеня в епiгастрiї, точці Кера, зоні Шоффара, навколопупковiй дiлянцi, пiлородуоденальнiй зоні, по ходу кишечника, позитивний симптом Ортнера. Біль у животі був відсутній у 17 обстежених дітей основної групи. Здуття живота різного ступеня вираженості відзначалось у 8,3 % дітей, та помірне збільшення печінки спостерігалось у 13,3 ± 8,7 % обстежених цієї ж групи. З цього можна зробити висновок, що, з одного боку, гастроiнтестинальнi скарги та симптоми не є специфiчними для ХА, а з iншого — за наявностi таких скарг у дитини треба мати на увазi можливiсть розвитку гастроiнтестинальної алергії.
Прояви алергiї на шкiрi мали різний ступінь вираженості — сухість, тріщини, розчухи, лущення, гіперемія, папульозний та плямисто-папульозний висип, кірочки, еритематозно-сквамозні елементи та вогнища інфікування. Найчастіше відзначалась локалізація висипу по всьому тілу — у 18 (30 %) дітей, у ділянках обличчя, навколо рота — у 10 (16,7 %), кистей — у 8 (13,3 %), стоп, гомілок, стегон — у 10 (16,7 %).
Шлунково-кишковi розлади при гастроiнтестинальнiй алергії були представлені больовим синдромом та диспептичними проявами. Окрім того, спостерігалися також астеновегетативні розлади.
При пальпацiї живота виявлялась різного ступеня болючість в епiгастрiї (35 %), точці Кера (31,6 %), зоні Шоффара (5 %), навколопупковiй дiлянцi (10 %), пiлородуоденальнiй зоні (20 %), по ходу кишечника (3,3 %), позитивний симптом Ортнера (6,7 %). Абдоміналгія була відсутня у 17 (28 %) дітей. Здуття живота рiзного ступеня вираженостi вiдзначалось у 8,3 % дiтей. Помiрне збільшення печінки спостерігалось у 13,3 ± 8,7 % обстежених.
Випорожнення у дітей із гастроінтестинальною алергією характеризувалися різними проявами: у 76,7 ± 10,9 % хворих вони були оформленими й регулярними (1–3 рази на день), схильність до запорів спостерігалась у 18,3 % обстежених, а схильність до діареї — у 5 % дітей.
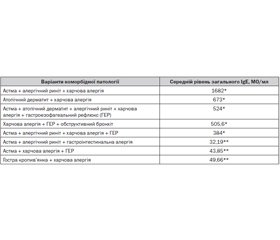
У 61,7 % дітей кількість еозинофілів дорівнювала 4,6 ± 0,6 %, а у 40,5 % була понад 5 %. Рівень загального сироваткового IgE у хворих на поєднану алергічну патологію наведено в табл. 2, дані якої демонструють високий ступінь сенсибілізації дітей із коморбідністю ХА та інших алергічних захворювань.
У дітей основної групи частiше виявлялось пiдвищення рiвня еозинофiлiв периферичної крові та загального сироваткового IgE. При цьому рівні IgE не залежали від тяжкості стану дитини чи кількості наявних у неї алергічних захворювань (табл. 3).
Спостерігалися варіанти поєднання ХА, бронхіальної астми та алергічного риніту, при яких рівень IgE залишався в межах вікових нормативів, натомість при легкій формі АД та ХА рівень IgE був у декілька разів вищий за норму. Це підтверджує той факт, що в розвитку алергічного процесу беруть участь найрізноманітніші механізми, не обов’язково із залученням IgE (табл. 2 і 3). Отже, можна зробити висновок про важливiсть визначення специфiчних IgE до конкретних харчових продуктiв, проте це дослiдження не можна вважати єдиним способом підтвердження діагнозу гастроiнтестинальної харчової алергії.
Особливості моторної функції шлунка за даними ФЕГДС в обстежених пацієнтів наведено в табл. 4, з якої видно, що майже всі діти, хворі на гастроінтестинальну алергію, мали проблеми з порушенням моторної функції шлунка, стравоходу або дванадцятипалої кишки, причому переважно за рахунок рефлюксів.
При порівнянні порушення моторики ШКТ у дiтей з алергiєю та з патологією ШКТ було виявлено, що незмикання кардiї у виглядi гастроезофагеального рефлюксу (ГЕР) має значення для дiагностики алергiчної патологiї ШКТ (а2(1) = 14,095, ф = 0,374, що свідчить про середню силу зв’язку).
Вiзуальнi особливостi слизової оболонки верхнього відділу ШКТ у дiтей із проявами ХА і хворобами ШКТ, що виявлялись під час ФЕГДС, були різноманітними. У стравоході слизова оболонка стравоходу характеризувалась рожевим, блідо-рожевим кольором або гіперемією в нижній третині, по всій площі чи вогнищевою гіперемією; відзначались ерозії або наліт у нижній його третині. Слизова оболонка шлунка була блідою, рожевою, гіперемованою, субатрофічною, з елементами лімфоїдної гіперплазії, білуватими утвореннями за типом «манної крупи». У дванадцятипалій кишці спостерігалися рожевий чи червоний колір слизової оболонки, без нальотів та вогнищ деструкції, а також із наявністю слизуватих або фібринових нальотів за типом «манної крупи», з елементами лімфоїдної гіперплазії і вираженим набряком чи атрофією слизової оболонки. При порівнянні візуальних змін слизової оболонки за кольором, наявністю лімфоїдних елементів, нальоту за типом «манної крупи» стравоходу, шлунка чи дванадцятипалої кишки не виявлено статистично значущих взаємозв’язків між хворими на алергічну патологію і дітьми з хворобами ШКТ (величина χ2 не перевищувала критичного значення). Отже, візуальна оцінка верхніх відділів ШКТ за допомогою ФЕГДС не дає можливості чітко підтвердити алергічний характер патологічних змін.
Особливий інтерес становили результати морфологічного дослідження біоптатів слизової оболонки верхніх відділів травного каналу (табл. 5).
Як видно з даних табл. 5, у якій наведено узагальненi результати біопсії слизової оболонки верхніх відділів ШКТ, яку виконано 5 дiтям із ХА та 3 пацієнтам із хворобами ШКТ, у дітей із ХА стравохiд не мав патологічних змін; а у шлунку та дванадцятипалій кишці виявлено ознаки хронiчного iмуноалергiчного запалення у вигляді помiрної атрофiї ворсинок із вкороченням та розширенням крипт, у просвіті окремих залоз виявлено щільний оксифільний секрет, а у власній пластинці слизової оболонки спостерігалась нерівномірна помірна інфільтрація плазматичними клiтинами з поодинокими лiмфоцитами та еозинофілами, що є характерними морфологічними ознаками гастроінтестинальної алергії. У дітей групи порівняння з боку стравоходу теж без патологічних знахідок; у шлунку і дванадцятипалій кишці помітні ознаки хронічного неспецифiчного запалення з вогнищами субатрофiї, псевдополiпозної гіперплазії та щільної сполучної тканини, у власній пластинці слизової оболонки визначено розсiяну лiмфоїдно-плазмоклiтинну iнфiльтрацiю, наявність лiмфатичних фолiкулів, крипт-абсцесів, вкорочення ворсинок.
Висновки
1. Iзольованих випадкiв гастроінтестинальної харчової алергiї не виявлено, у 67 % дiтей з алергiчними хворобами визначено конкретний харчовий продукт як причину гастроiнтестинальних симптомiв.
2. Поєднання алергiчних захворювань (харчової алергії, алергічного риніту, атопічного дерматиту і бронхіальної астми) супроводжується пiдвищенням рівня загального сироваткового IgE в 3–5 разiв та еозинофiлiв периферичної крові у 2–3 рази.
3. Морфологiчне дослiдження слизової оболонки верхнiх вiддiлiв ШКТ дозволяє виявити ознаки хронiчного iмуноалергiчного запалення для остаточного підтвердження діагнозу гастроiнтестинальної харчової алергії.
4. Показаннями для активного виявлення гастроiнтестинальної алергії можна вважати обтяжений з алергії сімейний анамнез та несприйняття харчових продуктiв у дитини чи в її рідних.
5. У разi виражених атопiчних проявiв, пов’язаних із харчовими продуктами, доцiльно проводити обстеження щодо сенсибiлiзацiї до конкретних харчових алергенiв для встановлення дiагнозу та дiєтотерапiї, яка є основним методом лiкування харчової алергiї.
6. При повторних скаргах на функціональні порушення органів травлення варто мати на увазi гастроiнтестинальну алергiю та проводити активне виявлення цiєї патологiї ендоскопiчним методом із бажаною бiопсiєю слизової оболонки в декiлькох (не менше 5, краще — 8) дiлянках верхнiх вiддiлiв ШКТ.
1. Балаболкин И.И. Клинико-иммунологические варианты атопического дерматита у детей и подростков и эффективность патогенетической терапии [Текст] / И.И. Балаболкин, Т.Е. Садикова // Педиатрия. — 2013. — Том 92, № 3. — С. 6-13.
2. Белицкая М.Ю. Особенности течения гастроинтестинального синдрома у детей первого года жизни, находящихся на естественном вскармливании [Текст] / М.Ю. Белицкая, Т.Б. Сенцова, С.Н. Денисова, И.Я. Конь и др. // Российский вестник перинатологии и педиатрии. — 2010. — № 5. — С. 45-51.
3. Боровик Т.Е. Механизмы развития пищевой аллергии [Текст] / Т.Е. Боровик, С.Г. Грибакин, С.Г. Макарова и др. // Педиатрия. — 2011. — Том 86, № 4. — С. 128-134.
4. Волосовец А.П. Теоретическое обоснование превентивной роли кишечной микробиоты в генезе аллергических заболеваний у детей [Текст] / А.П. Волосовец, С.П. Кривопустов, Н.Т. Макуха и др. // Дитячий лікар. — 2013. — № 4 (25). — С. 5-8.
5. Денисова С.Н. Диетотерапия гастроинтестинального синдрома у детей с атопическим дерматитом [Текст] / С.Н. Денисова // Лечащий врач. — 2012. — № 4. — С. 54-55.
6. Казначеева Л.Ф. Гастроинтестинальная форма пищевой аллергии у детей [Текст] / Л.Ф. Казначеева // Практическая медицина. — 2010. — № 45. — С. 88-92.
7. Клыкова Т.В. Пищевая аллергия у детей раннего возраста: подходы к диагностике и лечению [Текст] / Т.В. Клыкова, Е.В. Агафонова, И.Д. Решетникова // Практическая медицина. — 2011. — № 51. — С. 125-131.
8. Круглова Л.С. Симптомокомплекс дисбиоза у больных атопическим дерматитом и методы его коррекции [Текст] / Л.С. Круглова // Лечащий врач. — 2012. — № 5. — С. 38-44.
9. Мачарадзе Д.Ш. Атопический дерматит и пищевая аллергия. Что общего? [Текст] / Д.Ш. Мачарадзе// Лечащий врач. — 2013. — № 5. — С. 24-30.
10. Охотникова Е.Н. Гастроинтестинальная пищевая аллергия у детей [Текст] / Е.Н. Охотникова // Клінічна імунологія. Алергологія. Інфектологія. — 2013. — № 2. — С. 5-13.
11. Охотникова Е.Н. «Аллергический марш»: связь поколений и эскалация аллергии у детей [Текст] / Е.Н. Охотникова // Клінічна імунологія. Алергологія. Інфектологія. — 2008. — № 4 (15). — С. 7-15.
12. Ревякина В.А. Пищевая аллергия, гастроинтестинальные проявления [Текст] / В.А. Ревякина // Лечащий врач. — 2013. — № 4. — C. 13-17.
13. Сазонова Н.Е. Поражение верхнего отдела пищеварительного тракта у детей дошкольного возраста с атопическим дерматитом и гастроинтестинальными проявлениями пищевой аллергии [Текст] / Н.Е. Сазонова, Е.И. Шабунина, Н.Ю. Широкова и др. // Педиатрия. — 2013. — Том 92, № 3. — С. 13-17.
14. Blázquez A.B., Mayer L., Berin M.C. Thymic stromal lymphopoietin is required for gastrointestinal allergy but not oral tolerance [Теxt] / A.D. Blázquez, L. Mayer, M.C. Berin // Gastroenterology. — 2010. — Vol. 139 (4). — P. 1301-1309.
15. Bol-Schoenmakers M. et al. Regulation by intestinal gd T cells during establishment of food allergic sensitization in mice [Теxt] / [published online ahead of print September 29, 2010] // Allergy. — 2010. — P. 02479.
16. Can We Produce true Tolerance in Patients With Food Allergy? [Text] / M.C. Berin, L. Mayer // J. Allergy Clin. Immunol. — 2013. — Vol. 131, Issue 1. — P. 14-22.
17. Food allergy [Text] / S.Р. Sicherer, H.A. Sampson // J. Allergy Clin. Immunol. — 2010. — Vol. 125, Issue 2, Suppl. 2. — P. S354.
18. Mechanisms of Immune Tolerance Relevant to Food Allergy [Теxt] / B.P. Vickery, A.M. Scurlock et al. // J. Allergy Clin. Immunol. — 2011. — Vol. 127 (3). — P. 576-586.
19. Ostblom E., Lilja G., Pershagen G., van Hage M., Wickman M. Phenotypes of food hypersensitivity and Development of Allergic Diseases During the First 8 Years of Life [Теxt] / E. Ostblom, G. Lilja et al. // Clin. Exp. Allergy. — 2008. — Vol. 38. — P. 1325-1332.
20. Robison R.G. Food Allergy [Теxt] / R.G. Robison, J.A. Pongracic // Allergy Asthma Proc. — 2012. — Vol. 33, № 3. — P. 77-79.

/30/30.jpg)
/31/31_2.jpg)
/32/32.jpg)
/33/33.jpg)