Журнал «Здоровье ребенка» 1 (60) 2015
Вернуться к номеру
Прогнозування індивідуального ризику розвитку бронхіальної обструкції при гострих бронхітах у дітей раннього віку
Авторы: Абатуров О.Є., Русакова О.О. - Державний заклад «Дніпропетровська медична академія Міністерства охорони здоров’я України»
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Метою дослідження було визначення високоінформативних клініко-анамнестичних, імунологічних і молекулярно-генетичних факторів ризику розвитку бронхіальної обструкції при гострих бронхітах у дітей раннього віку.
Методи. Вміст γ-інтерферону (IFN-γ), інтерлейкінів-4 (IL-4) та -13 (IL-13) у сироватці крові вивчався за допомогою імуноферментного аналізу, концентрація загального IgE — електрохемілюмінесцентного імуноаналізу. Рівень експресії фактора транскрипції NF-κB у лімфоцитах периферійної крові досліджували методом проточної цитометрії.
Результати. Обстежено 80 дітей віком від 6 місяців до 3 років, хворих на гострий обструктивний бронхіт, та 40 дітей аналогічного віку з гострим простим бронхітом. Визначено фактори високого ризику та створена математична модель прогнозу формування бронхіальної обструкції при гострому бронхіті. Прогностичної значущості набули вік батька понад 38 років, затримка внутрішньоутробного розвитку, синдром дезадаптації, раннє штучне вигодовування, спадкова схильність до атопії, пасивне паління, лихоманка у поствакцинальному періоді, захворюваність на гострий обструктивний бронхіт в анамнезі та кількість його епізодів понад 2, паратрофія. Лихоманка до 37,7 °С, слабо виражений інтоксикаційний синдром до 3 діб, повільне носове дихання, IL-13 у межах 4,05–6,71 пг/мл і відносна кількість лімфоцитів, що експресують NF-kB, менша за 49,8 %, також були асоційовані з розвитком бронхіальної обструкції при гострому бронхіті.
Целью исследования было определение высокоинформативных клинико-анамнестических, иммунологических и молекулярно-генетических факторов риска развития бронхиальной обструкции при острых бронхитах у детей раннего возраста.
Методы. Содержание γ-интерферона (IFN-γ), интерлейкинов-4 (IL-4) и -13 (IL-13) в сыворотке крови изучалось с помощью иммуноферментного анализа, концентрация общего IgE — электрохемилюминесцентного иммуноанализа. Уровень экспрессии фактора транскрипции NF-κB в лимфоцитах периферической крови исследовали методом проточной цитометрии.
Результаты. Обследовано 80 детей в возрасте от 6 месяцев до 3 лет с острым обструктивным бронхитом и 40 детей аналогичного возраста с острым простым бронхитом. Определены факторы высокого риска и создана математическая модель прогноза формирования бронхиальной обструкции при остром бронхите. Прогностически значимыми признаны возраст отца старше 38 лет, задержка внутриутробного развития, синдром дезадаптации, раннее искусственное вскармливание, наследственная предрасположенность к атопии, пассивное курение, лихорадка в поствакцинальном периоде, более 2 эпизодов острого обструктивного бронхита в анамнезе, паратрофия. Лихорадка до 37,7 °С, слабо выраженный интоксикационный синдром продолжительностью до 3 суток, медленное носовое дыхание, IL-13 в пределах 4,05–6,71 пг/мл и относительное количество лимфоцитов, экспрессирующих фактор транскрипции NF-kB, менее 49,8 %, также были ассоциированы с развитием бронхиальной обструкции при остром бронхите.
The objective of the study was to determine highly informative clinical-anamnestic, immunological and molecular-genetic risk factors of bronchial obstruction in acute bronchitis in infants.
Methods. We have evaluated the content of IFN-γ, IL-4 and IL-13 in blood serum using enzyme-linked immunosorbent assay, the concentration of total IgE — using electrochemiluminescence immunoassay. The level of the transcription factor NF-κB expression in peripheral blood lymphocytes was studied by flow cytometry.
Results. We have examined 80 children aged from 6 months to 3 years with acute obstructive bronchitis, and 40 age-matched children with acute nonobstructive bronchitis. The factors of high risk were determined and the mathematical model for predicting bronchial obstruction in acute bronchitis was created. Father’s age over 38 years, intrauterine growth restriction, maladjustment syndrome, early artificial feeding, genetic predisposition to atopy, passive smoking, fever in the postvaccination period, history of acute obstructive bronchitis and number of its episodes more than 2, paratrophia became prognostically significant. Fever up to 37.7 °C, mild intoxication syndrome up to 3 days, slow nasal breathing, IL-13 within 4.05–6.71 pg/ml and the relative number of lymphocytes expressing NF-kB less than 49.8 % were also associated with the development of bronchial obstruction in acute bronchitis.
гострий бронхіт, бронхіальна обструкція, фактори ризику, діти раннього віку.
острый бронхит, бронхиальная обструкция, факторы риска, дети раннего возраста.
acute bronchitis, bronchial obstruction, risk factors, infants.
Статья опубликована на с. 55-60
Розвиток бронхіальної обструкції при гострих бронхітах у дітей реєструється у 20–25 % випадків, і значно частіше на гострий обструктивний бронхіт (ГОБ) хворіють діти перших трьох років життя [5, 8]. Упродовж останнього десятиріччя відзначається стабільне зростання поширеності даної клінічної форми гострого бронхіту [6, 7]. Формування ГОБ при інфекційному ураженні бронхіального дерева визначається анатомо-фізіологічними особливостями організму, а також характером і вираженістю запального процесу, що є результатом взаємодії генетичних, медико-біологічних і соціально-гігієнічних факторів [2, 6, 9].
Мета: визначити високоінформативні клініко-анамнестичні, імунологічні та молекулярно-генетичні фактори, що дасть можливість прогнозувати розвиток бронхіальної обструкції при гострих бронхітах у дітей раннього віку.
Матеріали та методи
Нами проведено обстеження 120 дітей віком від 6 місяців до 3 років, які отримували медичну допомогу в інфекційному відділенні № 3 КЗ «Дніпропетровська МДКЛ № 1» ДОР» з приводу гострого бронхіту. З них 80 пацієнтів, у яких діагностовано гострий обструктивний бронхіт з проявами дихальної недостатностi (ДН) I–II ст., становили основну групу спостереження. До групи порівняння ввійшли 40 дітей із діагнозом «гострий простий бронхіт» (ГПБ). Обстеження та лікування всіх дітей проводилось з урахуванням рекомендацій МОЗ України (наказ № 18, 2005). Крім того, для досягнення поставленої мети застосовувались імунологічні та молекулярно-генетичні методи дослідження. Від батьків чи опікунів пацієнтів було отримано інформовану згоду на участь у науковому дослідженні, яке проводилось відповідно до основних положень GСP ICH і Гельсінської декларації та з дозволу локальної комісії з біоетики КЗ «Дніпропетровська МДКЛ № 1» ДОР».
Визначення імунного статусу пацієнтів проводилось у центральній науково-дослідницькій лабораторії ДЗ «Дніпропетровська медична академія МОЗ України» та включало вивчення рівню концентрації γ-інтерферону (IFN-γ), інтерлейкінів-4 (IL-4) та -13 (IL-13) у сироватці крові за допомогою імуноферментного аналізу, вмісту загального IgE — електрохемілюмінесцентного імуноаналізу. Рівень експресії фактора транскрипції NF-kB у лімфоцитах периферійної крові досліджували методом проточної цитометрії на базі НДІ генетичних та імунологічних основ розвитку патології та фармакогенетики ВДНЗУ «УМСА» (м. Полтава). Зазначені обстеження проводились у гострому періоді захворювання та в періоді реконвалесценції.
Для статистичної обробки результатів дослідження використовувались комп’ютерні програми Statgraf, Matstat, Microsoft Excel для Windows. Для визначення факторів ризику розвитку гострого обструктивного бронхіту у дітей раннього віку було проведено послідовний аналіз Вальда. З використанням математичної програми оброблено 147 клініко-анамнестичних, імунологічних і молекулярно-генетичних параметрів, для кожного з них розраховано відносний ризик (ВР) та діагностичний коефіцієнт (ДК). Критерій відносного ризику визначався за формулою: ВР = fб (1 – fк) / fк(1 – fб), де fб — частота зустрічальності ознаки у дітей, хворих на ГОБ, fк — частота зустрічальності ознаки у дітей із ГПБ. Аналіз отриманих даних та оцінка вірогідності їх відмінностей проводились за допомогою пара- та непараметричних методів статистики. Різниця між ознаками, що порівнювались, вважалась значущою при р < 0,05 [3, 4].
Результати дослідження та їх обговорення
Вивчення прогностичної значущості досліджуваних параметрів дозволило відокремити найбільш інформативні клініко-анамнестичні, імунологічні та молекулярно-генетичні фактори ризику розвитку бронхіальної обструкції при гострих бронхітах у дітей перших трьох років життя.
Вік та стать дитини
Середній вік пацієнтів із гострим обструктивним бронхітом становив 14,6 ± 1,4 міс., з гострим простим бронхітом — 18,4 ± 2,0 міс. (р > 0,05). Найбільш високий ризик розвитку бронхіальної обструкції виявлено у віковій групі 6–16 міс. (ВР = 1,46), що певною мірою пояснюється анатомо-фізіологічними особливостями.
За гендерною ознакою в обох групах спостереження переважали хлопчики, при чому їх відносна кількість серед дітей, хворих на ГОБ, перевищувала таку серед дітей із ГПБ (77,5 проти 55 % відповідно), однак статистична значущість цих відмінностей не спостерігалась (р > 0,05). У той же час відзначено, що чоловіча стать є фактором ризику розвитку бронхообструкції при гострих бронхітах у дітей раннього віку (ВР = 1,46 у хлопчиків, ВР = 0,48 у дівчаток).
Вік батьків
Нами виявлено певний зв’язок між можливістю виникнення ГОБ та віком батька хворої дитини. У дітей, батьки яких були молодшими за 28 та старшими за 38 років, відносний ризик формування бронхіальної обструкції зростав (ВР = 1,53 та ВР = 2,08 відповідно), тоді як вік батька 28–38 років виступав протекторним фактором (ВР = 0,47).
Особливості анамнестичних даних
Діти основної групи спостереження частіше, ніж діти групи порівняння, народжувались від повторних (III–V) вагітностей (ВР = 1,67). Виникнення бронхіальної обструкції при гострому бронхіті також було пов’язано зі застосуванням матір’ю дитини антибіотиків під час вагітності (ВР = 1,75) та передчасними пологами (ВР = 1,67). Високий ризик формування ГОБ спостерігався у дітей із затримкою внутрішньоутробного розвитку (ЗВУР) (ВР = 2,92) та синдромом дезадаптації у неонатальному періоді (ВР = 2,0). Однак анемія під час вагітності була асоційована з розвитком гострого простого бронхіту (ВР = 0,29).
За нашими даними, середня тривалість грудного вигодовування дітей основної групи спостереження дорівнювала 3,6 ± 0,9 міс., дітей групи порівняння — 7,1 ± 2,1 (р > 0,05). Аналіз Вальда показав, що раннє переведення на штучне вигодовування відігравало значну роль у розвитку ГОБ (ВР = 2,23), тоді як годування дитини грудним молоком більше року визначено протектором гострого обструктивного бронхіту (ВР = 0,29).
Спадкова схильність до атопії, що відзначалась у 77,5 % дітей, хворих на ГОБ, та у 35 % дітей із ГПБ (р < 0,05), значно підвищувала ризик розвитку бронхіальної обструкції при гострому бронхіті (ВР = 2,23).
Формуванню ГОБ суттєво сприяло пасивне паління (ВР = 3,77). Цей факт реєструвався в анамнезі у 39 дітей (48,8 %) основної групи спостереження та у 5 дітей (12,5 %) групи порівняння (р < 0,05).
Розвиток бронхіальної обструкції при гострому бронхіті у дітей перших трьох років життя був також пов’язаний з наявністю поствакцинальної реакції у вигляді підвищення температури тіла, відносний ризик був високим і становив 2,14.
Захворюваність на гострі респіраторні інфекції
Більшість обстежених дітей (85 %) раніше хворіли на гостру респіраторну інфекцію (ГРІ). В обох групах спостереження середній вік дітей, коли вони вперше захворіли на ГРІ, був однаковим (6,7 ± 0,8 міс. для дітей основної групи, 6,5 ± 0,6 міс. для дітей групи порівняння). Однак перша захворюваність на респіраторну інфекцію у віці 8–15 міс., а також повторні ГРІ в анамнезі значно підвищували ймовірність розвинення бронхіальної обструкції при гострому бронхіті у майбутньому (ВР = 1,70 та ВР = 1,88 відповідно), що може пояснюватись підвищеним навантаженням незрілої імунної системи дитини. Перенесений раніше ГОБ, як і кількість його епізодів понад 2, були визначені факторами високого ризику формування рекурентних форм захворювання (ВР = 5,35 та ВР = 4,0 відповідно).
Супутня патологія
Ризик формування гострого обструктивного бронхіту був високим у дітей із рахітом (ВР = 1,46), перинатальним ураженням центральної нервової системи (ВР = 1,87) та паратрофією (ВР = 4,58), що збігається з даними інших дослідників [5, 7].
Особливості клінічних проявів захворювання
Початок захворювання у дітей основної групи спостереження характеризувався максимальним підвищенням температури тіла до 37,9 ± 0,2 °С, у дітей групи порівняння — до 38,8 ± 0,2 °С, що вірогідно не відрізнялось (р > 0,05). Однак лихоманку не вище 37,7 °С було визнано фактором високого ризику розвитку бронхіальної обструкції (ВР = 7,50), у той час як гіпертермія понад 38,9 °С значно знижувала ймовірність формування ГОБ (ВР = 0,32). Серед особливостей клінічних проявів захворювання у дітей основної групи спостереження реєструвались слабо виражений інтоксикаційний синдром (ВР = 5,83), що тривав не більше 3 діб (ВР = 3,33), та повільне носове дихання (ВР = 3,75). Відсутність синдрому периферичної лімфаденопатії знижувала можливість розвинення бронхіальної обструкції при гострому бронхіті у дітей перших трьох років життя (ВР = 0,42).
Імунний статус
У дітей основної групи спостереження продукція IFN-γ була значно нижчою, ніж у групі порівняння. Так, на початку захворювання середній вміст IFN-γ у сироватці крові пацієнтів з ГОБ становив 1,12 ± 0,45 пг/мл проти 1,92 ± 1,03 пг/мл у дітей, хворих на ГПБ (р < 0,05). За допомогою аналізу Вальда визначено малий ризик розвинення бронхіальної обструкції при рівні концентрації IFN-γ понад 9,83 пг/мл (ВР = 0,50). Середні показники вмісту IL-4 та IL-13 у сироватці крові дітей з ГОБ та ГПБ вірогідно не відрізнялись (1,79 ± 0,08 пг/мл та 4,15 ± 0,34 пг/мл проти 1,88 ± 0,12 пг/мл та 4,86 ± 0,76 пг/мл відповідно). Однак концентрація IL-13 у межах 4,06–6,71 пг/мл визнана фактором високого ризику формування бронхіальної обструкції (ВР = 4,0), у той час як рівень цього протизапального цитокіну понад 6,71 пг/мл запобігав розвитку ГОБ (ВР = 0,40), що можна пояснити інгібуючим впливом IL-13 на активність основного транскрипційного фактора запалення NF-kB [1].
У більшості обстежених дітей (54,5 % дітей із ГОБ та 60 % дітей із ГПБ) у гострому періоді захворювання спостерігалась підвищена концентрація IgE, середні значення якого дорівнювали у пацієнтів основної групи спостереження 96,0 ± 27,5 MO/мл (діти першого року життя — 36,4 ± 13,6 MO/мл, діти віком старше 1 року — 130,1 ± 35,5 MO/мл) та були значно вищими (р < 0,05) за показники пацієнтів групи порівняння — 50,5 ± 18,6 MO/мл (діти першого року життя — 22,0 ± 6,2 MO/мл, діти віком старше 1 року — 69,4 ± 31,1 MO/мл).
Рівень експресії фактора транскрипції NF-kB та відносна кількість лімфоцитів, що експресують нуклеарний фактор NF-kB, у дітей обох груп спостереження статистично не відрізнялись, що свідчить про подібність молекулярно–генетичних характеристик інфекційно-запального процесу у бронхіальному дереві [10]. Однак виявлено прямий кореляційний зв’язок цих параметрів з вираженістю інтоксикаційного синдрому (r = +0,35) та обернений — з наявністю синдрому бронхіальної обструкції (r = –0,38).
Ризик розвитку ГОБ був високим при відносній кількості лімфоцитів, що експресують фактор транскрипції NF-kB, менше за 49,8 % (ВР = 3,27), низьким — понад 49,9 % (ВР = 0,40). Протектором формування бронхіальної обструкції при гострому бронхіті у дітей раннього віку також визнано рівень експресії нуклеарного фактора kB 0,91–1,40 Од (ВР = 0,20).
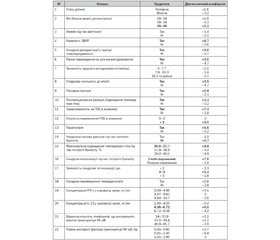
Таким чином, нами визначено високоінформативні клініко-анамнестичні, імунологічні та молекулярно-генетичні фактори та створено прогностичну таблицю, що дає можливість розрахувати ймовірність розвитку ГОБ (табл. 1).
Принцип роботи з математичною моделлю прогнозу розвитку бронхіальної обструкції при гострих бронхітах у дітей раннього віку полягає у складенні діагностичних коефіцієнтів, що відповідають виявленим у пацієнта ознакам. Імовірність формування ГОБ становить 80 % при досягненні суми ДК 6 балів, 90 % — 9,5 бала, 95 % — 13 балів.
Приклад. Дитина П., 9 міс., хлопчик (+1,6 бала) хворіє на гострий обструктивний бронхіт, ДН II ст. З анамнезу відомо: вік батька 46 років (+3,2 бала), під час вагітності анемії не було (–5,4 бала), неонатальний період перебігав гладко: відсутність ЗВУР (–0,6 бала) та синдрому дезадаптації (–0,7 бала), дитина рано переведена на штучне вигодовування (+3,5 бала), грудне молоко отримував протягом тижня (+1,1 бала), спадкової схильності до атопії немає (–4,7 бала), пасивний курець (+5,8 бала), –поствакцинальних реакцій не було (–0,2 бала), захворів на ГОБ вперше (–1,8 бала). Об’єктивно: нормотрофія (–0,2 бала), носове дихання повільне (+5,7 бала), максимальне підвищення температури тіла до 38,7 °С (–0,4 бала), слабо виражений інтоксикаційний синдром (+7,6 бала) купірувався на другу добу (+5,2 бала), периферична лімфаденопатія (+0,8 бала). Дані додаткових методів дослідження: IFN-k = 0,22 пг/мл (+0,5 бала), IL-13 = 2,82 пг/мл (–0,4 бала), відносна кількість лімфоцитів, що експресують фактор транскрипції NF-kB, дорівнювала 21,7 % (+2,1 бала), рівень експресії NF-kB 0,6 Од (+0,7 бала).
Загальна сума балів — 23,4, що свідчить про високий ризик формування бронхіальної обструкції при гострому бронхіті.
Показники ефективності даної математичної моделі прогнозу розвитку бронхіальної обструкції при гострих бронхітах у дітей раннього віку, що були отримані при її використанні на 48 пацієнтах, становили: чутливість — 90,9 %, специфічність — 86,7 %, тест прогнозування позитивного результату — 93,8 %, тест прогнозування негативного результату — 81,3 %.
Висновки
1. Факторами високого ризику формування бронхіальної обструкції при гострому бронхіті у дітей раннього віку визнано вік батька хворої дитини понад 38 років, наявність ЗВУР, синдром дезадаптаціїї у ранньому неонатальному періоді, раннє переведення на штучне вигодовування, спадкову схильність до атопії, пасивне паління, поствакцинальну реакцію у вигляді підвищення температури тіла, захворюваність на ГОБ в анамнезі та кількість його епізодів понад 2, паратрофію.
2. Розвинення гострого обструктивного бронхіту асоційовано з лихоманкою не вище 37,7 °С, слабо вираженим інтоксикаційним синдромом, що триває не більше 3 діб, та повільним носовим диханням.
3. Рівень концентрації IL-13 у сироватці крові у межах 4,05–6,71 пг/мл та відносна кількість лімфоцитів, що експресують фактор транскрипції NF-kB, менша за 49,8 %, значно підвищують ймовірність розвитку бронхіальної обструкції при гострому бронхіті у дітей перших трьох років життя.
4. Протекторами гострого обструктивного бронхіту визнано жіночу стать дитини, анемію під час вагітності, грудне вигодовування понад 15 місяців, відсутність периферичної лімфаденопатії, концентрацію IFN–y у сироватці крові у межах 9,84–14,7 пг/мл та рівень експресії фактора транскрипції NF-kB 0,91–1,40 Од.
5. Простота у використанні, а також високі показники ефективності розробленої математичної моделі прогнозу ймовірності розвитку бронхіальної обструкції при гострому бронхіті у дітей раннього віку дозволяють рекомендувати її в практичній діяльності сімейного лікаря для виділення контингенту дітей, у яких існує загроза формування ГОБ, та своєчасного призначення раціональної терапії.
1. Абатуров А.Е., Волосовец А.П., Юлиш Е.И. Индукция молекулярных механизмов неспецифической защиты респираторного тракта. — К.: Приватна друкарня ФОП Сторожук О.В., 2012. — 240 с.
2. Абатуров А.Е., Волосовец А.П., Юлиш Е.И. Инициация воспалительного процесса при вирусных и бактериальных заболеваниях, возможности и перспективы медикаментозного управления. — Х.: С.А.М., 2011. — 392 с.
3. Антомонов М.Ю. Математическая обработка и анализ медико-биологических данных / М.Ю. Антомонов. — К.: Фірма малого друку, 2006. — 558 с.
4. Двойрин В.В. Методика контролируемых испытаний / В.В. Двойрин, А.А. Клименков. — М.: Медицина, 1985. — 144 с.
5. Коваленко Т.С. Клінічна характеристика дітей раннього віку, хворих на гострий обструктивний бронхіт / Т.С. Коваленко // Український медичний альманах. — 2012. — Т. 15, № 6. — С. 79–83.
6. Коренюк О.С. Особливості терапії гострого обструктивного бронхіту у дітей раннього віку / О.С. Коренюк // Актуальні питання педіатрії, акушерства та гінекології. — 2014. — № 2. — С. 50–53.
7. Недельская С.Н. Факторы риска развития острого обструктивного бронхита у детей раннего возраста / С.Н. Недельская, Л.Н. Боярская, Т.Е. Шумная [и др.] // Здоровье ребенка. — 2007. — № 3(6). — С. 14–17.
8. Сміян О.І. Особливості клінічного перебігу гострого обструктивного бронхіту в дітей раннього віку / О.І. Сміян, В.А. Плахута // Проблеми безперервної медичної освіти та науки. — 2014. — № 2. — С. 38–41.
9. Bessa O.A. Prevalence and risk factors associated with wheezing in the first year of life / O.A. Bessa, A.J. Leite, D. Sole, J. Mallol // J. Pediatr. (Rio J.). — 2014. — V. 90, Issue 2. — P. 190–196.
10. Wullaert A. NF-B in the regulation of epithelial homeostasis and inflammation / A. Wullaert, M.C. Bonnet, M. Pasparakis // Cell. Res. — 2011. — V. 21, № 1. — P. 146–158.

/58/58.jpg)