Журнал «Здоровье ребенка» 1 (60) 2015
Вернуться к номеру
Структурна організація факторів уродженого імунітету в розвитку запалення слизової оболонки шлунка при H.pylori-інфекції у дітей
Авторы: Абатуров О.Є., Герасименко О.М. — Державний заклад «Дніпропетровська медична академія Міністерства охорони здоров’я України»
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Метою дослідження було вивчення за допомогою факторного аналізу структурних змін стану факторів уродженого імунітету в розвитку запалення слизової оболонки шлунка (СОШ) у дітей iз хелікобактерною інфекцією.
Методи. Для визначення рівня експресії TLR4, NLRC1/NOD1 у біоптаті СОШ та NF-κB у лімфоцитах периферичної крові використовувались молекулярно-генетичні методи, рівня в сироватці крові sCD14 та NT-proBNP — метод твердофазного імуноферментного аналізу.
Результати. За допомогою факторного аналізу вивчено структурнi зміни стану факторів уродженого імунітету в розвитку запалення СОШ у 128 дітей iз хронічними гастродуоденальними захворюваннями (ХГДЗ) у стадії загострення: 70 (54,7 %) пацієнтів, інфікованих Н.pylori, та 58 (45,3 %) дітей, у яких Н.pylori був відсутнім. Отримано фактори, що дозволили виділити основні структурні осі експресії компонентів уродженого імунітету, неспецифічних механізмів захисту, що визначають розвиток локального запалення СОШ (Р < 0,001). Показано, що запалення СОШ у пацієнтів iз хронічними гастродуоденальними захворюваннями, не асоційованими з Н.pylori, визначається двома сигнальними системами, активність яких знаходиться в обернено пропорційному співвідношенні: NLRC1/NOD1-асоційовані і TLR4-асоційовані каскади. У той час як провідним механізмом запалення СОШ при Н.pylori-асоційованих ХГДЗ у дітей є рецепторнезалежна активація фактора транскрипції NF-κB, а рецепторзалежні механізми більшою мірою зумовлюють продукцію NT-proBNP.
Целью исследования было изучение с помощью факторного анализа структурных изменений состояния факторов врожденного иммунитета в развитии воспаления слизистой оболочки желудка (СОЖ) у детей с хеликобактерной инфекцией.
Методы. Для определения уровня экспрессии TLR4, NLRC1/NOD1 в биоптате СОЖ и NF-κB в лимфоцитах периферической крови использовались молекулярно-генетические методы, уровня в сыворотке крови sCD14 и NT-proBNP — метод твердофазного иммуноферментного анализа.
Результаты. С помощью факторного анализа изучены структурные изменения состояния факторов врожденного иммунитета в развитии воспаления СОЖ у 128 детей с хроническими гастродуоденальными заболеваниями (ХГДЗ) в стадии обострения: 70 (54,7 %) пациентов, инфицированных Н.pylori, и 58 (45,3 %) детей, у которых Н.pylori отсутствовал. Получены факторы, позволившие выделить основные структурные оси экспрессии компонентов врожденного иммунитета, неспецифических механизмов защиты, которые определяют развитие локального воспаления СОЖ (Р < 0,001). Показано, что воспаление СОЖ у пациентов с хроническими гастродуоденальными заболеваниями, не ассоциированными с Н.pylori, определяется двумя сигнальными системами, активность которых находится в обратно пропорциональном соотношении: NLRC1/NOD1-ассоциированные и TLR4-ассоциированные каскады. В то время как ведущим механизмом воспаления СОЖ при Н.pylori-ассоциированных ХГДЗ у детей является рецепторнезависимая активация фактора транскрипции NF-κB, а рецепторзависимые механизмы в большей степени обусловливают продукцию NT-proBNP.
The objective of the study was to examine, using factor analysis, structural changes in the state of innate immunity factors in the development of gastric mucosal (GM) inflammation in children with H.pylori infection.
Methods. We used molecular genetic methods to determine the level of expression of TLR4, NLRC1/NOD1 in GM biopsy material and NF-B in peripheral blood lymphocytes, and enzyme-linked immunosorbent assay — to determine sCD14 and NT-proBNP levels in blood serum.
Results. Using factor analysis, we have studied structural changes in the state of innate immunity factors in the development of GM inflammation in 128 children with exacerbations of chronic gastroduodenal diseases (CGDD): 70 (54.7 %) patients infected with H.pylori, and 58 (45.3 %) children, in whom H.pylori was not detected. There were obtained factors enabled to identify the main structural axes in the expression of innate immunity components, non-specific defense mechanisms that determine the development of local GM inflammation (P < 0.001). It is shown that GM nflammation in patients with chronic gastroduodenal diseases, not associated with H.pylori, is determined by two signaling systems, the activity of which is in inverse proportion: NLRC1/NOD1-associated and associated TLR4-cascades. While the leading mechanism of GM inflammation in children with H.pylori-associated CGDD is receptor-independent activation of transcription factor NF-κB, and receptor-dependent mechanisms are mostly determine NT-proBNP production.
Helicobacter pylori, уроджений імунітет, факторний аналіз, діти.
Helicobacter pylori, врожденный иммунитет, факторный анализ, дети.
Helicobacter pylori, innate immunity, factor analysis, children.
Статья опубликована на с. 77-80
Вступ
В основі клінічних проявів запалення лежить неспецифічна захисна реакція організму на вплив будь-якого екзогенного або ендогенного ушкоджуючого фактора, основною метою якої є елімінація патогенного агента, локалізація його дії і репарація пошкоджених органів і тканин. Захист макроорганізму від патогенних інфекційних агентів обумовлений функціонуванням двох взаємопов’язаних ієрархічних імунних систем — неспецифічної вродженої та специфічної адаптивної. Неспецифічні механізми вродженого імунітету представляють філогенетично більш давню систему захисту організму від агресивної дії мікроорганізмів порівняно з адаптивною імунною системою. На відміну від специфічної відповіді імунної системи, для розвитку якої потрібен певний час, реакція неспецифічних механізмів захисту практично миттєва [1].
Колонізація шлунково-кишкового тракту Н.pylori не завжди призводить до розвитку патологічного процесу. Відповідь організму на Н.pylori залежить від стану імунітету людини, як уродженого, так і адаптивного, кількості рецепторів на поверхні шлунка, що сприяють адгезії мікроорганізму, вірулентності Н. pylori та ін.
Модуляція експресії генів, які індуковані H.pylori-інфекцією, пов’язана з активацією образрозпізнавальних рецепторів (pattern-recognition receptors, PRR), насамперед Toll-подібних (Toll-like receptor, TLR) і NOD-подібних (Nod-like receptor, NLR, NLR/NOD) рецепторів, а також сигнальних шляхів, що призводять до активації факторів транскрипції (насамперед ядерного фактора транскрипції kB (nuclear factor kappa-light-chain-enhancer of activated B cells, NF-kB). Глікопротеїн sСD14 — солютабна форма СD14, локалізований у плазмі і забезпечує взаємодію Н.pylori з епітеліоцитами слизової оболонки шлунка (СОШ). NT-proBNP та sСD14 також є інтегральними складовим вродженої імунної відповіді на інфекцію Н.pylori. Ліпополісахариди (lipopolysaccharide, LPS) — структурні компоненти зовнішньої мембрани грамнегативних бактерій — є одними з найвпливовiших патогенасоційованих молекулярних структур мікроорганізмів (pathogen-associated molecular patterns, PAMP), у тому числi H.pylori. [1–4, 6].
Метою дослідження було вивчення за допомогою факторного аналізу структурних змін стану факторів уродженого імунітету в розвитку запалення слизової оболонки шлунка у дітей iз хелікобактерною інфекцією.
Матеріали та методи дослідження
128 дітей віком від 7 до 17 років iз хронічними гастродуоденальними захворюваннями (ХГДЗ) у стадії загострення, які знаходилися на обстеженні і лікуванні в спеціалізованому дитячому гастроентерологічному відділенні Комунального закладу «Дніпропетровська дитяча міська клінічна лікарня № 1» Дніпропетровської обласної ради», залежно від наявності Н.pylori були розділені на дві групи. До першої (основної) групи увійшли 70 (54,7 %) пацієнтiв, інфікованих Н.pylori, до другої (порівняння) — 58 (45,3 %) дітей, у яких Н.pylori був відсутнім. Середній вік дітей у перший групі становив 14,04 ± 0,34 року, у другій — 14,12 ± 0,43 року. Для верифікації діагнозу та Н.pylori-статусу використовували ендоскопічне дослідження стравоходу, шлунка і дванадцятипалої кишки (Pentax FG-15W (Японія)), швидкий уреазний «Хелпіл»-тест та дихальний «Хелік»-тест з використанням індикаторних «Хелік»-трубок (ТОВ «АМА», Росія, Санкт-Петербург).
Визначення експресії NF-κB у лімфоцитах та експресії генів TLR4 та NLRC1/NOD1 у біоптаті СОШ проводилося в НДІ генетичних та імунних основ розвитку патології та фармакогенетики ВДНЗУ «Українська медична стоматологічна академія», м. Полтава (д.м.н., професор І.П. Кайдашев; к.м.н., ст.н.с. О.А. Шликова).
Метод твердофазного імуноферментного аналізу (ELISA) застосовували для оцінки концентрації в сироватці крові sCD14 та N-кінцевого фрагмента мозкового натрійуретичного пептиду В-типу (NT-proBNP), використовуючи ELISA test kit, Diaclone, France та HNP 1-3 ELISA, Biotech Lab-S відповідно (лабораторія «Діагностичний центр медичної академії», м. Дніпропетровськ).
Було отримано інформовану згоду батьків пацієнтів на участь у науковому дослідженні, яке проводили з дозволу локальної комісії з біоетики ДЗ «ДМА МОЗ України» та відповідно до етичних принципів GCP (якісна клінічна практика) щодо медичного дослідження. Статистичну обробку отриманих результатів проведено за допомогою пакетів комп’ютерних статистичних програм Statgraf, Matstat. Статистично значущими вважали відмінності при Р < 0,05.
Результати дослідження та їх обговорення
За допомогою факторного аналізу вивчено структурнi зміни стану факторів уродженого імунітету в розвитку запалення СОШ у 128 дітей iз ХГДЗ у стадії загострення. Отримано фактори, що дозволили виділити основні структурні осі експресії компонентів уродженого імунітету, неспецифічних механізмів захисту, що визначають розвиток локального запалення СОШ (Р < 0,001).
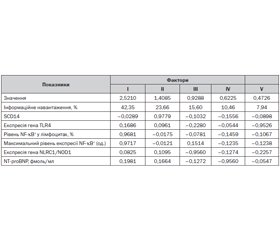
Факторна структура експресії компонентів неспецифічних механізмів захисту, що визначають розвиток локального запалення СОШ у дітей, які інфіковані Н.pylori, складалася з 5 чинників, що мають наступну інформаційну значимість та організовані наступними факторами (табл. 1): I фактор — 42,35 %; II фактор — 23,66 %; III фактор — 15,60 %; IV фактор — 10,46 %; V фактор — 7,94 %.
Факторна структура експресії компонентів неспецифічних механізмів захисту, що визначають розвиток локального запалення СОШ у дітей, які інфіковані Н.pylori, була організована 2 групами: позитивними І, ІІ (інформаційне навантаження 42,35 та 23,66 %) і негативними ІІІ, IV, V (інформаційне навантаження факторами 15,60; 10,46; 7,94 %). Провідне місце серед факторів локального запалення СОШ, асоційованого з Н.pylori, займав фактор, що характеризує активність ядерного фактора транскрипції NF-κB, що дозволяє зробити припущення про провідну роль NF-κB-асоційованого сигнального шляху в процесі запалення СОШ, яке індукується патогенасоційованими молекулярними патернами Н.pylori. Прямий зв’язок рівня активності NF-κB і змісту sCD14 у сироватці крові в дітей iз ХГДЗ, асоційованими з Н.pylori, може бути обумовлений патогенетично значимим впливом ліпополісахарида Н.pylori у розвитку запалення СОШ.
Групу факторів (ІІІ, IV, V) з обернено пропорційним відношенням до рівня активності NF-kB і sCD14 можна позначити як рецепторну групу, тому що вона містить такі фактори як експресія гена TLR4 і гена NLRC1/NOD1. Знаходження фактора V антимікробного пептиду NT-proBNP дозволяє вважати, що активність його продукції пов’язана з порушенням цих рецепторів. Обернено пропорційні відношення між рівнем збудження таких PRR, як TLR4, NLRC1/NOD1, та активністю ядерного фактора транскрипції NF-kB, цілком ймовірно, підкреслює рецепторнезалежні NF-κB шляхи збудження при інфікуванні Н.pylori.
У цей час виділено 12 різних внутрішньоклітинних сигнальних шляхів, за допомогою яких H.pylori активує фактор транскрипції NF-κB T4SS-залежним і T4SS-незалежним способом. T4SS-залежний каскад внутрішньоклітинних молекулярних шляхів, що активують фактор транскрипції NF-κB, у свою чергу, поділяють на CagA-залежний і CagA-незалежний [5].
До T4SS-залежних і CagA-залежних шляхів відносяться:
1) CagA → Ras → Raf → MEK → NF-κB;
2) CagA → c-Met → PI3K → Akt → NF-κB;
3) CagA → PPM1E/a PIX → PAK1 → NF-κB;
4) CagA → TRAF6 → TAK1 → NF-κB.
T4SS-незалежними сигнальними шляхами, що активують NF-κB, вважають:
1) UreB → CD74 → NF-κB;
2) OMV → NOD1 → NF-κB.
Факторна структура експресії компонентів неспецифічних механізмів захисту, що визначають розвиток локального запалення СОШ у дітей, які мали негативний Н.pylori-статус, складалася з 6 чинників, що мають наступну інформаційну значимість (табл. 2): I фактор — 39,27 %; II фактор — 16,37 %; III фактор — 14,51 %; IV фактор — 14,11 %; V фактор — 8,85 %; VI фактор — 6,89 %.
Факторна структура в групі пацієнтів з Н.pylori-негативним статусом складалася з 2 груп факторів з обернено пропорційним відношенням між ними. Перша, позитивна група (І, ІІ фактори) містила NT-proBNP і sCD14, тобто можна вважати, що основною спрямованістю досліджених нами молекулярних шляхів розвитку запального процесу в СОШ, що не асоційований з Н.pylori, є NLRC1/NOD1-залежна продукція антимікробного пептиду NT-proBNP.
Друга група з негативним значенням факторів (IV, V, VI) була організована фактором експресії гена TLR4 і активності фактора транскрипції NF-κB, що дозволяє вважати TLR4-залежний шлях збудження при розвитку запалення СОШ за відсутності хелікобактерної інфекції.
Таким чином, запалення СОШ у пацієнтів iз ХГДЗ, не асоційованих iз Н.pylori, визначається двома сигнальними системами, активність яких знаходиться в обернено пропорційному співвідношенні: NLRC1/NOD1-асоційовані і TLR4-асоційовані каскади. У той час як провідним механізмом запалення СОШ у дітей iз Н.pylori-асоційованими хронічними гастродуоденальними захворюваннями є рецепторнезалежна активація фактора транскрипції NF-κB, а рецепторзалежні механізми більшою мірою зумовлюють продукцію NT-proBNP.
Ураховуючи особливості розвитку запального процесу слизової оболонки при інфікуванні Н.pylori (а саме рецепторнезалежну активацію фактора транскрипції NF-κB), ми вважаємо, що проведення ерадикаційної терапії необхідно поєднувати з призначенням препаратів, які пригнічують активність молекулярних компонентів NF-κB-залежних механізмів запалення.
1. Абатуров А.Е. Инициация воспалительного процесса при вирусных и бактериальных заболеваниях, возможности и перспективы медикаментозного управления [Текст] / А.Е. Абатуров, А.П. Волосовец, Е.И. Юлиш. — Х.: С.А.М., 2011. — 392 с.
2. Леженко Г.О. Патогенетичне значення антимікробних пептидів у реалізації антибактеріального захисту у дітей, хворих на муковісцидоз [Текст] / Г.О. Леженко, О.Є. Абатуров, О.Є. Пашкова, Л.І. Пантюшенко // Здоровье ребенка. — 2013. — 3(46). — 44-49.
3. Kawai T., Akira S. The role of pattern-recognition receptors in innate immunity: update on Toll-like receptors [Text] // Nat. Immunol. — 2010. — 11(5). — 373-84. doi: 10.1038/ni.1863.
4. Lu Y.C. LPS/TLR4 signal transduction pathway [Text] / Y.C. Lu, W.C. Yeh, P.S. Ohashi // Cytokine. — 2008. — 42(2). — 145-51. doi: 10.1016/j.cyto.2008.01.006.
5. NF-kappaB activation and potentiation of proinflammatory responses by the Helicobacter pylori CagA protein [Text] / S. Brandt, T. Kwok, R. Hartig, W. König, S. Backert // Proc. Natl Acad. Sci. USA. — 2005. — 102(26). — 9300-5.
6. Yang Z.M. Gene expression profiling in gastric mucosa from Helicobacter pylori-infected and uninfected patients undergoing chronic superficial gastritis [Text] / Z.M. Yang, W.W. Chen, Y.F. Wang // PLoS One. — 2012. — 7(3). — e33030. doi:10.1371/journal. pone.0033030.

/79/79.jpg)