Журнал «Здоровье ребенка» 1 (60) 2015
Вернуться к номеру
Результаты мониторинга осложнений вакцинации БЦЖ
Авторы: Лепшина С.М. — Донецкий национальный медицинский университет им. М. Горького; Скрипка Л.В. — Государственное учреждение «Донецкий областной лабораторный центр Госсанэпидслужбы
в Украине»; Тищенко Е.В., Скрипка Н.С., Юровская Е.И. — Донецкий национальный медицинский университет им. М. Горького
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
В условиях напряженной эпидемиологической ситуации по туберкулезу в Украине сохраняется актуальность вакцинации БЦЖ. Вакцины БЦЖ безопасны, однако при их применении существует риск развития осложнений. В Донецкой области с 2004 по 2008 г. удельный вес осложнений после иммунизации не превышал 0,09 %, с 2008 по 2012 г. отмечен его рост до 0,6 %. Установлено, что он связан с использованием вакцины БЦЖ «Statens Serum Institut» производства Государственного серологического института (Дания). В 2008 г. в регионе впервые были зарегистрированы случаи БЦЖ-оститов на вакцину БЦЖ и БЦЖ-М (штамм БЦЖ-1, Российская Федерация), ранее подобные случаи относили к туберкулезу костей.
В умовах напруженої епідеміологічної ситуації з туберкульозу в Україні зберігається актуальність вакцинації БЦЖ. Вакцини БЦЖ безпечні, однак при їх застосуванні існує ризик розвитку ускладнень. У Донецькій області з 2004 по 2008 р. питома вага ускладнень після імунізації не перевищувала 0,09 %, з 2008 по 2012 р. відзначено її зростання до 0,6 %. Установлено, що воно пов’язане з використанням вакцини БЦЖ «Statens Serum Institut» виробництва Державного серологічного інституту (Данія). У 2008 р. в регіоні вперше були зареєстровані випадки БЦЖ-оститів на вакцину БЦЖ і БЦЖ-М (штам БЦЖ-1, Російська Федерація), раніше подібні випадки відносили до туберкульозу кісток.
BCG vaccination remains relevant because of the tense epidemiological situation on tuberculosis in Ukraine. BCG vaccines are safe, but when they are used, there is a risk of complications. In the Donetsk region, from 2004 to 2008 the proportion of complications after immunization did not exceed 0.09 %, from 2008 to 2012 their growth was marked up to 0.6 %. It was found that it was associated with the use of BCG vaccine manufactured by Statens Serum Institut (Denmark). In 2008, cases of BCG-induced osteitis on BCG and BCG-M vaccine (strain BCG-1, Russian Federation) were detected firstly in the region, earlier such cases were considered as bone tuberculosis.
вакцинация БЦЖ, осложнения.
вакцинація БЦЖ, ускладнення.
BCG vaccination, complications.
Статья опубликована на с. 160-162
В Украине эпидемиологическая ситуация по туберкулезу остается напряженной. По мнению специалистов ВОЗ, главными компонентами программы борьбы с туберкулезом являются выявление больных и вакцинация против туберкулеза [2]. Вакцинация БЦЖ завоевала признание во многих странах мира. Она обязательна в 64 странах, официально рекомендована в 118. Данная прививка проведена приблизительно 2 млрд человек. Она предупреждает развитие тяжелых форм заболевания, связанных с гематогенным распространением микобактерий туберкулеза [5].
Противотуберкулезная вакцина — это препарат из живых аттенуированных бактерий БЦЖ. Их способность размножаться внутриклеточно приводит к возможности развития осложнений после иммунизации (от 0,04 до 4 %) [1, 6]. Осложнения БЦЖ диагностируются в разные сроки от момента введения вакцины. Согласно классификации, предложенной Международным союзом по борьбе с туберкулезом (1984), выделяют категорию 1 — локальные поражения (подкожные инфильтраты, холодные абсцессы, язвы) и региональные лимфадениты, категорию 2 — персистирующая и диссеминированная БЦЖ-инфекция без летального исхода (волчанка, оститы), категорию 3 — диссеминированная БЦЖ-инфекция, генерализованное поражение с летальным исходом, категорию 4 — пост-БЦЖ-синдром (узловатая эритема, кольцевидная гранулема, высыпания) [5].
В Украине длительное время применяли вакцины БЦЖ и БЦЖ-М (штамм БЦЖ-1, Российская Федерация). С учетом важности и необходимости проведения противотуберкулезной иммунопрофилактики в условиях эпидемии туберкулеза Министерством здравоохранения Украины было принято решение о целесообразности внедрения противотуберкулезной вакцины БЦЖ SSI (Statens Serum Institut) производства Государственного серологического института (Дания) [3, 4].
В течение четырех лет (2008–2012 гг.) вакцинацию против туберкулеза проводили вакцинами БЦЖ разного штаммового состава и разных производителей: SSI (Дания), «Медгамал» НИИЭМ им. Н.Ф. Гамалеи РАМН (Российская Федерация), ФГУП «НПО «Микроген» Минздравсоцразвития России (Российская Федерация). Нами были изучены результаты мониторинга осложнений после иммунизации вакциной БЦЖ в Донецкой области за период 2004–2013 гг.
Целью исследования было изучение количества и характера осложнений вакцинации БЦЖ в Донецкой области в течение двух периодов: 2004–2007 и 2008–2013 гг.
Материалы и методы
Использовали материалы расследований 1004 случаев осложнений после использования вакцины БЦЖ, предоставленные специалистами лечебно-профилактических учреждений и санэпидслужбы области, обобщенные данные о поствакцинальных реакциях и осложнениях после введения вакцин (отчеты 2004–2013 гг.), обобщенные данные о выполнении профилактических прививок (компьютерная программа «УкрВак», отчеты 2004–2013 гг.). Осложнения вакцинации БЦЖ определены согласно приказу Министерства здравоохранения Украины от 16.09.2011 г. № 595 «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обігу медичних імунобіологічних препаратів». Материал обработан методами вариационной статистики.
Результаты
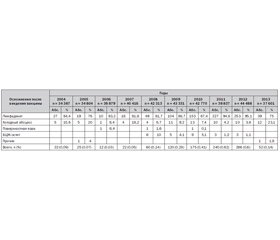
В среднем ежегодно в области вакциной БЦЖ прививают около 40 тысяч новорожденных детей. Поствакцинальные осложнения регистрируют ежегодно (табл. 1).
Из табл. 1 видно, что в первые четыре года наблюдения удельный вес поствакцинальных осложнений не превышал 0,09 %. Существенный рост осложнений — до 0,14 % отмечен с 2008 г., когда преимущественно использовали вакцину БЦЖ SSI (производство Дании). С целью проверки качества вакцинации был проведен мониторинг лечебных учреждений, осуществляющих вакцинацию БЦЖ новорожденных и детей. Техника введения вакцины была нарушена в 36 случаях. Через год число осложнений выросло еще в 2 раза. В 2011 г. количество осложнений достигло 0,62 %. Приказом Министерства здравоохранения Украины от 22.06.2011 г. № 371 «Про затвердження використання вакцини БЦЖ для щеплення новонароджених» был отменен приказ Министерства здравоохранения Украины от 07.07.2008 г. № 366 «Про затвердження програми переходу до протитуберкульозного щеплення вакциною БЦЖ SSI (Данський штам) в Україні». В 2013 г. в результате отказа от вакцины БЦЖ датского производства количество осложнений снизилось до 52 (0,14 %), р < 0,001.
Нами изучен также характер осложнений. Наибольшее их количество зарегистрировано в виде регионарных лимфаденитов: 789 (0,4 %) случаев после применения вакцины БЦЖ SSI (производства Дании), 31 (0,07 %) случай — на вакцину БЦЖ производства ФГУП «НПО «Микроген» (Российская Федерация), 4 (0,01 %) — на вакцину БЦЖ производства «Медгамал» НИИЭМ им. Н.Ф. Гамалеи РАМН (Российская Федерация).
В целом техника введения вакцины была нарушена в 56 случаях. В 2 (0,0004 %) случаях это явилось причиной развития поверхностной язвы после применения вакцины БЦЖ производства ФГУП «НПО «Микроген» (Российская Федерация) и SSI (Дания), в 54 (0,04 %) — подкожных холодных абсцессов, в т.ч. 25 — на вакцину БЦЖ производства SSI (Дания), 28 — производства ФГУП «НПО «Микроген», 1 — «Медгамал» НИИЭМ им. Н.Ф. Гамалеи РАМН (Российская Федерация). Зарегистрировано 26 случаев БЦЖ-ассоциированных оститов, в т.ч. 2 на вакцину БЦЖ производства SSI (Дания). Таким образом, в течение всего срока наблюдения среди поствакцинальных осложнений превалировали лимфадениты (более 80 %), холодные абсцессы составили 20 %. Поверхностная язва была отмечена в единичных случаях в 2005, 2008, 2010 гг. В 2008 г. впервые были зарегистрированы случаи БЦЖ-оститов на вакцину БЦЖ российского производства. Ранее подобные случаи трактовались как туберкулез костей.
Всем детям с поствакцинальными осложнениями была проведена химиотерапия противотуберкулезными препаратами 1-го ряда, исключая пиразинамид. При формировании холодного абсцесса использовали хирургический метод лечения, при поверхностной язве — местное лечение.
Выводы
В структуре осложнений после вакцинации БЦЖ независимо от вида вакцины превалируют лимфадениты. Рост осложнений с 0,09 до 0,6 % обусловлен использованием вакцины БЦЖ датского производства, случаи БЦЖ-оститов отмечены при использовании вакцины БЦЖ российского производства.
1. Імунопрофілактика туберкульозу у дітей: проблеми і перспективи / Білогорцева О.І. // Український пульмонологічний журнал. — 2008. — № 3. — С. 29–30.
2. Осложнения после вакцинации против туберкулеза / Д.Т. Леви, Н.В. Александрова, Т.А. Севостьянова [и др.] // Туберкулез и болезни легких. — 2013. — № 9. — С. 15–22.
3. Приказ Министерства здравоохранения Украины от 30.10.2009 № 787 «Інструкція про застосування БЦЖ вакцини SSI».
4. Приказ Министерства здравоохранения Украины от 07.07.2008 г. № 366 «Про затвердження програми переходу до протитуберкульозного щеплення вакциною БЦЖ SSI (данський штам) в Україні».
5. Фтизиатрия: Национальное руководство / Под ред. М.И. Перельмана. — М.: ГЭОТАР-Медиа, 2007. — 512 с.
6. Щодо моніторингу післявакцинальних ускладнень після вакцинації БЦЖ в Донецькій області / С.В. Моховик, Т.А. Біломеря, Г.М. Дараган, Р.А. Родина, О.О. Демкович, Т.В. Кирилова, Л.В. Скрипка // Український пульмонологічний журнал. — 2013. — № 3 (81). — С. 181.

/161/161.jpg)