Журнал «Здоровье ребенка» 3 (63) 2015
Вернуться к номеру
Місце пробіотиків у терапії та профілактиці виникнення вторинного ацетонемічного синдрому
Авторы: Леженко Г.О., Пашкова О.Є. — Запорізький державний медичний університет
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
Стаття присвячена проблемі терапії ацетонемічного синдрому у дітей із гострими респіраторними вірусними інфекціями. Патогенетично обґрунтовано застосування в терапії вторинного ацетонемічного синдрому пробіотичного препарату Субалін. Показано, що застосування Субаліну в комплексній терапії дітей з ацетонемічним синдромом, який розвинувся на тлі гострої респіраторної вірусної інфекції, усуває синдром інтоксикації та сприяє швидкому регресу клінічних симптомів захворювання. Відмічено зменшення частоти виникнення ацетонемічних кризів протягом 6 місяців у групі дітей, які отримували Субалін, що дозволяє рекомендувати використання даного пробіотика як неспецифічної профілактики розвитку означеного патологічного стану.
Статья посвящена проблеме терапии ацетонемического синдрома у детей с острыми респираторными вирусными инфекциями. Патогенетически обосновано применение в терапии вторичного ацетонемического синдрома пробиотического препарата Субалин. Показано, что применение Субалина в комплексной терапии детей с ацетонемическим синдромом, который развился на фоне острой респираторной вирусной инфекции, устраняет синдром интоксикации и способствует быстрому регрессу клинических симптомов заболевания. Отмечено уменьшение частоты развития ацетонемических кризов в течение 6 месяцев в группе детей, получавших Субалин, что позволяет рекомендовать использование данного пробиотика в качестве неспецифической профилактики развития указанного патологического состояния.
The article deals with the problem of therapy for acetonemic syndrome in children with acute respiratory viral infections. Application of probiotic preparation Subalin in the treatment of secondary acetonemic syndrome is pathogenetically reasonable. It has been shown that the use of Subalin in the combination therapy of children with acetonemic syndrome against the background of acute respiratory viral infections removed intoxication syndrome and contributed to the rapid regression of clinical symptoms of the disease. Reduction of the acetonemic crises incidence over the 6 months has been noted in the group of children who received Subalin that enables to recommend the use of this probiotic agent as a non-specific prevention for the above-mentioned pathological condition.
ацетонемічний синдром, гострі респіраторно-вірусні інфекції, діти, Субалін.
ацетонемический синдром, острые респираторно-вирусные инфекции, дети, Субалин.
acetonemic syndrome, acute respiratory viral infection, children, Subalin.
Статья опубликована на с. 31-34
Ацетонемічний синдром — один із найбільш поширених патологічних станів дитячого віку, що проявляється стереотипними повторними епізодами блювоти, які чергуються з періодами повного благополуччя. Основними ланками метаболічних порушень при ацетонемічних станах виступають підвищення енергетичних витрат, порушення процесів гліколізу і ліполізу, неповне окислення жирних кислот, розпад кетогенних амінокислот, накопичення кетонових тіл, що призводить до розвитку кетоацидозу і, як наслідок, — ендогенної інтоксикації, що супроводжується нападами нестримного блювання [4]. Ацетонемічний синдром негативно впливає на організм дитини [8]. Надлишок кетонових тіл поводиться в організмі вкрай агресивно — подразнює слизову оболонку шлунково-кишкового тракту, пошкоджує ліпідний бішар клітинних мембран, посилює нестачу кисню тощо. Таким чином формується порочне коло.
Більшість вітчизняних педіатрів виділяють два різновиди ацетонемічного синдрому — первинний і вторинний [1, 3, 11]. Первинний ацетонемічний синдром зустрічається у дітей із порушенням пуринового обміну з надлишковою продукцією сечової кислоти та її попередників, нестійкістю вуглеводного й ліпідного обміну (зі схильністю до кетозу), лабільністю медіаторних функцій нервової системи, що визначають особливості її реакцій. Вторинний ацетонемічний синдром найбільш часто виникає при інфекційному токсикозі; поєднаній патології шлунково-кишкового тракту, що супроводжується симптомами інтоксикації, холестазу; токсичному ураженні печінки; при порушенні мікрофлори кишечника.
Схильність дітей до розвитку ацетонемічного синдрому на тлі різноманітних інфекційних захворювань підкреслюється багатьма авторами [8, 9]. Протягом останніх років у структурі причин госпіталізації питома вага дітей із вторинним ацетонемічним синдромом збільшилася в 5,4 раза [10]. Передумовами для розвитку кетозу виступають вікові особливості обміну речовин, аліментарне голодування та стрес будь-якої природи, що завжди мають місце при інфекційних захворюваннях у дітей [5]. Крім того, це може бути пов’язано з існуванням субкомпенсованого дисбактеріозу, що посилюється призначенням антибактеріальної терапії у зв’язку з тривалою лихоманкою, вираженістю інтоксикаційного і катарального синдромів, розвитком бактеріальних ускладнень. Як відомо, аутофлора кишечника бере участь у метаболізмі азот- і вуглецевмісних сполук та сечовини. Мікробіоценоз кишечника реалізує функцію гідролізу продуктів метаболізму білків, ліпідів, вуглеводів, декон’югацію жовчних і гідроксилювання жирних кислот та ін. Недостатність детоксикаційної функції аутофлори шлунково-кишкового тракту при дисбіотичних порушеннях підвищує напруження ферментних систем із подальшими метаболічними і структурними змінами в органах травлення. Вкрай важливою захисною функцією мікробіоти кишечника є створення власної колонізаційної резистентності, що забезпечує запобігання заселенню організму господаря іншими штамами, пригнічення життєдіяльності патогенних або умовно-патогенних мікроорганізмів [6]. Мікрофлора кишечника бере активну участь у формуванні імунобіологічних реакцій організму. Бактеріальні модуліни біфідо- і лактобактерій стимулюють синтез імуноглобулінів, інтерферонів, цитокінів, збільшують кількість комплементу, підвищують активність лізоциму, стимулюють дозрівання макрофагально-гістіоцитарної системи [2]. При цьому порушення нормального складу мікрофлори кишечника уповільнює процеси знешкодження токсичних продуктів обміну речовин, погіршує всмоктування вуглеводів за рахунок посилення процесу бродіння, а це, у свою чергу, ускладнює перебіг ацетонемічного стану. І знову формується порочне коло. У зв’язку з цим призначення пробіотиків у терапії ацетонемічного синдрому є обґрунтованим. Застосування препаратів даної групи призводить до відновлення нормальної кишкової мікрофлори і таким чином сприяє нормалізації всмоктування глюкози та відновленню енергетичного балансу в організмі. Крім того, застосування пробіотиків у дітей, які мають схильність до розвитку ацетонемічного синдрому, у періоді клінічного благополуччя може зменшити ймовірність виникнення кризів надалі.
Враховуючи, що саме прийом антибіотиків на тлі ускладнень гострої респіраторно-вірусної інфекції (ГРВІ) провокує посилення дисбактеріозу й виникнення ацетонемічного синдрому, раціональний вибір пробіотичного препарату є запорукою адекватної терапії. Зважаючи на це, нашу увагу привернув біопрепарат Субалін (ПрАТ «Біофарма», Україна), що являє собою ліофілізовану масу бактерій Bacillus subtilis. Специфічна активність препарату визначається кількістю життєздатних бактерій в одній дозі препарату і їх антагоністичною активністю. В одній дозі препарату міститься 1 • 109 живих мікробних клітин Bacillus subtilis 2335/105. Препарат Субалін має антивірусні та імуномодулюючі властивості, а також пригнічує ріст патогенних і умовно-патогенних мікроорганізмів, сприяючи, таким чином, нормалізації якісного й кількісного складу кишкової мікрофлори. Препарат має антагоністичну дію щодо тест-штамів: Shigella sonnei, Salmonella typhimurium, Staphylococcus aureus, Candida albicans, а також характеризується здатністю продукувати α-2-інтерферон людини. Завдяки цим ефектам Субалін одночасно впливає на причину, що спровокувала ацетонемічний синдром (тобто на збудника ГРВІ), і відновлює нормальну флору, роль якої також важлива у вуглеводному обміні. Противірусна активність Субаліну була підтверджена в експериментальних дослідженнях. Так, навіть при однократному пероральному введенні препарату лабораторним щурам за добу до зараження вірусом грипу індекс ефективності становив 73 [14]. Аналогічні результати були отримані і при експериментальній герпесвірусній інфекції [12].
Субалін відрізняється високим ступенем безпеки — пробіотична культура Bacillus subtilis 2335/105 не містить факторів патогенності, не є вірулентною, токсигенною, токсичною. Безпечність Субаліну було підтверджено в клінічних дослідженнях [13]. При прийомі препарату добровольцями, а також під час усього терміну спостереження після курсу введення Субаліну не відмічені побічні явища або ускладнення, пов’язані з прийомом препарату (навіть в осіб зі схильністю до алергії). При пероральному застосуванні препарату Субалін не відбувалися патологічні зміни нормобіоценозу мікрофлори кишечника. Встановлено, що культура, що входить до складу препарату, не персистує тривалий час в організмі і, ймовірно, з цим можна пов’язати швидке зниження рівня інтерферону в організмі після закінчення застосування препарату. Цей факт є особливо важливим, оскільки можна регулювати кількість інтерферону в організмі людини призначенням певних доз і курсів введення Субаліну. При застосуванні препарату в добровольців не виявлялися антитіла до інтерферону, який продукує рекомбінантна культура. Це також є додатковим свідченням нешкідливості препарату для організму людини [13].
Мета дослідження — оцінка ефективності застосування препарату Субалін у комплексній терапії дітей із ацетонемічним синдромом, що розвинувся на тлі гострої респіраторної вірусної інфекції.
Матеріали та методи дослідження
Під нашим наглядом знаходилося 32 дитини з ацетонемічним синдромом, що розвинувся на тлі гострих респіраторних вірусних інфекцій, віком від 3 до 7 років. Ступінь тяжкості ацетонемічного синдрому оцінювали за 3-бальною системою, запропонованою О.П. Волосовцем із співавт. (2009) [3]. Всі хворі були розподілені на дві групи, репрезентативні за віком, статтю та ступенем клінічних проявів ацетонемічного синдрому. Першу групу становили 15 хворих (основна група), другу — 17 дітей (група порівняння). Всім пацієнтам було призначено терапію основного захворювання та базисне лікування ацетонемічного синдрому, що включало дезінтоксикаційну та регідратаційну інфузійну терапію, ентеросорбенти, протиблювотні засоби та панкреатичні ферменти за показаннями. Всі діти отримували лужне питво та акетогенну дієту. Додатково діти першої групи з другого дня терапії (після зменшення блювоти) отримували препарат Субалін по 1 дозі два рази на день за 30 хвилин до вживання їжі протягом 20 днів. Ефективність терапії оцінювалась за швидкістю оборотного розвитку симптомів інтоксикації, астенічного синдрому та ступеня ацетонурії.
Результати дослідження та їх обговорення
У всіх дітей, які знаходилися під спостереженням, перебіг ацетонемічного синдрому на тлі ГРВІ характеризувався наявністю багаторазової блювоти — від 5 до 10 разів на добу, підвищенням температури тіла до фебрильних цифр, болем у животі, відмовою від їжі. При об’єктивному огляді звертала на себе увагу сухість слизової оболонки порожнини рота, сухість та блідість шкірних покривів, яскравий рум’янець на щоках, запах ацетону в повітрі при видиху. При цьому прояви кетоацидозу поєднувалися з симптомами ГРВІ — нежитем, кашлем, гіперемією слизової ротоглотки. Гострий ринофарингіт було діагностовано у 4 (26,7 %) дітей основної групи та 6 (35,3 %) — групи порівняння, гострий ларинготрахеїт — у 7 (46,7 %) та 6 (35,3 %) хворих відповідно, а в 6 (40,0 %) пацієнтів основної групи та 5 (29,4 %) дітей групи порівняння ацетонемічний синдром розвинувся на тлі гострого бронхіту.
У клінічному аналізі крові у 5 (33,3 %) пацієнтів основної групи та 6 (35,3 %) дітей групи порівняння виявлялася лейкопенія. Помірний лейкоцитоз із паличкоядерним зсувом лейкоцитарної формули та підвищення ШОЕ відмічались у 10 (66,7 %) та 11 (64,7 %) хворих відповідно. Підвищення гематокриту було зареєстровано у 3 (20,0 %) хворих основної групи та в 4 (23,5 %) дітей групи порівняння. У клінічному аналізі сечі в дітей обох груп визначалася кетонурія від 2 до 4 плюсів.
Визначення рівня глюкози крові виявило наявність тенденції до гіпоглікемії у 2 (13,3 %) дітей основної групи та у 3 (17,6 %) хворих групи порівняння. Як відомо, гіпоглікемія поряд із повним або частковим голодуванням може бути однією з причин підвищеного утворення кетонових тіл у дітей та виступає як провокуючий фактор розвитку ацетонемічного синдрому [7].
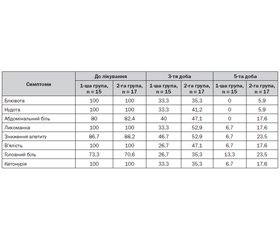
У всіх дітей на фоні терапії, що проводилася, відмічено клінічне поліпшення (табл. 1).
Проте в пацієнтів першої групи відмічався більш швидкий регрес показників. З урахуванням отриманих даних найбільш інтенсивній вплив прийом препарату Субалін справляв на такі симптоми, як блювота, нудота, абдомінальний біль та ступінь кетонурії. Крім того, додаткове призначення до комплексної терапії ацетонемічного синдрому препарату Субалін сприяло зменшенню тривалості лихоманки (2,5 ± 0,4 дня в основній групі проти 3,9 ± 0,5 дня в групі порівняння, р < 0,05), інтоксикаційного синдрому, який в основній групі становив у середньому 2,5 ± 0,2 доби, а в групі порівняння — 4,0 ± 0,3 доби (р < 0,05).
Препарат добре переносився. За період його прийому не відмічено жодного випадку побічних ефектів.
Проведений аналіз катамнезу дітей груп спостереження показав, що в подальші 6 місяців при захворюванні на ГРВІ ацетонемічний синдром розвинувся лише в 1 (6,7 %) дитини основної групи, тоді як у групі дітей, які не отримували препарат Субалін, ацетонемічні кризи спостерігалися у 6 (35,3 %) пацієнтів (р < 0,05).
Висновки
1. Застосування препарату Субалін у комплексній терапії ацетонемічного синдрому у дітей із гострими респіраторними вірусними інфекціями сприяє ранній ліквідації проявів ацетонемічного синдрому та симптомів ГРВІ.
2. Застосування пробіотичного препарату в комплексній терапії вторинного ацетонемічного синдрому виступає фактором неспецифічної профілактики розвитку означеного патологічного синдрому.
1. Бережной В.В. Ацетонемический синдром — шаги доктора-практика / В.В. Бережной, Л.В. Курило, В.В. Корнева, М.А. Капичина // Современная педиатрия. — 2012. — № 2 (42). — С. 1–5.
2. Береза Н.Н. Проблемы дисбактериоза кишечника и его коррекции / Н.Н. Береза // Гастроэнтерология. — 2000. — Вып. 31. — С. 432–435.
3. Волосовец А.П. Ацетонемический синдром у детей / А.П. Волосовец, С.П. Кривопустов, А.Н. Кожина, Е.Н. Щербинская // Здоровье ребенка. — 2009. — № 6 (21). — С. 17–19.
4. Георгиянц М.А. Недиабетические кетоацидозы в детском возрасте: клиника, диагностика и инфузионная терапия (методические рекомендации) / М.А. Георгиянц, В.А. Корсунов, Е.В. Шилова. — К., 2006. — 24 с.
5. Гордеев В.И. Педиатрическая анестезиология-реаниматология. Частные разделы / В.И. Гордеев, Ю.С. Александрович. — СПб., 2004. — 408 с.
6. Ершова И.Б. Особенности кишечного микробиоценоза при вирусных гепатитах и возможности его коррекции / И.Б. Ершова // Актуальна інфектологія. — 2014. — № 2. — С. 6–10.
7. Зрячкин Н.И. Особенности ацетонемического синдрома у детей / Н.И. Зрячкин, С.А. Хмилевская, Г.В. Зайцева [и др.] // Российский педиатрический журнал. — 2013. — № 3. — С. 22–26.
8. Казак С.С. Діагностика та дієтотерапія ацетонемічного синдрому у дітей / С.С. Казак, Г.В. Бекетова // Ліки України. — 2005. — № 1. — С. 83–86.
9. Курило Л.В. Первичный ацетонемический синдром у детей / Л.В. Курило // Medicus Amicus. — 2002. — № 5. — С. 4–7.
10. Оковитый С.В. Гепатопротекторы / С.В. Оковитый, Н.Н. Безбородкина, С.Г. Улейчик, С.Н. Шуленин. — М.: ГЭОТАР-Медиа, 2010. — 112 с.
11. Сенаторова А.С. Ацетонемический синдром у детей / А.С. Сенаторова, Е.В. Осипенко // Здоровье ребенка. — 2007. — № 5 (7). — С. 115–120.
12. Сорокулова И.Б. Рекомбинантные пробиотики: проблемы и перспективы использования для медицины и ветеринарии / И.Б. Сорокулова, В.А. Белявская, В.И. Масычева, В.В. Смирнов // Вестн. РАМН. — 1997. — № 3. — С. 46–49.
13. Сорокулова И.Б. Изучение безопасности и реактогенности нового пробиотика субалина для добровольцев / И.Б. Сорокулова // Микробиол. журн. — 1998. — Вып. 60, № 1. — С. 43–46.
14. Чудновская Н.В. Антивирусная активность пробиотиков из бацилл / Н.В. Чудновская, С.Л. Рыбалко, И.Б. Сорокулова [и др.] // Доповіді Національної академії наук України. — 1995. — № 2. — С. 124–126.

/72/72.jpg)