Журнал «Здоровье ребенка» 2 (61) 2015
Вернуться к номеру
Влияние персистирующих внутриклеточных инфекций на процессы ремоделирования дыхательных путей при бронхиальной астме у детей.
Авторы: Чернышева О.Е. — Донецкий национальный медицинский университет им. М. Горького, г. Красный Лиман
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
В статье представлены сведения о влиянии персистирующих внутриклеточных инфекций на процессы ремоделирования дыхательных путей при бронхиальной астме у детей. Описано влияние матричных металлопротеиназ, тканевого ингибитора матричных протеиназ, трансформирующего фактора роста, аутоантител к коллагену III типа, эндотелина-1 на процессы морфологической перестройки дыхательных путей в виде гипертрофии гладких мышц, усиленного образования новых сосудов, гиперплазии эпителиальных клеток, отложения коллагена, уплотнения базальной мембраны, наблюдаемые при бронхиальной астме у детей.
У статті представлені відомості про вплив персистуючих внутрішньоклітинних інфекцій на процеси ремоделювання дихальних шляхів при бронхіальній астмі в дітей. Описано вплив матричних металопротеїназ, тканинного інгібітору матричних протеїназ, трансформуючого фактора росту, аутоантитіл до колагену III типу, ендотеліну-1 на процеси морфологічної перебудови дихальних шляхів у вигляді гіпертрофії гладких м’язів, посиленого утворення нових судин, гіперплазії епітеліальних клітин, відкладення колагену, ущільнення базальної мембрани, що спостерігаються при бронхіальній астмі.
The article presents information about the impact of persistent intracellular infections on the processes of airway remodeling in bronchial asthma in children. The influence of matrix metalloproteinases, tissue inhibitor of matrix metalloproteinase, transforming growth factor, antibodies to type III collagen, endothelin-1 on the processes of morphological reconstruction of the airway by way of smooth muscle hypertrophy, enhanced neovascularization, epithelial cell hyperplasia, collagen deposition, thickening of the basal membrane, observed in bronchial asthma in children, were described.
ремоделирование дыхательных путей, персистирующие инфекции, бронхиальная астма.
ремоделювання дихальних шляхів, персистуючі інфекції, бронхіальна астма.
airway remodeling, persistent infections, bronchial asthma.
Статья опубликована на с. 77-82
На современном этапе бронхиальная астма остается одной их наиболее актуальных медико-социальных проблем педиатрии [1, 2]. Несмотря на многочисленные фундаментальные исследования механизмов патогенеза, разработки новых селективных лекарственных препаратов, создание специальных программ ВОЗ, в настоящее время не удается взять под контроль течение заболевания [3]. Одной из возможных причин этого является ремоделирование дыхательных путей.
В результате воспалительного процесса, развивающегося при бронхиальной астме под воздействием специфических и неспецифических факторов, особенно при тяжелом течении заболевания, происходят морфологические и функциональные изменения во всех структурах бронхов [4, 5]. Одной из причин развития ремоделирования дыхательных путей является вирусная инфекция [6, 7]. Согласно современным представлениям, ремоделирование развивается достаточно рано, в течение первого года персистирующего аллергического воспаления [2]. Развитие необратимых изменений возможно уже через четыре года после начала заболевания [8]. Согласно исследованиям Н. Nagai [9], эпителиальные клетки, базальная мембрана, гладкомышечные элементы, фибробласты и макрофаги являются основными участниками процесса ремоделирования дыхательных путей, возникающего вследствие хронического, длительно протекающего воспалительного процесса. В результате развиваются необратимые морфологические изменения в виде гипертрофии или гиперплазии гладкомышечных элементов, роста и формирования новых сосудов, десквамации эпителия дыхательных путей, гиперплазии бокаловидных клеток, а также накопления коллагена в зонах, расположенных ниже базальной мембраны [10, 11]. Глубокие трофические нарушения характеризуются гипертрофией гладких мышц, усиленным образованием новых сосудов, сопровождающимся застоем, гиперплазией и метаплазией бокаловидных эпителиальных клеток, увеличением подслизистых желез и отложением коллагена в lamina reticularis (уплотнение базальной мембраны), в результате чего происходит перестройка (ремоделирование) стенки бронхов [8, 12]. Со временем в стенке бронхов развивается диффузное хроническое воспаление, утолщение и склероз межальвеолярных перегородок, увеличивается гипертрофия мышц, воспаление мелких дыхательных путей, склероз, то есть происходит патологическое ремоделирование дыхательных путей [8].
Субэпителиальный фиброз возникает вследствие накопления в ретикулярной пластинке фрагментов экстрацеллюлярного матрикса, относящегося к протеингликанам, в частности различных видов коллагена, фибронектина, тенасцина [6]. Причем утолщенный слой базальной мембраны большей частью состоит из коллагена III, V типов [13].
Структурные изменения в дыхательных путях, свидетельствующие о ремоделировании, могут происходить в начале патологического процесса, когда на основании клинических данных еще не установлен диагноз бронхиальной астмы [14].
Несмотря на то что в последние годы достигнут определенный прогресс в выявлении основных закономерностей, определяющих ремоделирование дыхательных путей при бронхиальной астме, проблема остается нерешенной [8]. Отсутствуют исследования роли персистирующих внутриклеточных инфекций при процессах ремоделирования дыхательных путей у детей, а также возможности коррекции патологических изменений при помощи лекарственных средств.
Проблемной особенностью диагностики процессов воспаления и ремоделирования дыхательных путей при бронхиальной астме у детей является необходимость использования инвазивной волоконно-оптической бронхоскопии с биопсией. Поэтому рядом исследователей был проведен комплексный анализ корреляции между признаками воспаления и ремоделирования, выявленными при бронхоскопии, компьютерной томографии, изучении биоптата, и уровнем маркеров воспаления в мокроте и сыворотке крови при развитии ремоделирования и подтверждена равнозначность данных исследований [14, 16, 17].
Целью нашей работы стало определение влияния персистирующих внутриклеточных инфекций на процессы ремоделирования дыхательных путей при бронхиальной астме у детей.
Под нашим наблюдением находилось 328 детей в возрасте от 1 до 15 лет с персистирующей формой бронхиальной астмы. У всех пациентов определялся уровень иммуноглобулинов классов M и G в сыворотке крови, а также ДНК вируса простого герпеса І–ІІ типов, цитомегаловируса, вируса Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе в соскобе слизи со слизистой оболочки ротовой полости и мокроте. В результате полученных данных были выделены 2 группы обследуемых детей. Основную группу (I группа) составили 256 детей с бронхиальной астмой, инфицированных перечисленными внутриклеточными инфекциями, в группу сравнения (ІІ группа) вошли 72 ребенка с бронхиальной астмой, не инфицированные внутриклеточными инфекциями. Группу контроля составили 50 практически здоровых детей.
Активное течение инфекционного процесса, вызываемого внутриклеточными персистирующими возбудителями, определялось по наличию в соскобе со слизистой оболочки ротовой полости и мокроте ДНК возбудителей. По результатам исследования пациенты основной группы были разделены на 2 подгруппы — с активным течением инфекционного процесса, включающей 164 ребенка, и с латентным течением — 92 ребенка.
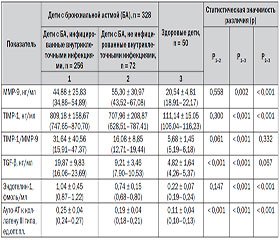
Сравнительным путем нами были изучены уровни различных медиаторов ремоделирования бронхов в сыворотке крови детей, больных бронхиальной астмой, инфицированных цитомегаловирусом, вирусом простого герпеса І–ІІ типов, вирусом Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе, при активном и латентном течении инфекционного процесса, а также у неинфицированных внутриклеточными возбудителями пациентов. В частности, определялись уровни фермента металлопротеиназы-9 (ММР-9), специфического тканевого ингибитора ММР-9 — TIMP-1, трансформирующего фактора роста b (TGF-b), эндотелина-1, аутоантител к коллагену III типа, рассчитывался индекс фиброзированияTIMP-1/ММР-9 (табл. 1, 2).
В результате исследования было выявлено, что уровень фермента эндопептидазы ММР-9 в сыворотке крови детей, как инфицированных (основная или І группа), так и не инфицированных внутриклеточными возбудителями (группа сравнения), был более чем в 2–2,5 раза выше, чем в группе практически здоровых детей. В группе детей, больных бронхиальной астмой и инфицированных внутриклеточными инфекциями, уровень ММР-9 составил 44,18 ± 25,83 нг/мл,
неинфицированных — 55,30 ± 30,97 нг/мл, что статистически значимо отличалось от показателя практически здоровых детей — 20,50 ± 5,44 нг/мл
(соответственно p = 0,002 и p < 0,001). Не было выявлено статистически значи–мого различия данного показателя у пациентов основной группы и группы сравнения, р = 0,558. В случае активного течения инфекции у пациентов I группы уровень ММР-9 был выше (56,74 ± 24,16 нг/мл),
чем при латентном инфекционном процессе (39,97 ± 21,59 нг/мл), статистическая разница была незначимой, р = 0,111. Не отмечалась статистическая разница показателя ММР-9 у детей с бронхиальной астмой с активным течением инфекционного внутриклеточного процесса и пациентов с бронхиальной астмой, не инфицированных внутриклеточными инфекциями (р = 0,999), а также у наблюдаемых пациентов с латентным течением инфекции и неинфицированных детей (р = 0,171).
Активность матричных металлопротеиназ является одной из значимых причин ремоделирования дыхательных путей. Металлопротеиназы способны гидролизировать все компоненты экстрацеллюлярного матрикса: коллагены, проколлагены, протеогликаны, эластин, фибронектин, ламинин, а также адгезивные и другие белки соединительной ткани. Кроме того, данные белки являются единственными протеолитическими ферментами, способными денатурировать фибриллярные коллагены [18, 19]. ММР-9 участвует в ангиогенезе дыхательных путей и способна активировать TGF-b1, приводящий к суб–эпителиальному фиброзу [20]. Выявлена противомикробная функция ММР-9, что свидетельствует не только о повреждающем действии данного фермента при бронхиальной астме, но и о возможной роли данной желатиназы В в профилактике обострений заболевания [21].
Полученные данные свидетельствуют о том, что повышение уровня сывороточной ММР-9 указывает на дефект гомеостаза экстрацеллюлярного матрикса даже у детей со стабильной, контролируемой астмой, что позволяет использовать данный показатель в качестве неинвазивного маркера воспаления и ремоделирования дыхательных путей при бронхиальной астме у детей.
В физиологических условиях металлопротеиназы секретируются в незначительных количествах и регулируются специфическими тканевыми ингибиторами металлопротеиназ (TIMP). Подавление ММР-9 происходит под действием тканевого ингибитора I типа — TIMP-1.
В ходе исследования было выявлено, что уровень тканевого ингибитора металлопротеиназ TIMP-1 в сыворотке крови детей, больных бронхиальной астмой, как инфицированных, так и не инфицированных внутриклеточными возбудителями, был более чем в 7 раз выше, чем в группе практически здоровых детей. Так, в группе детей, больных бронхиальной астмой и инфицированных внутриклеточными инфекциями, уровень TIMP-1 составил 809,18 ± 158,67 нг/мл, неинфицированных — 707,96 ± 208,87 нг/мл, что статистически значимо отличалось от показателя практически здоровых детей — 111,14 ± 15,05 нг/мл (p < 0,001). Статистически значимой разницы данного показателя у пациентов основной группы и группы сравнения выявлено не было, р = 0,300. При активном течении инфекции у пациентов I группы уровень TIMP-1 был выше (891,27 ± 207,86 нг/мл), чем при латентном инфекционном процессе (645,39 ± 210,33 нг/мл),
статистическая разница составила p < 0,001. Было выявлено статистически значимое различие данного показателя в основной группе детей при активном течении инфекции и детей группы сравнения, р = 0,004. При сравнении данного показателя при латентном течении инфекционного процесса у пациентов І группы и группы сравнения статистического различия выявлено не было (р = 0,758).
Повышение уровня тканевого ингибитора металлопротеиназ TIMP-1 свидетельствует об определенном контроле и регулировании чрезмерной активности ММР-9. Избыток тканевого ингибитора металлопротеиназ-1 в сыворотке крови больных бронхиальной астмой связан с хронической бронхиальной обструкцией [22].
Вследствие таких изменений происходит усугубление процессов ремоделирования дыхательных путей. Поэтому важное значение имеет определение уровня соотношения ММР с ингибитором TIMP (TIMP-1/MMP-9) как маркера фиброза, склероза тканей, влияющего на толщину стенки дыхательных путей у пациентов с бронхиальной астмой вследствие нарушения баланса между синтезом и деградацией компонентов внеклеточного матрикса в пользу чрезмерной протеолитической активности [23]. Кроме того, дисбаланс между матриксными металлопротеиназами и их тканевыми ингибиторами лежит в основе патогенеза эмфизематозных изменений в легких, наблюдаемых у детей с бронхиальной астмой [18].
При обследовании детей, больных бронхиальной астмой, было выявлено, что индекс фиброзирования TIMP-1/ММР-9 в сыворотке крови детей, больных бронхиальной астмой и инфицированных внутриклеточными возбудителями, составил 31,64 ± 40,56 и статистически отличался (p < 0,001) от показателя в группе здоровых детей, в которой он составил 5,68 ± 1,45. В группе детей, больных бронхиальной астмой и не инфицированных внутриклеточными инфекциями, соотношение TIMP-1/ММР-9 составило 16,08 ± 8,85, что статистически значимо не отличалось от показателей основной группы пациентов (р = 0,061) и практически здоровых детей (р = 0,332). При активном и латентном течении инфекции у пациентов I группы индекс фиброзирования TIMP-1/ММР-9 был практически на одинаковом уровне и составил соответственно 18,74 ± 10,20 и 20,58 ± 12,82 (р = 0,998). Не было выявлено статистической разницы между названными показателями фиброзирования и их уровнем у пациентов группы сравнения (соответственно р = 0,992 и р = 0,942). Уменьшение мольного соотношения TIMP-1/ММР-9 свидетельствует о повреждении тканей, а избыток TIMP-1, приводящий к увеличению соотношения TIMP-1/ММР-9, отображает ремоделирование дыхательных путей вследствие хронического воспалительного процесса, возникающего при бронхиальной астме у детей, за счет субэпителиального осаждения коллагена [24]. Хронический, длительный дисбаланс TIMP-1/ММР-9 приводит к утолщению дыхательных путей и ограничению воздушного потока, что усугубляет течение бронхиальной астмы у детей [16, 24]. Гиперпродукция ММР-9 и TIMP-1, наблюдаемая при инфицировании дыхательных путей вирусом гриппа A H1N1/v, свидетельствовала об их подавляющем действии на возбудителя [25]. Таким образом, повышение уровня ММР-9 и TIMP-1 у детей с бронхиальной астмой, особенно инфицированных внутриклеточными возбудителями, при активном течении инфекционного процесса может быть также связано с их действием на процессы, способствующие инактивации внутриклеточных возбудителей.
Повышенная выработка металлопротеиназ приводит к освобождению и активации факторов роста, в частности профибротического трансформирующего фактора роста b-1 (TGFb-1) [16]. При изучении в ходе исследования уровня цитокина TGFb-1 в сыворотке крови детей, больных бронхиальной астмой, который рассматривается как иммунопатологическая молекула при заболеваниях, связанных с избыточным фиброзом [25], было выявлено повышение данного фактора роста как в основной группе детей, так и в группе сравнения. Так, в группе детей с бронхиальной астмой, инфицированных внутриклеточными возбудителями, уровень TGFb-1 был практически в 5 раз выше показателя здоровых детей (4,82 ± 1,64 нг/мл) и составил 19,87 ± 9,83 нг/мл,
p < 0,001. В группе детей, не инфицированных внутриклеточными инфекциями, уровень данного цитокина был в 2 раза выше, чем у здоровых детей, и составил 9,21 ± 3,46 нг/мл, однако статистическая разница при этом была р = 0,067. При определении уровня TGFb-1 в основной группе пациентов при активном и латентном течении внутриклеточных персистирующих инфекций, составившего соответственно 18,34 ± 7,82 нг/мл и 10,51 ± 3,34 нг/мл, было выявлено его статистически значимое различие (p < 0,001). Показатель содержания данного цитокина при активном течении инфекции у детей І группы значимо отличался от показателя группы сравнения (p < 0,001). В случае латентного течения инфекции у пациентов основной группы статистически значимого различия с показателями детей группы сравнения выявлено не было (р = 0,952).
Таким образом, повышенные концентрации TGFb-1 связаны с прогрессированием фиброза и ремоделированием дыхательных путей у пациентов с бронхиальной астмой. Инфицирование внутриклеточными инфекциями усугубляет этот процесс, особенно в случае активного течения инфекции.
Следует отметить, что противовоспалительная активность TGFb-1 проявляется в супрессии продукции провоспалительных цитокинов, ингибировании активности макрофагов и клеточного деления Т- и В-лимфоцитов и активизации пролиферации фибробластов. Поэтому гиперпродукция TGFb-1, особенно в основной группе детей, при активном течении инфекционного процесса, обусловлена снижением активации клеток иммунной системы, направленной на ограничение воспалительной реакции, что приводит к поддержанию хронического воспаления и замыкает круг патологических процессов, происходящих в дыхательных путях.
В связи с тем, что в легкие попадает значительное количество патогенов, в том числе и внутриклеточных персистирующих инфекционных агентов, происходит как активация механизмов врожденного иммунитета, так и развитие хронического воспаления, впоследствии приводящего к процессам фиброза, участие в которых принимает TGFb-1.
При бронхиальной астме наблюдаются изменения сосудов, включающие ангиогенез, расширение сосудов, микроваскулярную проницаемость, продукцию факторов роста, адгезию клеток, трансмиграцию и фильтрацию, увеличение кровотока вследствие расширения резистентных артерий и увеличения количества сосудов, коррелирующие со степенью тяжести заболевания [15]. Однако существуют биологически активные вещества, способные вызывать сужение сосудов. К ним относится эндотелин-1, который является наиболее мощным вазоконстриктором и продуцируется сосудистым эндотелием в дыхательных путях при бронхиальной астме под действием ФНО-a. Действие эндотелина-1 многогранно и заключается в способности вызывать бронхоконстрикцию, усиливать реакцию бронхов на ингалируемые антигены, увеличивать приток воспалительных клеток, продукцию цитокинов, участвовать в формировании отека и в процессах ремоделирования дыхательных путей, ускорять хемотаксис, адгезию и активацию нейтрофилов, стимулировать развитие фиброза субэпителиального слоя стенки бронхов и образование хемоаттрактанта для лейкоцитов [15]. Исследования некоторых авторов выявили увеличение выработки эндотелина-1 при воспалении, развивающемся при бронхиальной астме, его хронизации, повышении выраженности обструкции дыхательных путей под действием данного пептида [15].
При обследовании наблюдаемых нами детей было выявлено, что уровень эндотелина-1 был статистически значимо выше (p < 0,001) в сыворотке крови детей, больных бронхиальной астмой, как инфицированных (1,04 ± 0,45 фмоль/мл), так и неинфицированных внутриклеточными инфекциями (0,74 ± 0,15 фмоль/мл), по сравнению со здоровыми детьми (0,22 ± 0,07 фмоль/мл). Статистически значимого различия в показателях детей основной группы и группы сравнения выявлено не было (р = 0,147). При активном и латентном течении внутриклеточных персистирующих инфекций показатели эндотелина-1 были практически одинаковыми и составили соответственно 1,06 ± 0,52 фмоль/мл и 1,06 ± 0,71 фмоль/мл (р = 0,999).
Показателем, определяющим прогноз при бронхолегочной патологии у детей, является уровень аутоантител к коллагену ІІІ типа. В результате хронического воспаления, лежащего в основе ремоделирования дыхательных путей при бронхиальной астме, формируется субэндотелиальный фиброз вследствие нарушения обмена коллагена аутоиммунного характера. Уже на ранних стадиях воспаления можно выявить в интерстиции легких накопление всех типов коллагена с преобладанием коллагена III типа [26]. До настоящего времени не проводилось изучения уровня аутоантител к коллагену ІІІ типа в сыворотке крови у детей при бронхиальной астме. Данный иммунохимический тест имеет высокую информативность, диагностическую и прогностическую значимость, характеризует воспалительную реакцию на всех ее этапах, в том числе и на ранних, и свидетельствует о ремоделировании дыхательных путей, вызванном дезорганизацией коллагеновых волокон.
В ходе обследования детей с бронхиальной астмой было выявлено, что в основной группе детей и в группе сравнения отмечалось статистически значимое (p < 0,001) повышение уровня аутоантител к коллагену ІІІ типа, соответственно 0,25 ± 0,04 ед.опт.пл.
и 0,19 ± 0,04 ед.опт.пл., по сравнению с группой практически здоровых детей (0,11 ± 0,04 ед.опт.пл.). При этом статистическая разница (p < 0,001) отмечалась и среди пациентов из основной группы и группы сравнения, что указывает на влияние внутриклеточного инфицирования на усугубление субэпителиального фиброза у пациентов с бронхиальной астмой. Показатели при активном течении инфекционного процесса, составившие 0,25 ± 0,05 ед.опт.пл., и показатели, определяемые при латентном течении, 0,20 ± 0,03 ед.опт.пл., также были статистически различны (р = 0,005).
Повышение уровня аутоантител к коллагену ІІІ типа при бронхиальной астме у детей, протекающей на фоне различного течения инфекционного процесса, вызванного внутриклеточными возбудителями и без инфицирования, свидетельствует о –дезорганизации коллагеновых структур, особенно при активном течении инфекции.
Таким образом, в результате проведенных исследований были получены данные, свидетельствующие о влиянии персистирующих внутриклеточных инфекций, в частности цитомегаловирусной, вызванной вирусом простого герпеса І–ІІ типов, вирусом Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе, особенно при активном их течении, на процессы ремоделирования дыхательных путей при бронхиальной астме, что вызывает необходимость проведения наряду с базисной терапией этиопатогенетического лечения с целью уменьшения выраженности процессов ремоделирования дыхательных путей, снижения тяжести заболевания и снижения инвалидизации.
1. Беш Л.В. Нове в діагностиці і терапії бронхіальної астми у дітей: практичний підхід до трактування найсучасніших вітчизняних та міжнародних узгоджувальних документів // Здоров’я України. — 2014, лютий, тематичний номер. — С. 16-17.
2. Недельская С.Н., Ярцева Д.А. Диагностика бронхиальной астмы у детей раннего возраста: возможности, проблемные вопросы, дифференциальная діагностика // Здоровье ребенка. — 2013. — № 2 (45). — С. 26-32.
3. Уманець Т.Р. Клініко-анамнестичні особливості фенотипів бронхіальної астми у дітей // Перинаталогия и педиатрия. — 2011. — № 2 (46). — С. 69-71.
4. Бронхиальная астма: современные концепции диагностики и лечения. Научно-информационный материал. — М., 2011. — 127 с.
5. Fixman E.D., Stewart A., Martin J.G. Basic mechanisms of development of airway structural changes in asthma // Eur. Respir. J. — 2007. — Vol. 29. — P. 379-389.
6. Фисенко В., Чичкова Н. Ремоделирование при бронхиальной астме: принципы формирования и возможности фармакологического воздействия // Врач. — 2006. — № 12. — С. 14-20.
7. Gosens R., Zaagsma J., Grootte M. et al. Acetylcholine: a novel regulator of airway smooth muscle remodeling? // Eur. J. Pharmacol. — 2004. — Vol. 500. — P. 193-201.
8. Антипкін Ю.Г., Надточій Т.Г. Сучасні погляди на етіопатогенез, клініко-діагностичні та лікувально-профілактичні особливості перебігу запального процесу при неспецифічних захворюваннях органів дихання у дітей (огляд літератури) // Перинаталогия и педиатрия. — 2011. — № 1 (45). — С. 19-23.
9. Nagai H. Immunopharmacological approach to elucidating the mechanism of allergic inflammation // Allerg. Inter. — 2005. — Vol. 54. — P. 251-261.
10. Jeffery P.K. Remodeling and inflammation of bronchi in asthma and chronic obstructive pulmonary disease // Proc. Am. Thorac. Soc. — 2004. — Vol. 1. — P. 176-183.
11. Kanazawa H. Anticholinergic agents in asthma: chronic bronchodilator therapy, relief of acute severe asthma, reduction of chronic viral inflammation and prevention of airway remodeling // Curr. Opin. Pulm. Med. — 2006. — Vol. 12. — P. 60-67.
12. Ласиця О.Л., Охотнікова О.М. Діагностика, лікування і профілактика бронхіальної астми у дітей. — К., 2006. —
С. 4-24.
13. Балаболкин И.И., Смирнов И.Е., Булгакова В.А., Горюнов А.В., Ларькова И.А. Современная концепция патогенеза бронхиальной астмы у детей // Иммунопатология, аллергология, инфектология. — 2006. — № 1. — С. 26-35.
14. Pohunek P. Pediatric asthma: how significant it is for the whole life? // Paediatr. Respir. Rev. — 2006. — № 7. — Р. 68-69.
15. Ненартович И.А., Жерносек В.Ф. Ремоделирование бронхов при бронхиальной астме и возможности его коррекции // Рецепт. — 2010. — № 3 (71). — С. 77-89.
16. Doğu F., Yildiran A., Loğlu D. Serum transforming growth factor-b (TGF-b), matrix metalloproteinase-2 (MMP-2), matrix metalloproteinase-9 (MMP-9) and tissue inhibitors of metalloproteinase (TIMP-1) levels in childhood asthma // Turk. J. Med. Sci. — 2008. — № 38 (5). — Р. 415-419.
17. Matsumoto H., Niimi A., Takemura M., Ueda T., Minakuchi M., Tabuena R. et al. Relationship of airway wall thickening to an imbalance between matrix metalloproteinase-9 and its inhibitor in asthma // Thorax. — 2005. — № 60. — Р. 277-81.
18. Невзорова В.А., Тилик Т.В., Гилифанов Е.А., Панченко Е.А., Вахрушева С.Е., Тилик В.В. Роль матриксных металлопротеиназ в формировании морфофункционального дисбаланса воздухоносных путей при хронической обструктивной болезни легких // Тихоокеанский медицинский журнал — 2011. — № 2. — С. 9-13.
19. Oikonomidi S., Kostikas K., Tsilioni I. et al. Matrix metalloproteinases in respiratory diseases: from pathogenesis to potential clinical implications // Cur. Med. Chem. — 2009. — Vol. 16, № 10. — Р. 1214-1228.
20. Kraus-Filarska M., Kosinska M., Tomcowicz A. Metalloproteinases and airway remodeling in asthma // Adv. Clin. Exp. Med. — 2007. — Vol. 16, № 3. — Р. 417-423.
21. Todorova L., Bjermer L., Miller-Larsson A. Relationship between matrix production by bronchial fibroblasts and lung function and AHR in asthma // Journal article. — 2010. — Vol. 104, № 12. — P. 1799-1808.
22. Hegazy L., Salwa Abu El Hana. Circulating MMP-9 and TIMP-1 in acute exacerbations and after remission induced by oral corticosteroids in asthmatic children // Egypt. J. Pediatr. Allergy Immunol. — 2006. — № 4 (1). — Р. 23-29.
23. Рукина Д.А., Догадова Л.П., Маркелова Е.В., Абдуллин Е.А., Осыховский А.Л., Хохлова А.С. Иммунологические аспекты патогенеза первичной открытоугольной глаукомы // Русский медицинский журнал. — 2011. — № 4. — С. 162-164.
24. Doherty G.M., Kamath S.V., Courcey F., Christie S.N., Chisakuta A., Lyons J.D. Children with stable asthma have reduced airway matrix metalloproteinase-9 and matrix metalloproteinase-9/tissue inhibitor of metalloproteinase-1 ratio // Clin. Exp. Allergy. — 2005. — № 35 (9). — Р. 1168-74.
25. Мироманова Н.А., Жамсуева Д.Р. Значение матриксных металлопротеиназ и трансформирующего фактора роста b1 в развитии осложненных форм гриппа у детей // Врач-аспирант. — 2013. — № 5 (60). — С. 16-22.
26. Стройкова Т.Р. Клинико-диагностическое значение аутоантител к коллагену III типа при бронхолегочных заболеваниях у детей: Автореферат дис… канд. мед. наук. — Астрахань, 2009. — 20 с.

/79.jpg)