Журнал «Здоровье ребенка» 2 (61) 2015
Вернуться к номеру
Патогенетическое обоснование выбора муколитических средств полинаправленного действия при лечении заболеваний органов дыхания у детей.
Авторы: Чернышева О.Е. — Донецкий национальный медицинский университет им. М. Горького, г. Красный Лиман
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
Нарушения мукоцилиарного транспорта сопровождают любое поражение органов дыхания. В работе представлены механизмы патогенеза развивающихся при этом изменений и их последствия. Рассмотрены методы восстановления процессов очищения дыхательных путей на фоне использования муколитика комплексного воздействия ацетилцистеина.
Порушення мукоциліарного транспорту супроводжує будь-яке ураження органів дихання. У роботі представлені механізми патогенезу змін, що розвиваються при цьому, і їх наслідків. Розглянуто методи відновлення процесів очищення дихальних шляхів на фоні використання муколітика комплексної дії ацетилцистеїну.
Violations of mucociliary clearance accompany any damage of the respiratory system. The paper presents the pathogenetic mechanisms of changes developing at this time and their consequences. The methods to recover airway clearance processes on the background of using acetylcysteine, mucolytic with complex effects, were considered.
дети, болезни органов дыхания, муколитические средства.
діти, хвороби органів дихання, муколітичні засоби.
children, respiratory diseases, mucolytics.
Статья опубликована на с. 99-104
Болезни органов дыхания являются одной из наиболее важных проблем в педиатрии, занимая первое место в структуре детской заболеваемости. К числу основных факторов патогенеза респираторных заболеваний относится нарушение механизмов мукоцилиарного транспорта, что чаще всего связано с избыточным образованием и/или повышением вязкости секрета в дыхательных путях. Причем на всем их протяжении, независимо от генеза патологического процесса (инфекционного, аллергического, ирритативного) и места поражения (легкие, бронхи, трахея, гортань, носоглотка), основными клиническими проявлениями являются нарушения образования и выделения мокроты и синдром кашля.
Во время вдоха воздух, проходя через дыхательные пути, согревается, увлажняется и очищается. Инородные частицы и микроорганизмы, поступающие с вдыхаемым воздухом, осаждаются на слизистых респираторного тракта и в дальнейшем, благодаря содружественной работе реснитчатого аппарата мерцательного эпителия слизистых и перистальтических движений бронхов, выводятся вместе с образующимся бронхиальным секретом (БС). Его образование и продвижение в проксимальном направлении от альвеол к бронхам является одним из важнейших, наряду с дыханием, защитным физиологическим процессом в респираторной системе человека.
У детей даже раннего возраста система очищения легких функционирует достаточно хорошо. Местом образования БС являются бронхиальные железы, бокаловидные клетки, секреторные клетки Клара, эпителий бронхиол и альвеол. Количество клеток, вырабатывающих БС, увеличивается в направлении от альвеол к трахее. БС не только механически защищает слизистую дыхательных путей от микроорганизмов, но и сам оказывает бактериостатическое и бактерицидное действие благодаря своему составу — макрофагам, лизоциму, секреторному иммуноглобулину А и др.
БС представляет собой сложную систему, хотя на 95 % состоит из воды. Кроме того, в его состав входят клеточные элементы (цилиарный эпителий, макрофаги и др.), органические соединения и микроэлементы, являющиеся продуктом синтеза клеток респираторного эпителия, бронхиальных желез и факторов плазмы крови. Вязкость БС определяется соотношением двух фаз: наружного слоя — геля (плотного и нерастворимого) и внутреннего — золя (жидкого и растворимого). Золь — это секрет желез, капиллярный транссудат, межклеточная жидкость. Он находится под более плотным слоем геля и напоминает по вязкости плазму. Золь продуцируется в бронхиолах и альвеолах и содержит биологически активные вещества, ферменты, иммуноглобулины, что обусловливает мощную биологическую защитную функцию слизи. Именно в этом слое реснички мерцательного эпителия совершают свои колебательные движения и передают кинетическую энергию наружному слою трахеобронхиального секрета. Кроме этого, благодаря постоянному движению ресничек существенно укорачивается продолжительность контакта микроорганизмов с клетками слизистых оболочек дыхательных путей и, следовательно, значительно затрудняется проникновение возбудителей в трахеобронхиальный эпителий.
Гель — это вязкий поверхностный слой слизистой бронхов, располагающийся на ресничках мерцательного эпителия в виде непрерывной подвижной пленки, в состав которого входят гликопротеины, альбумин, лизоцим, альфа-1-антитрипсин, IgA, сурфактант, комплекс липидов. Гель формируется в результате смешивания золя с секретами бокаловидных и серомукоидных клеток. Перемещение геля, содержащего комочки слизи, осевшие микроорганизмы, чужеродные частицы, становится возможным только после разрыва поперечных ди–сульфидных связей между гликопротеинами.
Процесс физиологического очищения дыхательных путей называется мукоцилиарным клиренсом (МЦК). У здоровых детей мукоцилиарный клиренс является основным механизмом очищения трахео–бронхиального дерева. Процесс образования секрета и его выведения является одной из защитных функций органов дыхания. В клинической практике для обозначения трахеобронхиального секрета обычно пользуются термином «мокрота».
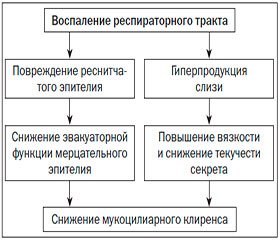
Одним из ведущих факторов патогенеза воспаления при заболеваниях бронхиального дерева является нарушение образования и эвакуации трахеобронхиального секрета и, как следствие, дезорганизация функции системы самоочищения бронхов [1]. Воспаление трахеи и бронхов в первую очередь сопровождается компенсаторным увеличением слизеобразования с гиперсекрецией в поврежденных бронхах, что определяется морфологическими и воспалительными изменениями в трахеобронхиальном дереве. При воспалении дыхательных путей развивается гиперемия бронхов, увеличивается количество бокаловидных клеток, продуцирующих более густой и вязкий секрет, обволакивающий реснитчатый аппарат эпителия, что значимо нарушает его двигательную функцию, а значит, и МЦК. Имеет место не только нарушение реологических свойств трахеобронхиальной слизи, но и развитие структурных изменений клеток мерцательного эпителия в виде повреждения ультраструктуры ресничек, нарушения их пространственной ориентации, деструкции клеточных органелл и др. Причем повышение вязкости мокроты происходит как при избыточном ее образовании, так и при недостаточном.
Одновременно с гиперпродукцией слизи изменяется и состав трахеобронхиального секрета: в нем уменьшается удельный вес воды и повышается концентрация муцинов (нейтральных и кислых гликопротеинов). Это приводит к увеличению вязкости мокроты (рис. 1).
В результате замедления МЦК страдает вентиляционно-респираторная функция легких и на фоне снижения мукоцилиарного транспорта нарастает колонизация бронхов патогенной микрофлорой — развивается вторичный инфекционный воспалительный процесс. Более того, получены многочисленные данные о формировании в дыхательных путях при нарушениях МЦК мощных генераций существования микробов — микробных биологических пленок, значимо ухудшающих течение инфекционных, в т.ч. респираторных, заболеваний и затрудняющих проведение антибактериального лечения. Предполагается, что более 65 % всех инфекционных заболеваний органов дыхания обусловлены колониями микроорганизмов, существующими в форме биопленок [2].
Микробные биопленки состоят из агрегатов микроорганизмов, окруженных образованным в ходе их метаболизма защитным матриксом и фиксированных к поверхностям респираторного тракта. Данный конгломерат является защитой колоний микроорганизмов, входящих в состав биопленки, от неблагоприятных и вредных для них физических, химических и биологических воздействий, в т.ч. и от антибактериальных средств. То есть биопленка является защитной формой существования микроорганизмов, повышающей их устойчивость к факторам внешней среды, т.е. к системам адаптации человека. Вне сомнения, нарушение бронхолегочного дренажа, задержка густой мокроты в нижних дыхательных путях способствуют образованию микробных биопленок, содержащих в своем составе микроорганизмы с измененными свойствами и со сформированной повышенной резистентностью к действию антибиотиков, что повышает риск осложнений течения респираторных заболеваний и сужает спектр эффективности лекарственных средств [3].
Ухудшению течения патологического процесса при респираторных заболеваниях на фоне снижения МЦК способствует повышение активности реакций перекисного окисления с повышением в мокроте уровня свободных радикалов [4]. В связи с этим развитие оксидативного (окислительного) стресса при воспалении усугубляет патогенетические нарушения при воспалительных заболеваниях легких. Поэтому недостаточность антиоксидантной защиты является одной из причин прогрессирования воспалительного процесса в бронхах и легких, так как развившийся при воспалении оксидативный стресс обусловливает избыточное образование в паренхиме легких О–2, ОН–, Н2О2 и др., что вызывает повышенное сокращение гладкомышечных волокон, ухудшает функционирование адренергических рецепторов. В результате оксидативного стресса развивается лизис клеток, повышается проницаемость альвеолярного эпителия, а в строме легких происходит снижение синтеза эластина и коллагена. Кроме того, увеличивается продукция провоспалительных цитокинов.
Еще один механизм патологического воздействия дезорганизации мокроты с нарушением ее дренажа — уменьшение продукции лимфоидными и макрофагальными клетками защитных и иммунных факторов (лизоцим, интерфероны, секреторный IgA), а также глутатиона, играющего важнейшую роль в детоксикационной активности клеточного аппарата слизистых оболочек [5].
Таким образом, нарушение продукции БС, его дезорганизация и сгущение с нарушением транспорта не только приводит к ухудшению дыхательных функций и вентиляционных способностей легких, но и включает в себя другие механизмы патологического процесса:
— поддержание и прогрессирование бронхолегочного воспаления;
— усиление адгезии микробных, токсических и других патогенных агентов к слизистым дыхательных путей;
— колонизацию бронхов патогенной микрофлорой с формированием микробных биологических пленок с защитным матриксом, препятствующим воздействию антибактериальных средств, что способствует развитию вторичного инфекционного воспалительного процесса в органах дыхания;
— повышение активности окислительных реакций перекисного окисления с повышением в мокроте уровня свободных радикалов, определяющих усиление воспалительного процесса;
— угнетение продукции лимфоидными и макрофагальными клетками защитных и иммунных факторов (лизоцим, интерфероны, секреторный IgA и др.);
— резкое снижение секреции лимфоидными клетками глутатиона, играющего важнейшую роль в детоксикационной активности клеточного аппарата слизистых оболочек и в формировании местной иммунной защиты.
В результате нарушения дренажной функции легких рефлекторно возникает кашель, однако в отличие от мукоцилиарного клиренса кашель имеет вспомогательное значение в очищении трахеобронхиального дерева и при развитии патологического процесса сгущения и дезорганизации мокроты перестает выполнять физиологическую функцию защиты дыхательных путей.
Таким образом, многообразие патологических механизмов требует комбинированного многонаправленного действия муколитического средства.
Сегодня среди муколитиков наиболее широкое применение получили синтетические препараты: ацетилцистеин (АЦ), амброксол, карбоцистеин. Однако следует отметить, что из указанных препаратов только АЦ обладает не только прямым муколитическим действием, но и возможностью коррекции других патологических воздействий, развивающихся при нарушениях продукции, дезорганизации, сгущении мокроты и угнетении МЦК.
АЦ является производным L-цистеина, только в молекуле которого содержатся свободные сульфгидрильные группы, способные разрывать дисульфидные связи кислых мукополисахаридов мокроты. Это приводит к деполимеризации макромолекул мукопротеидов БС и, соответственно, к снижению его вязкости и уменьшению адгезивных свойств. Таким образом, АЦ улучшает отхождение мокроты за счет прямого воздействия на реологические свойства секрета. Важной для практического использования особенностью АЦ является сохранение его муколитических свойств при любом виде мокроты — слизистой, слизисто-гнойной и гнойной.
Под влиянием АЦ увеличивается и скорость мукоцилиарного клиренса. Данный эффект позволяет говорить об АЦ не только как о муколитике, но и как о мукокинетике. Кроме того, в результате действия АЦ потенцируется секреция бокаловидными клетками менее вязких сиаломуцинов, увеличивается содержание золя. Это способствует восстановлению функции мерцательного эпителия, который уже самостоятельно может элиминировать слизь из дыхательных путей. Таким образом, АЦ оказывает и мукорегуляторное действие [6, 7]. В табл. 1 представлены различные механизмы действия наиболее часто применяемых муколитиков [8].
При применении АЦ отмечается уменьшение деструктивных процессов в цилиарном эпителии бронхиального дерева, поврежденном на фоне воспалительного процесса, и восстановление секреторной способности пораженных бокаловидных клеток бронхов. Это, как и быстрое наступление эффекта, связано с прямым муколитическим действием АЦ, отличающего его от других муколитиков [9].
В последние годы появились работы, в которых показана способность АЦ снижать образование микробных биопленок, а также разрушать их уже зрелые генерации. Указанный эффект связывают с влиянием АЦ, как антиоксиданта, на метаболизм клеток бактерий и продукцию экзополисахаридов — главного компонента матрикса биопленки. АЦ может непосредственно разрушать дисульфидные связи энзимов бактерий, участвующих в их образовании или экскреции [6].
В исследованиях также показано, что АЦ способен угнетать рост многих микробов — Staphylococcus aureus, Pseudomonas aeruginosa, Klebsiella pneumonia, Enterobacter spp. и др. При этом АЦ более активен, чем амброксол и карбоцистеин. Так, например, активность в плане уменьшения жизнеспособности Staphylococcus aureus у АЦ в 6–7 раз выше, чем у амброксола и бромгексина [7]. Кроме того, выявлена способность АЦ ингибировать процессы адгезии вирусов и бактерий к слизистым дыхательных –путей.
Антибактериальное действие связывают с конкурентным угнетением утилизации аминокислоты цистеина бактериями и способностью сульфгидрильных групп АЦ к деструкции белков, входящих в состав микроорганизмов. Показано, что сочетанное назначение антибиотиков и АЦ увеличивает их антибактериальное действие. В эксперименте подобный эффект доказан для таких антибиотиков, как ципрофлоксацин, рифампицин, карбенициллин, гентамицин и др. [10].
Сегодня выявлено еще одно очень важное свойство АЦ — антиоксидантная и антитоксическая активность [11]. В экспериментах доказано, что АЦ снижает повреждающее действие практически всех факторов оксидативного стресса. Определено, что молекула АЦ, имеющая свободную SH-группу, при контакте с бронхиальным секретом блокирует свободные радикалы, образующиеся в мокроте. Это способствует нейтрализации токсинов и восстановлению эпителия бронхиального дерева, а также нормализации деятельности его секреторных функций. Именно антиоксидантной активностью АЦ в сочетании со способностью L-цистеина активизировать лейкоциты и лимфоциты объясняется его значимый противовоспалительный эффект. Антиоксидантным действием АЦ объясняют и его способность предотвращать обострение хронического воспалительного процесса в легких [12, 13].
АЦ оказывает как прямой, так и непрямой антиоксидантный эффект. Прямое антиоксидантное действие АЦ связано, как говорилось выше, с наличием в его молекуле свободной тиоловой сульфгидрильной группы, которая легко отдает водород, нейтрализуя окислительные радикалы. Непрямое обусловлено тем, что АЦ является предшественником трипептида глутатиона — основного фактора защиты от воздействия токсических внутренних и внешних агентов. Синтез глутатиона обусловлен наличием цистеина, составляющего АЦ. Назначение больному АЦ обеспечивает поступление цистеина для поддержания необходимого уровня глутатиона в организме.
Изучение действия АЦ в клинике показало его способность тормозить продукцию эозинофильно-катионного протеина, лактоферрина, антихимотрипсина, а также восстанавливать нормальную клеточность бронхоальвеолярной жидкости [14].
Недавно обнаружены иммуномодулирующие свойства АЦ. В частности, препарат стимулирует образование колоний Т-клеток [15]. Выявлено, что назначение ацетилцистеина предотвращает уменьшение количества CD4+ Т-клеток.
Доказано влияние АЦ на синтез сурфактанта [16].
АЦ является формой цистеина, в большом количестве содержащегося в соевых бобах и животных белках (молочных продуктах, яйцах, мясе птицы, рыбе). Этим объясняется высокая безопасность препаратов АЦ. Безопасность назначения АЦ доказана в метаанализе 39 исследований, проведенных в период с 1976 по 1994 год, в которых не обнаружено различий между АЦ и плацебо по частоте нежелательных явлений со стороны желудочно-кишечного тракта [21]. В последующих 20 исследованиях, число участников которых составило 1080, эффективность и безопасность применения АЦ были оценены с использованием клинических, биологических, радиографических параметров, а также результатов исследования функции легких. Биологические тесты включали полный анализ крови (уровень гемоглобина, количество эритроцитов, количество лейкоцитов и тромбоцитов) и мониторинг функции печени (билирубин, сывороточная глутаматпируваттрансаминаза, щелочная фосфатаза) и почек (креатинин). Все контролируемые исследования показали высокую клиническую эффективность и безопасность использования АЦ [3].
Применение препарата в самом начале заболевания, в его первые сутки, когда значимо увеличивается количество слизи, нарушается ее состав, консистенция и замедляется МЦК, предотвращает не только мукостаз, но и развитие оксидантного стресса. Кроме того, назначение АЦ в первые часы респираторного заболевания способствует раннему восстановлению синтеза глутатиона и иммунных факторов — IgA, интерферонов, лизоцима. Быстрое начало лечения АЦ облегчает отделение секрета, устраняет формирование бронхиальной обструкции, уменьшает вероятность микробной колонизации дыхательных путей, исключая дальнейшие бактериальные осложнения. При этом реологические свойства мокроты улучшаются уже с первого дня применения АЦ, достигая через трое суток максимума, что способствует ее эффективному отхождению и восстановлению дренажной функции даже мельчайших бронхов. Это подтверждается данными проведенных исследований функции внешнего дыхания у больных с бронхитами, получавших АЦ [22]. Таким образом, целесообразно назначение АЦ в начале респираторного заболевания, как мощного антиоксиданта и как средства, быстро восстанавливающего мукоцилиарный транспорт и адекватность кашля — от непродуктивного до эффективного откашливания. Это сокращает сроки болезни на несколько дней.
Комбинация АЦ с антибиотиками способствует достоверному уменьшению длительности заболевания при бактериальных инфекциях органов дыхания [23]. Кроме того, свойство АЦ уменьшать явления оксидативного стресса определяет антипиретический эффект препарата, что обусловливает использование жаропонижающих средств не ранее чем через 1,5–2 часа после его приема.
Следует подчеркнуть, что на фоне значимого муколитического эффекта АЦ и улучшения дренажной способности дыхательной системы не увеличивается объем мокроты. При этом на фоне снижения вязкости бронхиального секрета отмечался лизис сгустков слизи и «расплавление» сухих корочек в бронхах. Кроме того, получены данные о стимулирующем действии АЦ на клетки, продуцирующие секрет с фибринолитическими свойствами.
На рынке есть множество форм и производителей АЦ, например европейский препарат АЦЦ®. АЦЦ® выпускается в виде порошка для приготовления орального раствора, шипучих таблеток по 100 и 200 мг для приема 2–3 раза в день, шипучих таблеток по 600 мг для однократного приема в сутки (АЦЦ® Лонг), порошка для приготовления горячего раствора 600 и 200 мг и готового для применения раствора, содержащего ацетилцистеин в дозе 20 мг/мл.
Препарат назначается в следующих дозировках:
АЦЦ 100/200 мг порошок для приготовления орального раствора:
— взрослым и детям старше 14 лет назначают по 400–600 мг ацетилцистеина в сутки в 1–3 приема;
— детям от 6 до 14 лет назначают по 400–600 мг в сутки, разделенные на 2–3 приема;
— детям от 2 до 6 лет — по 200–400 мг в сутки, разделенные на 2 приема.
АЦЦ 200/600 горячий напиток:
— взрослым и детям старше 14 лет назначают по 400–600 мг ацетилцистеина в сутки в 1–3 приема;
— детям в возрасте от 6 до 14 лет — по 400–600 мг в сутки, разделенные на 2–3 приема;
— детям в возрасте от 2 до 6 лет — по 200–400 мг в сутки, разделенные на 2 приема.
АЦЦ оральный раствор:
— взрослым и детям старше 12 лет — по 10 мл раствора 2–3 раза в сутки (эквивалент 400–600 мг ацетилцистеина в сутки);
— детям в возрасте от 2 до 6 лет — по 5 мл раствора 2–3 раза в сутки (эквивалент 200–300 мг ацетилцистеина в сутки);
— детям в возрасте от 6 до 12 лет — по 10 мл раствора 2–3 раза в сутки (эквивалент 400–600 мг ацетилцистеина в сутки).
10 мл орального раствора соответствуют половине мерного колпачка или 2 шприцам.
Методика назначения АЦ. Препарат принимается после еды, через 2 часа после антипиретиков и не позднее 18 часов. Содержимое пакетика или таблетку АЦ растворяют в 1/2 стакана воды, сока или холодного чая. Через 30–40 минут после приема рекомендуется обязательная активизация дренажных функций бронхиального дерева: дыхательная гимнастика, физические упражнения, массаж, в т.ч. перкуссионный, смена положения тела и т.д. При назначении АЦ следует увеличить питьевой режим. Нельзя применять муколитики непосредственно перед сном и без активизации дренажа бронхиального дерева, так как возможно наступление так называемого заболачивания бронхов. Выполнение рекомендуемых методов использования АЦ исключает возможные осложнения применения препарата при его высоком терапевтическом эффекте.
При острых неосложненных заболеваниях продолжительность применения препарата обычно составляет 4–5 дней. Лечение при хронических заболеваниях проводят длительное время или курсами по несколько месяцев (до 6 мес.).
Таким образом, АЦ является эффективным и безопасным препаратом для лечения инфекций как верхних, так и нижних дыхательных путей, заболеваний, протекающих с нарушениями дренажных функций системы дыхания. Его высокая эффективность обусловлена достаточно редкой комбинацией механизмов воздействия на воспалительный процесс. В пульмонологии АЦ может применяться как при острых заболеваниях — пневмониях, острых бронхитах, так и при хронических — хронических бронхитах, бронхоэктатической болезни, муковисцидозе и многих других заболеваниях органов дыхания детей и взрослых.
1. Батагов С.Я. Ацетилцистеин в лечении инфекций нижних дыхательных путей у взрослых // Лечащий врач. — 2014. — № 10.
2. Охотникова Е.Н. Современные возможности комплексного воздействия мукоактивной терапии бронхообструктивного синдрома у детей // Здоровье Украины. — 2014. — С. 33-35.
3. Duijvestijn Y.C.M., Mourdi N.. Smuchny J. et al. Acetylcysteine and carbocysteine for acute upper and low respiratory tract infections in paediatric patients without chronic broncho-pulmonary disease (Review) // Cochrane Database Syst. Rev. — 2010. — Vol. 9. — P. 1-22.
4. Kupczyk M., Kuna P. Mucolytics in acute and chronic respiratory tract disorders. II. Use for treatment and antioxidant properties // Pol. Merkuriusz Lek. — 2002. — 12 (69). — 248-52.
5. Beeh K.M., Beier J., Esperester A., Paul L.D. Antiinflammatory properties of ambroxol // Eur. J. Med. Res. — 2008. — Vol. 13 (12), № 3. — P. 557-562.
6. Новикова Л., Баранова О., Илькович Ю. Применение ацетилцистеина в клинической пульмонологии // Врач. — 2014. — 2. — 13-16.
7. Симонова О.И. Муколитики для детей: сложные вопросы, важные ответы // Вопросы современной педиатрии. — 2014. — 13 (1). — 26-32.
8. Симонова О.И., Горинова О.И. Применение ацетилцистеина для лечения респираторных заболеваний у детей младшего возраста // Фарматека. — 2014. — № 1.
9. Речкина Е.А. Современный взгляд на выбор противокашлевого препарата // Здоровье Украины. — 2014. — № 3.
10. Ушкалова Е. N-ацетилцистеин в лечении инфекций, связанных с образованием биопленок // Врач. — 2013. — 11. — 33-36.
11. Dove M.S., Dockery D.W., Connolly G.N. Smoke-free air laws and asthma prevalence, symptoms, and severity among nonsmoking youth // Pediatrics. — 2011. — № 127 (1). — Р. 102-109.
12. Zhao T., Liu Y. N-acetylcysteinein hibitbiofilms produced by Pseudomonasaeruginosa // BMC Microbiol. — 2010. — Vol. 10 (1). — P. 140.
13. Pintucci J.P., Corno S., Garotta M. Biofilms and infections of theupper respiratory tract // Eur. Rev. Med. Pharmacol. Sci. — 2010. — Vol. 14 (8). — P. 683-690.
14. Гембицкая Т., Череменский А. Ацетилцистеин в терапии хронической обструктивной болезни легких // Врач. — 2013. — 2. — 37-40.
15. Samuni Y., Goldstein S., Dean О., Berk М. The chemistry and biological activities of N-acetylcysteine // Biochimica et Biophysica Acta. — 2013. — 1830. — 4117-29.
16. Геппе Н.А., Снегоцкая М.Н., Никитенко А.А. Ацетилцистеин в лечении кашля у детей // Педиатрия. Приложение Сonsilium medicum. — 2007. — № 2. — С. 43-472.
17. Kadota J., Mizunoe S., Kishi K., et al. Antibiotic-induced apoptosis in human activated peripheral lymphocytes. // Int. J. Antimicrob. Agents. — 2005. — V. 25, № 3. — Р. 216-20.
18. Chalumeau M., Cheron G. Assathiany R., Moulin F. et al. Mucolytic agents for acute respiratory tract infections in infants: pharmacoepidemiologic problem? // Arch. Pediatrie. — 2002. — Vol. 9. — P. 1128-1136.
19. Намазова-Баранова Л.С., Давыдова И.В. Ацетилцистеин в педиатрической практике // РМЖ. — 2013. — № 25. — С. 1233-1236.
20. Симонова О.И. Особенности применения и эффективность N-ацетилцистеина при респираторной патологии у детей // Врач. — 2010. — № 2. — С. 56-61.
21. Stey C. et al. The effect of oral N-Acetylcysteine in chronic bronchitis: a guantitative systematic review // Eur. Respir. J. — 2000. — 16. — 253-262.
22. Кахновский И.М. Муколитическое действие ацетилцистеина // Аптека. — 2000. — № 265.
23. Локшина Э.Э., Зайцева С.В., Зайцева О.В. Новые возможности муколитической терапии у детей с острыми респираторными заболеваниями // Вопр. практ. педиатрии. — 2011. — 6 (1). — 67-72.

/100.jpg)
/102.jpg)