Статья опубликована на с. 51-59
Вступ
Деформації великого вертлюга (ДВВ) у дітей є одним із синдромологічних проявів (синдромів) основного захворювання кульшового суглоба (КС) (уроджений вивих (УВ) та підвивих стегна (ПВС)), деформації проксимального відділу стегнової кістки (ПВСК) внаслідок травм та запальних захворювань КС (сепсис, гнійний артрит тощо), coxа vara (CV), асептичний некроз головки стегнової кістки (АН ГСК) тощо) [1–3].
Маємо зазначити, що ДВВ розвиваються поступово й на початкових етапах не супроводжуються вираженими клінічними змінами (при незначній деформації відсутнє обмеження рухів у КС, кульгання та больовий синдром). Однак виражені ДВВ (у першу чергу його високе розташування) супроводжуються не тільки болем і обмеженням рухів у КС, але й певними рентгенологічними, біомеханічними та електроміографічними змінами — інсуфіцієнтністю сідничних м’язів, зміною силових зусиль з перевантаженням певних зон кульшової западини і ГСК та створенням біомеханічних передумов для розвинення децентрації та підвивиху стегна [4, 5].
Існуючі на даний час методи діагностики цієї патології спрямовані в першу чергу на фіксацію рентгенологічних змін у вертлюжному компоненті КС та не враховують дані біомеханічних та електроміографічних даних, а отже, не дають всеосяжної інформації, через що не завжди є змога об’єктивно оцінити анатомо-функціональний стан КС у до- та післяопераційному періоді [6–8].
Окрім методів променевої діагностики, для визначення ступеня функціональної спроможності м’язів КС, особливостей та розподілу навантажень на різні компоненти КС застосовують і спеціальні біомеханічні та електроміографічні дослідження — статографію та електроміографію м’язів [9–11].
Біомеханічні дослідження, зокрема статографія, дозволяють отримати дані про біомеханічні особливості функціонування кульшових суглобів залежно від виду патології та ступеня ДВВ, перерозподіл у навантаженні елементів КСу до- та післяопераційний період, а отже слугують обґрунтуванням методів хірургічної корекції деформацій великого вертлюга і правильності обраної лікувальної тактики. Показники біоелектричної активності м’язів (електроміографія) у разі патології КС у дітей свідчать про функціональний стан різних груп м’язів, динаміку в до- та післяопераційному періоді, а в поєднанні з іншими обстеженнями можуть служити підставою для обґрунтування, розробки та впровадження певних лікувальних заходів щодо скорішої реабілітації дітей у післярепозиційному періоді [12–14].
Маємо зазначити, що спеціальних досліджень, присвячених визначенню певних біомеханічних та електроміографічних показників у випадках ДВВ у до- та післяопераційний період, у вітчизняній літературі нами не знайдено.
Мета роботи: описати динаміку біомеханічних та електроміографічних даних у випадках деформацій великого вертлюга стегнової кістки в до- та післяопераційний періоди.
Матеріал та методи
У роботі проведено аналіз даних 70 дітей (46 хлопчиків та 24 дівчинки) з деформацією великого вертлюга (ВВ) на тлі різної патології КС — УВ та ПВС, деформації ПВСК внаслідок запальних захворювань КС, coxа vara, АН ГСК, які перебували на стаціонарному лікуванні в дитячому відділенні ДУ «Інститут патології хребта та суглобів ім. проф. М.І. Ситенка НАМН» за період з 1998 до 2014 р. Вік дітей становив від 4 до 18 років. За запропонованими методиками були обстежені хворі в до- та післяопераційний період (через 5–10 років після втручань).
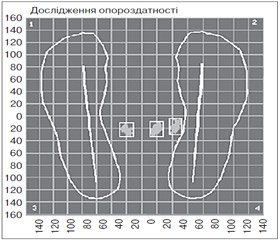
Методика статографії. Дослідження параметрів ходи виконували на пристрої «Статограф». Відповідно до методики протягом 30–40 c реєструються положення проекції загального центра маси тіла (ЗЦМ) та його переміщення щодо прямокутної системи координат при звичному стоянні на двох ногах. У результаті проведеного дослідження на екрані монітора з’являються три контактні зони у вигляді плям (рис. 1).
Математична обробка отриманих статограм дозволяє визначити положення ЗЦМ у системі координат, амплітуду коливань, величину навантаження при переважній опорі на одну кінцівку (табл. 1), а також розрахувати коефіцієнти хитання (Кх), навантаження (Кн), стійкості (Кс).
Зазначені показники характеризують такі параметри вертикального стояння:
— коефіцієнт хитання характеризує величину хитання ЗЦМ пацієнта у фронтальній і сагітальній площинах;
— коефіцієнт навантаження показує ступінь навантаження кожної кінцівки. При вільному стоянні Кн = 1, а при опорі на одну кінцівку він визначається як відношення маси, що припадає на опорну кінцівку, до загальної маси пацієнта: Кн = Рн / Рзаг;
— коефіцієнт стійкості як узагальнюючий показник стану опорно-рухової системи (ОРС) характеризує загальну стійкість пацієнта при різних типах стояння. Він визначається відношенням амплітуди хитання в нормі (10 мм) до амплітуди хитання, отриманої при дослідженні, помноженим на коефіцієнт навантаження: Кс = (10/Кх) • Кн.
Значення цих показників: у нормі Кх = 10 мм, при порушеннях в ОРС збільшується; Кн = 1,0–0,9, при порушеннях — зменшується; Кс = 1,0–0,9, при порушеннях — зменшується.
Аналіз цих показників дозволяє оцінити роботу системи регуляції рівноваги в двох площинах як при вільному стоянні, так і при зміні типу стояння, що вимагає зміни координації роботи м’язів пацієнта. Отримані статограми дозволяють досить точно судити про ступінь змін у стані опорно-рухового апарату [12, 13].
У зв’язку з тим, що хворі сильно відрізняються за віком та ступенем патологічного стану КС, як параметри для аналізу використовуємо не абсолютні, а відносні параметри вертикального стояння, а саме коефіцієнти асиметрії навантаження кінцівок, параметрів стійкості, асиметрію геометричних показників при одноопорному стоянні.
К_kх — коефіцієнт відношення показника хитання при одноопорному стоянні. Визначається як відношення меншого значення коефіцієнта хитання при стоянні з переважною опорою на одну кінцівку до більшого його значення: чим більше значення коефіцієнта наближається до 1, тим менше значення несиметричності.
К_kс — коефіцієнт відношення показника стійкості при одноопорному стоянні. Визначається як відношення меншого значення коефіцієнта стійкості при стоянні з переважною опорою на одну кінцівку до більшого його значення: чим більше значення коефіцієнта наближається до 1, тим менше значення несиметричності.
KasmN — коефіцієнт асиметрії навантаження стоп при стоянні на обох кінцівках. Визначається як відношення меншого значення до більшого: чим більше значення коефіцієнта наближається до 1, тим менше значення несиметричності.
RX — розкид загальних значень статограми по осі Х (фронтальна площина) за значеннями координат Х при одноопорному стоянні.
KasmX — коефіцієнт асиметрії координат Х при одноопорному стоянні.
RY — розкид значень по осі Y (сагітальна площина).
KasmY — коефіцієнт асиметрії розкиду координат Y при одноопорному стоянні.
KG — коефіцієнт геометрії (відношення розкиду по осі Y до розкиду по осі X за значеннями максимальних та мінімальних координат загальної статограми).
S_MO — загальна площа статограми за значеннями розкиду статограми по осях X та Y.
Динамометрію використовували для вимірювання сили м’язів КС. Отримані результати дозволяли визначити, які групи м’язів найбільше постраждали внаслідок захворювання або хірургічного втручання (отримані показники порівнювали з аналогічними показниками в нормі [15]), що дозволяло оцінити стан м’язів кінцівки та визначити процедури, які необхідно проводити при консервативному лікуванні.
Методика електроміографії (ЕМГ) дозволяє вимірювати й аналізувати сумарну біоелектричну активність скелетних м’язів під час їх довільного скорочення та в стані спокою [16–18]. Дані дослідження проводили за допомогою реєстрації біострумів м’язів поверхневими електродами з міжелектродною відстанню 20 мм на 4-канальному функціональному комплексі «Нейро-МВП-4». Запис і обробку сигналів здійснювали на ПК Pentium-5.
На м’яз, що досліджувався, а також на симетричний м’яз протилежної кінцівки накладали поверхневі одноразові електроди Skintakt з міжелектродною відстанню 2 см. Електроди розміщували в зоні рухової точки м’яза, вздовж ходу його волокон, або в центрі найбільшої контурованості м’яза.
Досліджували м’язи тазового поясу та стегна при їх максимальному напруженні під час виконання цільового руху м’яза. А саме: m.gluteus medius — відведення кінцівки в положенні лежачи на контралатеральному боці, m.adductor magnus — зведення стегон у положенні лежачи на спині (кінцівки зігнуті в кульшових та колінних суглобах), m.rectus femoris — підйом прямої кінцівки в положенні «лежачи на спині», m.biceps femoris — згинання кінцівки в коліні в положенні лежачи на животі. Для досягнення максимального скорочення дослідником чинився опір зазначеному довільному руху.
Обробка ЕМГ проводилася за допомогою турно-амплітудного аналізу (за Willison) в пакеті програм «Нейро-МВП.NETomega». Обчислювали середню амплітуду ЕМГ за 1 с та частоту потенціалів за 1 с.
За параметр частоти при турно-амплітудному аналізі береться не кількість перетинів ізолінії (фаз), а кількість поворотів (турнів) піків отриманої кривої (рис. 2). Для виключення можливих артефактів уся крива за амплітудою розподілялася на два потоки. Перший потік зафіксовано в межах 100 мкВ (± 50 мкВ щодо ізолінії), другий потік відмічається вище від даного коридору. Саме в другому потоці здійснюється аналіз поворотів і зміни амплітуди турнів для оцінки середньої амплітуди.
Статистична обробка результатів дослідження передбачала розрахунок основних описових характеристик груп — середнє значення та його стандартне відхилення, максимальне та мінімальне значення. Для порівняння періодів спостереження використовували Т-тест для парних вибірок. Для порівняння груп між собою — Т-тест для незалежних вибірок. Значення тесту приймали згідно з результатами тесту Левіня щодо припущення рівності дисперсій груп, що досліджували [19, 20].
Отримані результати і їх обговорення
Дані статографічних досліджень. Хворі були поділені на 2 групи. І групу становили діти, яким хірургічне лікування почали проводити до 6 років, ІІ групу — діти з оперативними втручаннями у віці понад 6 років. У табл. 1 показані дані розрахованих коефіцієнтів вертикального стояння в дітей до та після операції.
Як показали дослідження, у хворих з ДВВ К_kх був практично однаковим в обох групах (t = –0,691; p = 0,499) і залишився практично незмінним у віддаленому періоді після хірургічного лікування (t = 1,321; p = 0,235 у І групі та t = 0,529; p = 0,607 у ІІ групі). Аналогічну картину демонструє і K_kс: до лікування цей параметр у групах не відрізняється (t = –0,268; p = 0,792), а після операції мало змінюється (t = 0,835; p = 0,436 та t = 0,332; p = 0,746 у І та ІІ групах відповідно). Тобто особливості навантаження на суглоби залишаються у хворих як до, так і після лікування.
При дослідженні KasmN нами було виявлено, що до оперативного лікування у хворих І групи відмічали більш симетричне навантаження на нижні кінцівки (0,86 ± 0,12), ніж у хворих ІІ групи (0,67 ± 0,22), але різниця не досягала статистично значущого рівня (t = 2,007; p = 0,061). У віддаленому періоді після оперативного лікування KasmN у хворих ІІ групи статистично значущо покращився (t = –3,074; p = 0,011) (до 0,82 ± 0,18), хоча і не досяг середнього значення І групи до операції. У хворих І групи KasmN після хірургічного лікування декілька погіршився (до 0,74 ± 0,17), але різниця не досягла статистичного рівня (t = 1,524; p = 0,178).
До аналізу розкиду статограми у фронтальній площині треба підходити обережно, оскільки цей параметр залежить не тільки від спроможності людини опиратися на одну кінцівку, а й від антропометричних параметрів людини (ріст, довжина кінцівок, розмір стопи). Тому менший розкид координат Х у першій групі можна пояснити малим віком досліджених пацієнтів, а статистична значуща різниця (t = –2,444; p = 0,050) між періодами спостереження може пояснюватися ростом дитини. У дітей ІІ групи помітних змін не відбулося (t = –1,071; p = 0,307), хоча і спостерігається збільшення розкиду статограми по осі Х.
Параметр KasmX показує асиметричність розкиду по осі Х, тобто асиметричність опори на нижні кінцівки. Цей показник не залежить від антропометрії людини. До початку лікування в дітей обох груп KasmX був однаковим (t = –0,180; p = 0,859), а після хірургічного лікування у хворих ІІ групи він став хоча й у середньому гіршим (змінився з 0,67 ± 0,24 до 0,61 ± 0,25), але не досяг статистично значущого рівня (t = 0,647; p = 0,531). У хворих І групи KasmX погіршився статистично значущо (t = 2,457; p = 0,049) — з 0,65 ± 0,24 до 0,47 ± 0,21.
Параметри статограми у фронтальній площині мають переважно індивідуальний характер і залежать від особливостей осанки. Коефіцієнт асиметрії показує несиметричність відхилення тіла у сагітальній площині при переважній опорі на одну кінцівку.
У хворих із ДВВ порушена функція рівноваги, особливо при переважній опорі на одну кінцівку. Зберігається це порушення й після лікування. Хоча треба відмітити, що в зазначених хворих відхилення тіла в сагітальній площині при одноопорному стоянні практично не виходить за межі плями хитання двохопорного стояння.
Коефіцієнт геометрії показує, що у хворих із ДВВ геометрія статограми має переважно витягнутий у фронтальній площині характер, що й підтверджує попередній аналіз сагітального хитання тіла. KG у хворих із деформаціями ВВ мало відрізняється в осіб різних вікових груп і практично не змінюється з віком.
Аналіз даних табл. 2 показує, що вихідні дані залежали від особливостей патології КС. Так, найбільш виражені зміни у вертлюжному компоненті КС відзначені нами в разі розвитку деформацій ПВСК внаслідок запальних процесів: сила відвідних м’язів у разі одностороннього ураження була знижена від 25 до 40 % порівняно з протилежною стороною; показники статографічного дослідження (коефіцієнт навантаження кінцівок, коефіцієнт стійкості та відсоток навантаження на кожну кінцівку від маси тіла) також відзначалися найбільшими відхиленнями від норми та від здорової кінцівки саме в разі деформацій ПВСК внаслідок запальних процесів.
У разі деформації великого вертлюга, що розвинулася внаслідок coxа vara: сила відвідних м’язів при односторонньому ураженні була знижена не так виражено, як у випадках запальних захворювань, а в 44 % випадків навіть відзначено збільшення їх сили від 15 до 36 % порівняно з протилежною стороною; показники статографічного дослідження мали помірні відхилення від норми та від здорової кінцівки.
У разі деформації великого вертлюга, що розвинулася внаслідок УВ стегна, досліджувані показники варіювали в досить широких межах — від крайніх варіантів, які відзначалися при деструктивних запальних процесах, до помірних, які аналогічні змінам при coxа vara; показники статографічного дослідження також відзначалися різнонаправленими відхиленнями від норми та від здорової кінцівки й залежали від особливостей хірургічного втручання в кожному окремому випадку та від ступеня деформації ПВСК в цілому.
У разі деформації великого вертлюга, що розвинулася внаслідок АН ГСК, зміни показників мали найбільш помірний характер. Так, сила відвідних м’язів при односторонньому ураженні була збільшена від 11 до 41 % порівняно з протилежною стороною; показники статографічного дослідження відзначалися помірними відхиленнями від норми та від здорової кінцівки.
Маємо констатувати, що порушення функції КС за оцінкою клінічних даних (величина обмеження відведення стегна, порушення ходи та накульгування, а також синдром Тренделенбурга) за 3-бальною системою в пацієнтів із різною патологією КС, як правило, мала помірний характер, за винятком деяких хворих із наслідками запальних процесів, коли ці симптоми мали найбільш виражений ступінь.
У результаті вимірювання показників вертлюжного компонента ПВСК у віддаленому післяопераційному періоді (впродовж 5 років та більше) були отримані такі дані, що залежали від особливостей патології КС, виду хірургічного втручання та віку хворого, в якому це втручання виконано (нижче наведені середні дані): сила відвідних м’язів у всіх випадках збільшувалася порівняно з початковими даними, однак величина цього збільшення також варіювала в широких межах — від 5–20 % у разі наслідків запальних захворювань до 30–45 % у разі coxа vara та АН ГСК (у 15,7 випадків навіть відзначено збільшення їх сили від 7 до 26 % порівняно з протилежною стороною); показники статографічного дослідження відзначалися помірними відхиленнями від норми та від здорової кінцівки, але в усіх випадках мали чітку тенденцію до нормалізації своїх характеристик.
Оцінка клінічних даних стану КС за 3-бальною системою в пацієнтів у післяопераційний період, як правило, показує покращання функції КС в середньому на 1–3 бали у випадку врахування усіх трьох ознак — величини обмеження відведення стегна, нормалізації ходи та зменшення накульгування й синдрому Тренделенбурга.
Аналіз віддалених результатів хірургічних утручань на великому вертлюгу за допомогою оцінки клінікорентгенобіомеханічних даних показує, що найбільш сприятливі результати отримано у випадках утручань на ВВ у разі АН ГСК та coxа vara у строк від 3 років після операції, а найменш сприятливі отримані в групі дітей віком понад 6 років із патологічним вивихом стегна та наслідками остеомієлітичного ураження ПВСК. Несприятливі результати пояснюються початковими деструктивними змінами у ПВСК та рубцевим переродженням м’язів.
Дані електроміографічних досліджень. Як відомо, великий вертлюг є місцем прикріплення відвідних м’язів стегна, серед яких для поверхневої міографії досяжною є m.gluteus medius, окрім нього в даній роботі обстежувалися також привідні м’язи (m.аdductor magnus) та інші м’язи стегна (m.rectus femoris, m.biceps femoris).
Захворювання кульшового суглоба різного генезу призводять до порушення його функцій, обмеження об’єму рухів, формуванню патологічних динамічних стереотипів.
У результаті проведеного електроміографічного обстеження пацієнтів у до- та післяопераційний періоди лікування були отримані показники міограм ураженої та здорової кінцівок (табл. 3–5). Були обчислені середні значення амплітуди та частоти слідування біопотенціалів досліджуваних м’язів (табл. 3). На m.gluteus medius середня амплітуда біопотенціалів до оперативного лікування ВВ істотно не відрізнялася від такої на здоровій стороні (табл. 3).
Після оперативного лікування середня амплітуда біопотенціалів на стороні з патологією ВВ виявилася вірогідно нижчою, ніж на здоровій (табл. 4). За середньою частотою біопотенціалів m.gluteus medius здорова та хвора кінцівки істотно не відрізнялись ні до оперативного втручання, ні після нього. Також не виявлено сталої різниці між амплітудою та частотою біопотенціалів на m.аdductor magnus та на m.rectus femoris ні до, ні після оперативного лікування.
Після оперативного втручання за середньою амплітудою біопотенціалів на m.biceps femoris істотних відмінностей між здоровою та прооперованою кінцівками виявлено не було (табл. 4). Середня ж частота біопотенціалів на хворій стороні виявилася вірогідно нижчою, ніж на здоровій, імовірно, за рахунок сумації біопотенціалів.
У прооперованих пацієнтів на m.gluteus medius, m.adductor magnus та на m.rectus femoris середня частота біопотенціалів і на здоровій, і на хворій кінцівках підвищилася. Те ж саме можна сказати й про середню амплітуду біопотенціалів на m.rectus femoris.
Для вивчення участі м’язів у забезпеченні патологічних динамічних стереотипів нами були оцінені не тільки абсолютні показники біоелектричної активності м’язів тазового поясу, але й співвідношення цих показників в антагоністичних м’язах. Було виявлено, що співвідношення показників м’язів-антагоністів мало залежать від віку, фізичної тренованості та довжини кінцівки.
В обстежених нами здорових осіб коефіцієнт співвідношення середніх амплітуд біопотенціалів м’язів-антагоністів коливається в межах близько одиниці: m.gluteus medius/m.adductor magnus ≈ 1,3, m.gluteus medius/m.rectus femoris ≈ 1,4; m.adductor magnus/m.rectus femoris ≈ 1,06 (табл. 5, 6).
У 83 % пацієнтів із патологією великого вертлюга співвідношення середніх амплітуд біопотенціалів антагоністичних м’язів m.gluteus medius/m.adductor magnus на здоровій кінцівці також мало значення 0,8–1,7, у 100 % пацієнтів співвідношення m.gluteus medius/m.rectus femoris ≈ 0,957, співвідношення m.adductor magnus/m rectus femoris ≈ 1,17.
Для хворих кінцівок виявлено підвищення коефіцієнтів для m.gluteus medius/m.adductor magnus за рахунок підвищення середньої амплітуди біопотенціалів на m.gluteus medius. Таким чином, значення середнього співвідношення m.gluteus medius/m.adductor magnus для хворих кінцівок сягало 2,2. Причому в групі пацієнтів із coxa vara це співвідношення було меншим за одиницю (0,51), а в групі з уродженим вивихом стегна — 3,67 (вірогідна відмінність р = 0,05, Т-тест = 0,0018).
У хворих з УВ та ПВС у 77 % випадків середня амплітуда біопотенціалів на сідничних м’язах була вищою, ніж на привідних м’язах, а у групі з coxa vara в 50 % випадках відзначалося підвищення амплітуди саме на m.adductor magnus порівняно з m.gluteus medius, тобто знайдено вірогідні відмінності коефіцієнтів m.gluteus medius/m.adductor magnus у групах із різною патологією, що свідчить про різні реципрокні м’язові відношення.
Після операції в групі хворих кінцівок відзначалося вірогідне зниження коефіцієнта амплітуд glut/adductor (р = 0,05), причому відмінності між групами патології перестали бути вірогідними. Але в кожній групі відбулися суттєві зміни коефіцієнтів, особливо в групі соха vara, де коефіцієнт glut/adductor збільшився за рахунок зменшення активності m.gluteus medius.
При патології ВВ в описуваній групі хворих відбувається зближення точок кріплення m.gluteus medius, що сприяє ретракції м’яза, а в разі напруження цього м’яза відбувається сумація потенціалів від близько розташованих рухових одиниць, що відображається в підвищенні середньої амплітуди біопотенціалів. У цей час m.adductor magnus виявляється в розтягнутому стані. Відомо, що тонус привідних м’язів дорівнює тонусу відвідних м’язів, в умовах зрілості центральної нервової системи й відсутності пірамідної патології.
У післяопераційному періоді ми спостерігаємо вірогідну тенденцію до нормалізації біоелектричної активності привідних та відвідних м’язів КС за рахунок зменшення активності m.gluteus medius та підвищення m.adductor magnus.
При більш детальному аналізі даних ЕМГ у групі пацієнтів з АН ГСК та уродженим вивихом стегна видно, що в багатьох хворих спостерігається порушення реципрокного балансу між привідними і відвідними м’язами: зниження амплітуди біопотенціалів лише на m.glutaeus medius та підвищення амплітуди біопотенціалів на m.adductor magnus хворої кінцівки.
Висновки
1. Встановлена пряма залежність ступеня тяжкості анатомо-функціональних змін (у тому числі в м’язах) від особливостей основної патології КС (найбільші зміни відзначені у випадках патології КС внаслідок перенесеного запального процесу (патологічний вивих стегна), а найменші — у разі АН ГСК і coxa vara) та віку, у якому дана патологія виникла: чим менший вік, тим більш виражені зміни відзначаються.
2. Дані біомеханічного та електроміографічного дослідження дозволяють стверджувати, що у випадках виражених деформацій ВВ у м’язах, у першу чергу пельвіотрохантерної групи, відбуваються певні різнонаправлені зміни. Так, сила відвідних м’язів у разі одностороннього ураження була знижена від 25 до 40 % порівняно з протилежною стороною; показники статографічного дослідження (коефіцієнт навантаження кінцівок, коефіцієнт стійкості та відсоток навантаження на кожну кінцівку від маси тіла) також відзначалися найбільшими відхиленнями від норми та від здорової кінцівки саме в разі деформацій ПВСК внаслідок запальних процесів, а у випадку високого розташування ВВ при АН ГСК та coxa vara сила відвідних м’язів при односторонньому ураженні була знижена не так виражено, а у 44 % випадках навіть відзначено збільшення їх сили від 15 до 36 % порівняно з протилежною стороною; показники електроміографічного дослідження відзначалися аналогічними змінами в до- та післяопераційний період.
3. Отримані дані мають стати пунктом відліку для подальшого спостереження за їх динамікою, а комплексне клініко-рентген-біомеханічне та електроміографічне обстеження дітей з деформаціями ВВ дозволяє провести їх розподіл на певні групи залежно від ступеня анатомо-функціональних змін та визначати індивідуальні підходи до вибору лікувальної (у тому числі хірургічної) тактики в даної категорії хворих.
/57.jpg)

/52.jpg)
/54.jpg)
/53.jpg)
/55.jpg)
/56.jpg)