Статья опубликована на с. 38-42
Введение
В кровеносной системе живого организма циркуляция крови осуществляется согласованными действиями сердца и сосудов, что обеспечивает адаптацию к постоянно изменяющимся условиям жизнедеятельности в пределах гомеостатических границ. Среди интегральных характеристик сердечно-сосудистой системы наиболее доступной и важной характеристикой является величина артериального давления (АД), которая зависит от объема циркулирующей крови, работы сердца и сосудов (периферического сосудистого сопротивления, эластичности сосудов, участия мышц), а также реологических свойств крови. Величина АД выражается несколькими показателями: систолическим давлением S (максимальное давление при сокращении сердечной мышцы), диастолическим давлением D (минимальное давление между ударами сердца в момент расслабления сердечной мышцы, отражающее сопротивление периферических сосудов и частоту сердечных сокращений), а также пульсовым давлением W (по определению: W = S – D). Несмотря на большие колебания внутрисосудистого давления во время систолы и диастолы, кровоток осуществляется при устойчивом режиме давления, которое называется средним гемодинамическим давлением. Таким образом, величина АД содержит два компонента — постоянный, характеризующийся величиной среднего гемодинамического давления М, и пульсирующий, характеризующийся величиной W. Считается, что М отражает энергию непрерывного движения крови, зависит от сократительной функции сердца и общего периферического сосудистого сопротивления, поэтому эта величина может использоваться для оценки компенсаторных возможностей кровообращения [1]. Среднее давление М, как искусственно выделяемая величина, вычисляется обычно по наиболее популярной формуле Хикэма: М = D + (S – D)/3 [2].
Пульсовое давление W заключает в себе результат взаимодействия сократительной функции сердца, растяжимости артерий и величины волны отражения [2]. Считается, что повышение W связано с увеличением жесткости артерий (что сопровождается ростом амплитуды волны отражения). Показано, что повышение W является информативным предиктором смертности от сердечно-сосудистых заболеваний [3, 4].
Временные ряды измерений S и D могут быть подвергнуты анализу в прогностических целях [5], при этом каждое конкретное значение АД можно рассматривать как систему, где между «входом» (систолическое давление S) и «выходом» (диастолическое давление D) находится «состояние», называемое пульсовым давлением W, являющимся системообразующим элементом этой системы. Тогда нахождение связей между параметрами АД в интервале времени наблюдения может быть использовано для построения индивидуальной регрессионной модели кровообращения, характеризующей функционирование сердечно-сосудистой системы в интервале времени наблюдения [6, 7].
Основным результатом исследований [6] является нахождение в параметрическом пространстве величин АД линейных уравнений S = f1(W) и D = f2(W), которые описывают гемодинамическое состояние сердечно-сосудистой системы патентованной методикой количественного анализа связей параметров артериального давления [7]. Найденные связи между параметрами АД пациентов используются авторами для диагностики конкретного пациента, исходя из предложенной авторами классификации типов гемодинамики: гармонического (с подтипом миокардиально-недостаточным), дисфункциональных диастолического и систолического, а также пограничных типов.
В настоящее время показано, что линейная регрессионная модель может служить косвенным методом определения ригидности кровеносных сосудов по так называемому амбулаторному индексу жесткости артерий (AASI), который определяется через коэффициенты линейной регрессии D по S [8]. На большой популяции пациентов (более 11 тыс. человек) доказано, что коэффициенты линейной регрессии D по S при суточном мониторировании АД зависят от соотношений между пульсовой и постоянной компонентами АД и коррелируют со скоростью распространения пульсовой волны. Поэтому значения этих коэффициентов могут служить предиктором инсульта и сердечно-сосудистой смертности как у гипертензивных, так и у нормотензивных пациентов [9, 10]. Кроме того, авторами показано, что случайное исключение отдельных показаний из временного ряда измерений АД, сделанного через 30-минутные интервалы времени, существенно не влияет на коэффициенты линейной регрессии (среднее значение индекса жесткости) до тех пор, пока число измерений АД больше 7 [9, 10].
Таким образом, построение простейших линейных моделей дает ценную клиническую информацию о гемодинамике пациента и позволяет оценить риски развития опасных инцидентов. Наиболее актуальна такая информация прежде всего при ряде тяжелых заболеваний и состояний, которые сопровождаются опасным падением АД (сепсис, кровотечение, перитонит, инфаркт миокарда, тромбоэмболия легочной артерии и др.). Гипотензия может также провоцироваться вторично под воздействием сосудорасширяющих средств. Острая гипотензия, когда среднее гемодинамическое давление М опускается до 60 мм рт.ст. и ниже, увеличивает смертность пациентов в 2 раза [12]. Поэтому для отделений интенсивной терапии, где находятся такие пациенты, актуально выделение пациентов с высоким риском опасного снижения АД.
Целью настоящего исследования является развитие метода линейной регрессии параметров АД для классификации пациентов отделений интенсивной терапии по степени риска развития острых эпизодов вторичной гипотензии.
Материалы и методы исследования
Изучались временные ряды АД пациентов отделения интенсивной терапии, подверженных риску угрожающей гипотензии на фоне тяжелой формы основного заболевания. Использована база данных MIMIC II Clinical Database [12, 13], которая включает в себя временные ряды клинических измерений АД (S и D) в лучевой артерии с интервалом измерений 1 мин и длительностью не менее 10 часов у пациентов отделения интенсивной терапии. Часть пациентов (43 чел., группы H1, H2, C2 [12]) за это время пережили по крайней мере один острый гипотензивный эпизод (они образовали группу с высоким риском вторичной гипотонии), 15 пациентов (группа С1 [13]) не имели таковых эпизодов (группа низкого риска). Нами для удобства изменялась частота дискретизации до 1 измерения в 15 мин (подобная частота измерений характерна для аппаратного автоматического измерения АД при суточном мониторировании АД). Кроме того, сигналы АД подвергались усреднению посредством сглаживания при скользящем среднем.
Построение линейной регрессионной модели
Очевидно, что при рассмотрении взаимосвязей между S и W (или D и W) переменная S представляется независимой, а W — зависимой, но такая зависимость является неоднозначной в том смысле, что каждому конкретному значению S может соответствовать некоторое вероятностное распределение зависимой переменной W. Математическое ожидание переменной и определяет функцию регрессии S на W (рис. 1).
/40.jpg)
Применяемая здесь линейная регрессия является одним из методов восстановления зависимости между переменными. Ниже приведен пример построения линейной модели зависимости параметров S и D от W по заданной выборке и показан результат на графике (рис. 1). Для заданного множества из N пар измерений (Si,Wi), а также (Di,Wi), (i = 1, …, N) строится линейная модель: Si = f(Wi) + εi, Di = f(Wi) + εi c аддитивной случайной величиной ε. Предполагается, что случайная величина распределена нормально с нулевым математическим ожиданием и фиксированной дисперсией, которая не зависит от переменных S и D. При таких предположениях найдем линейную теоретическую функцию регрессии: S = Q + a1W — и коэффициенты регрессии Q и a1, используя метод наименьших квадратов. Поскольку пульсовое давление определяется как W = S – D, то D = Q + (a1 – 1)W. Параметры регрессии Q и a1 определяются методом наименьших квадратов с целью минимизации величины ошибки. Аналогично строится следующее уравнение: S = B + AD, где параметры А и В являются вторым набором коэффициентов линейной регрессии. Следует отметить, что проведенное нами предварительное преобразование W (возведение в степень, извлечение корней и т.д.) не позволило улучшить возможности регрессии.
Значение коэффициентов состоит в следующем. Считается, что Q характеризует давление потока крови в области затухающей пульсовой волны (в конечной части артериол), параметр а определяет соотношение вклада сердца и сосудов в кровообращение. Для нормального (гармонического) типа кровообращения пациента значение коэффициента Q практически совпадает со средним гемодинамическим давлением, которое является интегрированным средним значением АД за время сердечного цикла. Значение коэффициентов A и B, определяющих линейную регрессию систолического S на диастолическое давление D, может быть также определено в терминах индекса жесткости сосудов AASI [9, 10]. Кроме того, было сделано наблюдение связи выброса депонированного объема крови пациента и, как следствие, возникновения гипертонического криза со значениями параметров А и В [7].
Таким образом, использование вектора характерных особенностей гемодинамической системы x = {Q, a1, A, B} с полным набором коэффициентов регрессии параметров АД позволит классифицировать гемодинамику пациентов в диагностических и прогностических целях.
Вектор признаков гемодинамики и понижение размерности пространства признаков
Сокращение числа значимых входных признаков или уменьшение размерности модели является важной задачей классификации, поскольку, во-первых, удаляются менее значащие признаки, во-вторых, модель упрощается и улучшается ее качество. Существенного сокращения размерности пространства признаков можно достичь с помощью нелинейных преобразований переменных или применения пошаговой процедуры отбора переменных. Ранжирование наиболее значимых признаков вектора x в настоящей работе осуществляется по ROC-критерию (Receiver Operating Characteristics) [11], который широко применяется в медицине. ROC-кривая показывает зависимость количества верно классифицированных образцов от числа неверно классифицированных, поэтому для каждого признака вычислялась ROC-кривая и выбирались признаки с максимальной площадью под ROC-кривой. Применение ROC-критерия к компонентам вектора x позволило в итоге понизить размерность вектора признаков до 2, после чего рассчитанные данные x = {Q, a1} передавались для обучения классификатора на основе опорных векторов.
Обучение опорных векторов классификатора и классификация образцов АД
Задача классификации АД по степени риска развития острого гипотензивного эпизода заключается в построении линейной регрессионной модели, вычислении вектора характерных признаков (атрибутов), создании модели бинарного классификатора по методу опорных векторов (МОВ) [14], его обучения на тренировочном наборе образцов и, наконец, классификации тестовых образцов АД.
В настоящей работе для построения модели классификатора МОВ используется разбиение набора данных АД двух групп пациентов (группы высокого и низкого риска приступа гипотензии) на обучающее и тестовое множество случайным образом в пропорции 75 % : 25 %.
Особым свойством МОВ является непрерывное уменьшение эмпирической ошибки классификации объектов и поиск разделяющей гиперплоскости между классами с максимальным зазором в двухмерном пространстве признаков. Поскольку каждый сигнал представляется как вектор в пространстве признаков и принадлежит только одному из двух классов, максимизация зазора между классами означает более достоверную классификацию по степени риска возникновения эпизодов гипотонии (высокий/низкий). Обучение классификатора МОВ по степени риска считается завершенным при достижении максимального значения показателя качества. Таким образом, для образцов с низким и высоким риском гипотонии вектора x будут находиться по разные стороны разделяющей гиперплоскости, которая определяется путем максимизации расстояния до векторов x.
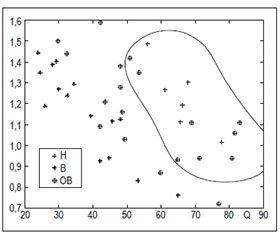
Зададим значения вектора атрибутов как x = {Q, a1} в двухмерном пространстве признаков. Задача построения разделяющей гиперплоскости эквивалентна нахождению единственного минимума квадратичного функционала, когда суммирование осуществляется только по опорным векторам (т.е. по приграничным векторам x0). При решении задачи классификации рассматриваемым методом требуется добавление так называемого оператора ядра. На рис. 2 показана основная идея МОВ с радиальной базисной функцией в качестве ядра при использовании двухмерного вектора атрибутов. На рис. 2 крестиками отмечены образцы АД с высоким риском, звездочками — образцы с низким риском гипотонии из обучающего и тестового набора, опорные вектора отмечены дополнительно кружком. Данный пример показывает, что классификация на основе всего 2 атрибутов (Q и a1) дает высокий показатель качества разделения сигналов (в нашем случае это значение составило 93 %).
/41.jpg)
Представим теперь результаты ROC-анализа, позволяющие оценить качество бинарной классификации и определить зависимость доли верных классификаций от доли ложных классификаций: 1 ложноотрицательный диагноз (FN = 1) для 43 образцов АД с высоким риском гипотензии (TP = 42) и 2 ложноположительных диагноза (FP = 2) для 15 образцов АД с низким риском гипотензии (TN = 13).
Заключение
В данной работе мы представили метод классификации медицинских сигналов АД по степени риска развития гипотензии, основанный на построении линейной регрессионной модели для параметров АД с последующим применением классификатора по методу опорных векторов. Обучаемый по прецедентам машинный алгоритм дифференциации сигналов дает высокий показатель качества (93 %). Для обучения классификатора был рассчитан 4-размерный вектор характерных особенностей АД: x = {Q, a1, A, B}, координатами которого являются коэффициенты линейной регрессии систолического, диастолического и пульсового давления. При этом наилучшими качествами для классификации медицинских сигналов АД по степени риска развития гипотензии обладали модели, в которых использовались параметры регрессии систолического давления по пульсовому давлению (или диастолического — по пульсовому), чем параметры регрессии систолического давления по диастолическому давлению. Применение ROC-критерия к компонентам вектора x позволило в итоге понизить размерность вектора признаков до 2, после чего рассчитанные данные x = {Q, a1} передавались для обучения классификатора на основе МОВ, где координаты вектора признаков представляют собой беспульсовое давление и соотношение вклада сердца и сосудов в кровообращение.
Следует отметить, что повышение качества классификации МОВ в основном происходит при удалении из обучающего множества образцов с ложным диагнозом, кроме того, качество классификации является высоким даже при относительно небольшом размере обучающего набора АД. Достоинство данного метода классификации состоит в высокой эффективности (93 %) и достаточности ограниченного набора данных, что отличает его от большинства других методов.
Результаты исследования могут быть полезными для фундаментальных исследований в области гемодинамики сердечно-сосудистой системы, в отделениях интенсивной терапии для раннего выявления пациентов с риском развития острых гипотензивных эпизодов, в кардиологической функциональной диагностике, а также для разработки и оценки диагностических и прогностических алгоритмов в медицине.
Список литературы
1. Кушаковский М.С. Гипертоническая болезнь. — СПб.: Сотис, 1995. — 4-е изд. — 311 с.
2. Рашмер Р. Динамика сердечно-сосудистой системы: Пер. с англ. М.А. Безносовой, Т.Е. Кузнецовой; под ред. Г.И. Косицкого. — М.: Медицина, 1981. — 600 с.
3. Weiss A., Boaz M., Beloosesky Y. et al. // J. Gen. Intern. Med. — 2009. — V. 24(8). — P. 893-896.
4. Frederique T., Jacques B., Athanase B. et al. // J. Hypertens. — 2008. — V. 26(6). — P. 1072-1077.
5. Баевский Р.М. Прогнозирование состояний на грани нормы и патологии. — М.: Медицина, 1979. — 298 с.
6. Хурса Р.В., Чеботарев В.М. Гемодинамические детерминанты гомеостаза сердечно-сосудистой системы // Клиническая физиология кровообращения. — 2007. — № 4. — С. 71-77.
7. Хурса Р.В., Чеботарев В.М., Балышева В.М. Способ перманентного контроля индивидуального функционального состояния кровообращения: Патент BY № 4876.
8. Benetos A., Lacolley P. From 24-Hour Blood Pressure Measurements to Arterial Stiffness: A Valid Short Cut? // Hypertension. — 2006. — V. 47. — P. 327-328.
9. Li Y, Wang J.G., Dolan E. et al. // Hypertension. — 2006. — V. 47. — P. 359-364.
10. Dolan E., Thijs L., Li Y. et al. // Hypertension. — 2006. — V. 47. — P. 365-370.
11. Цыплаков А.А. Некоторые эконометрические методы. Метод максимального правдоподобия в эконометрии: Учебное пособие. — Новосибирск: ЭФ НГУ, 1997. — 126 с.
12. Moody G.B., Lehman L.H. // Computers in Cardiology. — 2009. — V. 36. — P. 541-544.
13. The MIMIC II Project database: http://physionet.org/physio-bank/database/mimic2db
14. Vapnik V. Statistical learning theory. — Berlin: Springer, 1998.
Впервые опубликовано в журнале «Известия академии наук Беларуси», № 1, 2013, серия физико-математических наук, с. 117-122
/40.jpg)
/41.jpg)