Введение
Сосудистые нарушения являются достаточно частым и наиболее грозным осложнением острого некротического панкреатита (ОНП) и обострения хронического панкреатита (ХП). Они включают венозные тромбозы портальных, селезеночных и брыжеечных сосудов, диффузные кровотечения из варикозно расширенных вен, ишемические некрозы с образованием инфаркта селезенки и некроза желудка, тонкой и толстой кишки, аррозии артериальных сосудов с образованием ложных аневризм (ЛА). Аррозия сосудов с образованием ЛА висцеральных сосудов, вовлеченных в некротический процесс, является наиболее опасным осложнением. Данная категория осложнений ОНП и ХП нечастая, однако наиболее грозная и тяжелая.
Впервые описал аневризму селезеночной артерии в 1770 году M. Beaussier при аутопсии больного, умершего от внутреннего кровотечения, которая стала случайной находкой. Образование ЛА наблюдается как в острый период, так и в последующее время после перенесенного ОНП на этапе развития у пациента ХП. Предрасполагающими факторами в генезе ЛА являются дисплазия сосудов, портальная гипертензия, спленомегалия и локальные воспалительные процессы. Частота возникновения ЛА при ОНП составляет 1,2–14 % [1–7]. Зарегистрированная заболеваемость ХП, осложненного кровотечением из псевдоаневризм, колеблется от 4 до 10 % [8, 9]. Наиболее часто развиваются псевдоаневризмы селезеночной артерии, реже — гастродуоденальной, панкреатодуоденальной и печеночных артерий [10].
Формирование ЛА имеет два варианта. В случае аррозии артерии в ткани поджелудочной железы размеры ЛА бывают небольшими. Этот вариант ЛА протекает, как правило, бессимптомно и диагностируется случайно на этапах динамического обследования.
Второму варианту формирования ЛА предшествует образование псевдокисты. Развитие постнекротических псевдокист осложняет течение острого панкреатита у 5–15 % больных [3]. Самой частой причиной возникновения аневризм является аррозия сосудов псевдокист (жидкостных скоплений) поджелудочной железы. Псевдокисты содержат панкреатические энзимы, которые вызывают периартериальное воспаление, некроз стенки сосуда, расположенного рядом со стенкой кисты, и разрушают ее. Когда артерия «прорывается» в кисту, она формирует ложную аневризму или кровотечение в псевдокисту [2, 11, 12]. Таким образом, псевдокиста трансформируется в ложную аневризму. В таких вариантах размеры ЛА соответствуют размерам псевдокист и бывают достаточно большими. Чаще большая часть объема ЛА тромбируется, а полость с сохраненным кровотоком составляет 20–70 % от объема ЛА [1]. Развитие кровотечения в постнекротическую кисту является грозным осложнением и сопровождается летальностью до 80 % [13].
Еще одной особенностью ЛА второго типа является связь полости с панкреатическими протоками. Длительный контакт сосудов с агрессивными ферментами поджелудочной железы (ПЖ) ведет к повреждению стенки и аррозивному кровотечению с клиникой вирсунгоррагии и кишечного кровотечения. Эти кровотечения бывают различной интенсивности и часто рецидивируют [14, 15]. Дальнейшая патологическая картина связана с развитием тромбоза одноименных висцеральных вен на фоне продолжающегося некроза окружающих поджелудочную железу тканей. Повышение давления в питающей ложную аневризму артерии при сохраняющемся венозном блоке приводит к ее разрыву и массивному кровотечению. Кровоизлияние может распространяться в брюшную полость, забрюшинное пространство, в просвет кишки, чаще двенадцатиперстной, или в панкреатический проток.
В большинстве случаев клиническая картина ОНП и обострения ХП, осложненного ЛА непарных висцеральных артерий, является неспецифичной и вызывает трудности в дифференциальной диагностике. ЛА больших размеров клинически проявляются выраженным болевым синдромом. Часто отмечаются анемии неясного генеза и сдавления рядом расположенных органов брюшной полости. Заподозрить ЛА можно при возникновении осложнений, основное из которых — разрыв аневризмы и кровотечение в забрюшинную клетчатку, свободную брюшную полость, панкреатический проток или кисту поджелудочной железы. Часто единственным клиническим симптомом ЛА является рецидивирующее желудочно-кишечное кровотечение без выявленного источника. ЛА, как правило, не вызывают появления симптомов, пока не происходит их разрыв, что проявляется симптомами острой кровопотери.
Диагностический комплекс обследования включает рентгенографию брюшной полости и желудка, гастродуоденоскопию (ГДС), ультразвуковое исследование (УЗИ) с дуплексным сканированием сосудов, компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ), ангиографию. Рентгенографию брюшной полости выполняют всем пациентам с выраженным болевым синдромом для дифференциальной диагностики с другими острыми хирургическими заболеваниями. По данным рентгенографии выявляется наличие полостных образований в проекции ПЖ. Контрастная гастродуоденография показывает картину внешнего сдавления желудка и двенадцатиперстной кишки (ДПК) с явлениями частичной или полной гастродуоденальной непроходимости в зависимости от топографического расположения псевдокисты или ЛА. Данные ГДС (сдавление задней стенки желудка и медиально-верхней стенки двенадцатиперстной кишки, явления гастродуоденостаза, воспалительно-некротическое изменение слизистой) дополняют информацию о наличии объемного образования. Наблюдение о выделении свежей крови из дуоденального соска подтверждает аррозию сосуда с прорывом в главный панкреатический проток. Однако вышеперечисленные методы лишь косвенно указывают на наличие ложной аневризмы.
Эффективным методом инструментальной диагностики ЛА является УЗИ органов брюшной полости с дуплексным сканированием сосудов (УЗДГ) [16], а также КТ и МРТ органов брюшной полости с внутривенным контрастированием. Однако золотым стандартом в настоящее время является ангиография, позволяющая получить исчерпывающую информацию о наличии ЛА и ее локализации, топографические особенности зоны исследования и информацию об анатомии сосудов, питающих аневризму. Полученные при ангиографии данные помогают определить тактику лечения и выбор метода выключения ЛА из кровотока [17, 18].
Применяются два метода лечения ложных аневризм непарных висцеральных артерий — открытые операции или рентгенэндоваскулярные вмешательства.
Рентгенэндоваскулярные методы лечения ЛА включают в себя использование различных эмболизирующих спиралей, губок, гелей и стент-графтов. Ангиография широко используется для выявления источника висцерального артериального кровотечения с последующей артериальной эмболизацией для остановки кровотечения. Радиологический сосудистый подход показал свою эффективность для пациентов с псевдоаневризмами, осложненными кровотечениями [17, 19, 25]. На сегодняшний день сохраняется высокий риск рецидива кровотечения из псевдоаневризмы у больных после ангиоэмболизации. Тем не менее применение ангиографии и ангиоэмболизации в качестве первой линии терапии, для диагностики и остановки кровотечения и стабилизации жизненных показателей является рациональной стратегией лечения и широко используется в современной клинической практике [17, 18].
Открытые операции включают в себя различные варианты резекции ЛА, лигирования устья ЛА и резекции поджелудочной железы с ЛА. Хирургические вмешательства, в том числе прямая артериальная перевязка с опорожнением псевдокисты или резекция поджелудочной железы, используются для лечения ЛА, осложненных кровотечением. Для пациентов с ЛА, расположенными в головке и теле поджелудочной железы, используется цистотомическая артериальная перевязка и наружное дренирование кисты ПЖ. Дистальная панкреатэктомия рекомендуется для пациентов с ЛА, расположенными в хвосте поджелудочной железы. После безуспешной артериальной эмболизации рекомендуют выполнять экстренную открытую перевязку артерии, питающей ЛА. Однако лигирование или ушивание сосуда связано с более высокими показателями рецидива кровотечения и повторных вмешательств, и резекция ПЖ является предпочтительным выбором лечения. Таким образом, роль открытых хирургических вмешательств при кровотечениях из ЛА у больных с ХП остается спорной. Большинство специалистов считают, что хирургическое вмешательство следует проводить у пациентов, у которых эмболизация артерии, питающей ЛА, невозможна по техническим причинам или ее результат неэффективен [20, 21].
Клинический случай
Пациент Н., 37 лет, поступил в отделение хирургии Минской областной клинической больницы для планового оперативного лечения с диагнозом «хронический панкреатит, обострение, киста головки и тела поджелудочной железы больших размеров, сахарный диабет». На момент поступления рост — 169 см, масса тела — 50 кг, индекс массы тела — 17,5. Выраженный болевой синдром. Из анамнеза: страдает хроническим панкреатитом около 5 лет; за последний год состояние ухудшилось: усилился болевой синдром, неоднократно лечился стационарно без положительного эффекта, отмечает потерю массы тела на 10 кг.
По данным УЗИ: поджелудочная железа — 60 × 54 × × 5 мм, контур неровный, нечеткий, структура диффузно неоднородная, эхогенность смешанная. В головке-теле киста 63 × 35 мм с эхопозитивными включениями, вирсунгов проток 4–6 мм, расширен.
Гастроскопия: просвет желудка деформирован в пилородуоденальной зоне, перистальтика не изменена, слизистая оболочка умеренно гиперемирована в антральном отделе, складки нормальные, привратник асимметричный. Просвет двенадцатиперстной кишки деформирован и сужен из-за отека.
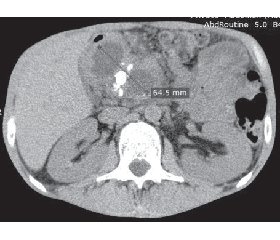
КТ: поджелудочная железа 75 × 16 × 16 мм, структура паренхимы неоднородная, множественные кальцинаты, вирсунгов проток расширен в области тела и хвоста до 8 мм с конкрементами до 7 мм. В области головки визуализируются два дополнительных объемных образования однородной жидкостной плотности (+8 едН) размерами 78 × 55 × 32 мм и 40 × 29 × 47 мм, имеющие стенку 3–10 мм, компримирующие ДПК. Заключение: хронический кальцифицирующий панкреатит, псевдокисты поджелудочной железы, панкреатолитиаз, вирсунгоэктазия (рис. 1).
/152-1.gif)
Учитывая данные обследований, диагноз псевдо–аневризмы установлен не был. Планировалось выполнить реконструктивную операцию на поджелудочной железе, включающую резекцию головки поджелудочной железы со вскрытием кисты. На операции была выявлена выраженная сеть варикозно расширенных вен в области большого и малого сальника, желудочно-ободочной связки. Выполнена холецистэктомия. После панкреатовирсунготомии над перешейком под давлением выделялся секрет поджелудочной железы, вирсунгов проток расширен до 6–7 мм. Выполнена локальная передняя резекция головки поджелудочной железы в объеме операции Фрея со вскрытием кисты, располагавшейся по задней стенке головки поджелудочной железы. При ревизии полости кисты установлено, что киста больших размеров, до 10 см в диаметре, многокамерная. Из полости кисты удалены сгустки крови и элементы аневризматической чашки, после чего открылось активное артериальное кровотечение из полости кисты. При попытке расширить цисто-панкреатическое отверстие по задней стенке головки поджелудочной железы произошло повреждение воротной вены, с последующим ушиванием дефекта последней. Достичь временного частичного гемостаза удавалось пальцевым прижатием и тампонированием полости псевдоаневризмы. Для установки источника произведена дополнительная мобилизация двенадцатиперстной кишки с головкой поджелудочной железы с последующим широким рассечением задней стенки псевдоаневризмы, где в глубине был выявлен крупный артериальный ствол, предположительно селезеночная или печеночная артерия, с большим дефектом в стенке, ушить последний не удалось из-за хрупкости сосуда, в связи с чем он был прошит и перевязан. Учитывая большой объем кровопотери (за время операции перелито 2500 мл свежезамороженной плазмы и 2000 мл эритроцитарной массы), длительность операции более 7 часов, а также неясный прогноз в отношении жизнеспособности печени и других органов брюшной полости, реконструктивный этап операции на поджелудочной железе решено отсрочить. При дополнительной ревизии патологии мезентериальных сосудов не выявлено, воротная вена после ушивания проходима. Зона операции тампонирована и дренирована, швы на рану через все слои на протекторах.
Биопсия: ткань ПЖ с выраженным интра- и перилобарным склерозом, эктазия протоков с застоем секрета и формированием конкрементов; очаговая пролиферация сосудов.
В послеоперационном периоде лечение проводилось в реанимационном отделении: инфузионная терапия, антибиотикотерпия, гепатопротекторы, низкомолекулярные гепарины, октреотид, раннее энтеральное питание и др. В 1-е сутки выявлены признаки ишемического повреждения печени: УЗИ — артериальный кровоток в паренхиме печени не определяется, воротная вена — до 13 мм, скорость кровотока — 0,47 м/с, перистальтика кишечника определяется. Лабораторные признаки цитолиза (общий билирубин — 30 мкмоль/л, аланинаминотрансфераза (АЛТ) — 1440 ед/л, аспартата–минотрансфераза (АСТ) — 1800 ед/л), с постепенной нормализацией показателей в течение 3 дней до АЛТ — 462 ед/л, АСТ — 244 ед/л. На контрольном УЗИ участки некроза паренхимы печени не определяются.
В связи с компенсацией состояния пациента и лабораторных показателей на 3-и сутки после операции было решено выполнить реконструктивный этап операции. На операции: после извлечения тампонов печень бледно-розового цвета, с очагами уплотнения. Зона резекции головки поджелудочной железы и вирсунгов проток несколько отечны, крови и сгустков в полости псевдокисты нет. Тонкая и толстая кишка розового цвета, с активной перистальтикой. Выполнена панкреатоеюностомия на петле по Ру. На 5-е сутки переведен из реанимации в хирургическое отделение. Послеоперационное течение без осложнений, однако на 8-е сутки по дренажу из брюшной полости начало ежедневно выделятся до 150–200 мл желчного отделяемого, в последующем сформировался неполный наружный желчный свищ. При выписке на 17-е сутки после операции: гемоглобин — 138/л, гематокрит — 40 %, общий белок — 71 г/л, мочевина — 2,5 ммоль/л, общий билирубин — 7,0 мкмоль/л, АЛТ — 108 ед/л, АСТ — 107 ед/л.
/153-1.gif)
Через 4 месяца пациент повторно госпитализирован с наружным желчным свищом и полным сбросом желчи, кал ахоличен. При выполнении МРТ с холангио–панкреатографией и ангиографией выявлено: дренаж под печенью в области общего печеночного протока, желчный пузырь и холедох не дифференцируются, расширены внутрипеченочные протоки. Головка и частично тело поджелудочной железы четко не дифференцируются, в S7 печени визуализируются два кольцевидных очага, окруженных перифокальным отеком 34 × 30 мм. Состояние после реконструктивной операции на поджелудочной железе, панкреатоеюноанастомоз (ПЕА) на петле по Ру, абсцесс правой доли печени? На КТ-ангиографии: холедох не дифференцируется, внутрипеченочные желчные протоки расширены, в них воздух, портальная вена проходима (рис. 2), выявлено отсутствие контрастирования общей печеночной артерии, собственная печеночная артерия контрастируется через коллатерали (рис. 3). На фистулографии через наружный дренаж контрастируются внутрипеченочные протоки, холедох не контрастируется.
/153-2.gif)
Для ликвидации полного наружного желчного свища пациенту выполнено 3-е оперативное вмешательство. На операции: выраженный спаечный процесс, из рубцовых сращений и спаек выделены печень, желудок, ДПК, ПЕА и печеночно-двенадцатиперстная связка, при детальной ревизии которой установлено отсутствие гепатикохоледоха в печеночно-двенадцатиперстной связке. В воротах печени определяются правый и левый долевые печеночные протоки. С учетом отсутствия данных об интраоперационном повреждении холедоха можно предположить его ишемический некроз после первичного вмешательства с перевязкой общей печеночной артерии. Петля тонкой кишки по Ру, участвующая в ПЕА, недостаточно подвижна из-за рубцовых сращений и непригодна для формирования дополнительного желчеотводящего анастомоза. Учитывая интраоперационные находки, выполнена резекция участка печени в области ворот с мобилизацией долевых печеночных протоков с последующей бигепатикоеюностомией на сформированной второй петле по Ру. В раннем послеоперационном периоде развилась частичная несостоятельность бигепатикоеюноанастомоза с желчным затеком в подпеченочное пространство. На 3-и сутки после первичной операции выполнена релапаратомия с дополнительным дренированием, после чего состояние пациента стабилизировалось. На 10-е сутки после операции желчеистечение прекратилось. На 30-е сутки после операции пациент в удовлетворительном состоянии выписан из стационара.
Пациент через 4 месяца прошел плановое обследование. Жалоб не предъявляет, прибавил в массе 10 кг. Клинические и биохимические показатели в пределах нормы, по данным УЗИ, МРТ — диффузные изменения печени, незначительные признаки внутрипеченочного холестаза.
Заключение
Результаты приведенного клинического случая свидетельствуют о возможности успешного хирургического лечения хронического панкреатита с редким осложнением — гигантской псевдоаневризмой общей печеночной артерии. Развившееся массивное кровотечение потребовало интенсивной интраоперационной терапии кровопотери с массивной гемотрансфузией препаратов крови (4,5 л). С целью спасения жизни пациента применена технология damage control (контроля повреждений) [22, 23] с выполнением реконструктивного этапа операции через 3 суток после стабилизации его состояния. В послеоперационном периоде развилось ишемическое повреждение печени, которое купировалось восстановлением кровотока в собственной печеночной артерии по коллатералям из левой желудочной артерии и верхнебрыжеечной артерии через артериальную дугу в головке ПЖ на фоне интенсивной комплексной терапии с применением гепатопротекторов. Развившийся ишемический некроз холедоха привел к формированию полного желчного свища. Это ослож–нение потребовало выполнения дополнительной реконструктивной операции: бигепатикоеюностомии на второй петле по Ру.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Кригер А.Г. Ложные аневризмы артерий бассейна чревного ствола у больных хроническим панкреатитом / А.Г. Кригер, Л.С. Коков, Г.Г. Кармазановский, Г.И. Кунцевич, В.Д. Федоров, П.Б. Барбин, Н.В. Тарбаева // Хирургия. — 2008. — Т. 12. — С. 17-23.
2. Воробей А.В. Неязвенные гастроинтестинальные кровотечения / А.В. Воробей, В.В. Климович. — Минск: Полипринт, 2008. — C. 228.
3. Покровский А.В. Клиническая ангиология. Руководство в 2 томах. — М.: Медицина, 2004. — Т. 2. — С. 127-128.
4. Bergert H. Prevalence and treatment of bleeding complications in chronic pancreatitis / H. Bergert, F. Dobrowolski, S. Caffier et al. // Langenbecks. Arch. Surg. — 2004. — № 389. — P. 504-510.
5. Sparrow P. Ultrasonic-Guided Percutaneous Injection of Pancreatic Pseudoaneurysm with Thrombin / P. Sparrow, J. Asquith, N. Chalmers // Cardiovasc. Int Radiol. — 2003. — № 26. — P. 312-315.
6. Sharma P. Hemorrhage in acute pancreatitis: should gastrointestinal bleeding be considered an organ failure? / P. Sharma, K. Madan, P. Garg // Pancreas. — 2008. — № 36. — P. 141-145.
7. Kiviluoto T. Pseudocysts in chronic pancreatitis. Surgical results in 102 consecutive patients / T. Kiviluoto, L. Kivisaari, E. Kivilaakso, M. Lempinen // Arch. Surg. — 1989. — № 124. — P. 240-243.
8. Udd M. Treatment of bleeding pseudoaneurysms in patients with chronic pancreatitis / M. Udd, A.K. Leppäniemi, S. Bidel, P. Keto et al. // World J. Surg. — 2007. — № 31. — P. 504-510.
9. Balachandra S. Systematic appraisal of the management of the major vascular complications of pancreatitis / S. Balachandra, A.K. Siriwardena // Am. J. Surg. — 2005. — № 190. — P. 489-495.
10. Moringhini A. Pseudocysts in acute non-alcoholic pancreatitis: incidence and natural history / A. Moringhini, G. Uomo, R. Patti // Dg. Dis. Sci. — 1999. — № 44. — P. 1669-1673.
11. Ido К. Case of hemorrhagic pancreatic pseudocyst in which ultrasound imaging was useful / К. Ido, К. Isobe, К. Kimura et al. // Med. Ultrasonics. — 2004. — № 31. — P. 41-45.
12. Kane M.G. Pancreatic pseudocyst / M.G. Kane, G.J. Krejs // Adv. Intern. Med. — 1984. — № 29. — P. 271-300.
13. Chen H.L. Ruptured Pancreaticoduodenal Artery Pseudoaneurysm with Chronic Pancreatitis Presenting as Recurrent Upper Gastrointestinal Bleeding / H.L. Chen, W.H. Chang, S.C. Shih et al. // Dig. Dis. Sci. — 2006.
14. Ikeda О. Hemorrhage into pancreatic pseudocyst / О. Ikeda, S. Кirе, Y. Torigoe et al. // Abdom. Imaging. — 2006. — № 20. — P. 1-4.
15. Fukatsu K. A case of chronic pancreatitis in which endoscopic ultrasonography was effective in the diagnosis of a pseudoaneurysm / K. Fukatsu, K. Ueda, H. Maeda et al. // World J. Gastrointest. Endosc. — 2012. — № 4. — P. 335-338.
16. Balthazar E.J. Hemorrhagic complications of pancreatitis: radiologic evaluation with emphasis on CT imaging / E.J. Balthazar, L.A. Fisher // Pancreatology. — 2001. — № 1. — P. 306-313.
17. Bergert H. Management and outcome of hemorrhage due to arterial pseudoaneurysms in pancreatitis / H. Bergert, I. Hinterseher, S. Kersting et al. // Surgery. — 2005. — № 137. — P. 323-328.
18. De Perrot M. Management of bleeding pseudoaneurysms in patients with pancreatitis / M. De Perrot, T. Berney, L. Bühler et al. // Br. J. Surg. — 1999. — № 86. — P. 29-32.
19. Bhasin D.K. Non-surgical management of pancreatic pseudocysts associated with arterial pseudoaneurysm / D.K. Bhasin, S.S. Rana, V. Sharma et al. // Pancreato–logy. — 2013. — № 13. — P. 250-253.
20. Chong C.N. Ruptured gastroduodenal artery pseudo–aneurysm as the initial presentation of chronic pancreatitis / C.N. Chong, K.F. Lee, K.T. Wong et al. // Am. J. Surg. — 2009. — № 197. — P. 38-40.
21. Rotondo M.F. Damage Control — an approach for improved survival in exsanguinating penetrating abdominal injury / M.F. Rotondo, C.W. Schwab, M.D. McGonigal et al. // J. Trauma. — 1993. — № 35. — P. 375-382.
22. Germanos S. Damage control surgery in the abdomen: an approach for the management of severe injured patients / S. Gourgiotis, C. Villias, M. Bertucci et al. // Int. J. Surg. — 2008 Jun. — № 6(3). — P. 246-52.

/152-1.gif)
/153-1.gif)
/153-2.gif)