Вступ
Алергічний риніт залишається глобальною медико-соціальною проблемою [1, 2]. За епідеміологічною оцінкою, 10–25 % населення хворіють на алергічний риніт [3]. Серед дітей цей показник досягає 30 % [4].
Алергічний риніт є фактором ризику розвитку таких серйозних захворювань, як бронхіальна астма, отит, синусит [2]. Мінімальна персистенція алергічного запалення слизової носа також призводить до частіших вірусних респіраторних захворювань. Тому з метою зниження ризику розвитку ускладнень та підвищення якості життя пацієнти повинні отримувати адекватне лікування алергічного риніту [5].
У патогенезі більшості симптомів алергічних захворювань найважливіша роль належить гістаміну, що обґрунтовує широке використання антагоністів Н1-рецепторів гістаміну як основних протиалергійних лікарських засобів [6], серед яких усе більш популярними стають антигістамінні препарати другого та третього покоління [7].
Такий вибір обумовлений їх порівнянною ефективністю та більш низькою частотою побічних ефектів порівняно з аналогами першого покоління [7–9].
Ці препарати необхідно застосовувати не тільки в період загострення алергічного захворювання, але й після того, як запалення ліквідовано, що допомагає прискорити процес одужання [10].
Представником антагоністів рецепторів гістаміну третього покоління з високою селективністю до H1-рецепторів, що призначається для лікування алергічних захворювань у дітей, є левоцетиризин [11, 12].
Левоцетиризин — це R-енантіомер, або активний ізомер цетиризину. Здатність зв’язуватися і тривалість зв’язку з Н1-рецептором у левоцетиризину в два рази перевищують афінність цетиризину та приблизно в 30 разів — афінність декстроцетиризину [13].
Вибірковість левоцетиризину щодо Н1-гістамі–нових рецепторів у 600 разів вища, ніж з іншими рецепторами, що призводить практично до відсутності антихолінергічної та антисеротонінової дії [14].
Левоцетиризин швидко всмоктується в кишечнику, досягаючи максимальної концентрації в плазмі через 0,5–1 годину після прийому [15]. Доведено, що в організмі людини левоцетиризин не піддається інверсії, тобто не відбувається утворення декстроцетиризину, що свідчить про стабільність речовини [13].
Ступінь всмоктування левоцетиризину не залежить від прийому їжі та дози препарату. Препарат майже повністю потрапляє в системний кровотік, тому його біодоступність близька до 100 %. З кишечника левоцетиризин транспортується в печінку, а звідти надходить у кровотік.
Левоцетиризин є кінцевим метаболітом, тому для його активації не потрібен печінковий метаболізм. Левоцетиризин не взаємодіє з цитохромом печінки P450, за рахунок чого не має конкурентної медикаментозної взаємодії [15, 16].
Результати рандомізованих контрольованих клінічних випробувань свідчать про клінічну ефективність левоцетиризину при лікуванні алергічного риніту та про його високий профіль безпеки як у дорослих, так і в дітей [17–20].
Левоцетиризин практично не проникає через гематоенцефалічний бар’єр, у зв’язку з чим він практично не проявляє седативного ефекту [21]. Проведений метааналіз, у який було включено 18 014 пацієнтів різного віку, підтвердив наявність мінімального седативного ефекту препарату [22]. Навіть тривале застосування левоцетиризину в дітей є безпечним та не пов’язане з несприятливим впливом на центральну нервову систему [23].
Левоцетиризин не справляє кардіотоксичної дії [15]. Доведено, що при застосуванні препарату не відбувається гематологічних, біохімічних або електрокардіографічних порушень; також не було виявлено негативного впливу препарату на фізичний розвиток, поведінку або навчання дітей. При цьому частота побічних ефектів левоцетиризину не відрізнялася від плацебо [17, 24–26].
Мета дослідження: вивчення ефективності та переносимості антигістамінного препарату L-Цет (левоцетиризин) у дітей, хворих на алергічний риніт.
Матеріали та методи
Під наглядом перебувало 30 дітей віком від 4 до 7 років, у яких згідно з Протоколом лікування дітей, хворих на алергічний риніт (Наказ МОЗ України № 767 від 27.12.2005 р.), на підставі анамнестичного, загальноклінічного та лабораторно-інструментального обстеження було діагностовано алергічний риніт середньої тяжкості, період загострення.
Загальна оцінка симптомів алергічного риніту проводилася за шкалою RTSS4 (Rhinitis Total Symptom Score) [27], яка включала 4 симптоми:
— закладеність носа;
— свербіж носа;
— чхання;
— ринорея.
Кожен симптом залежно від ступеня прояву оцінювали від 0 (відсутність симптомів) до 3 балів (тяжкий) (табл. 1).
Оцінка за шкалою RTSS4 проводилася до початку терапії, на 14-й та 30-й день терапії. При зниженні загальної бальної оцінки на 3 бали та більше терапія вважалася ефективною [27].
До комплексу лікування алергічного риніту всім дітям був включений антигістамінний препарат системної дії L-Цет (левоцетиризин) у вигляді сиропу, виробництва ТОВ «Кусум Фарм», Україна. Сироп L-Цет призначали дітям віком до 6 років по 1,25 мг (2,5 мл) 2 рази на добу, а дітям віком понад 6 років — по 5 мг (10 мл) 1 раз на добу.
Додатково для оцінки клінічної безпеки застосування препарату L-Цет сироп до початку лікування та через 4 тижні терапії проводили дослідження гемограми, біохімічних показників крові та електрокардіограму.
Результати й обговорення
Проведена оцінка клінічних проявів алергічного риніту до початку лікування показала наявність закладеності носа у 100,0 % пацієнтів, назального свербежу — у 23 (76,7 %), чхання — у 27 (90,0 %), ринореї — у 30 (100 %) хворих. При цьому бальна оцінка кожного із симптомів за шкалою RTSS4 відповідала 2–3 балам. Загальний бал за симптомами алергічного риніту становив 9,83 ± 0,25 бала. Аналіз результатів алергологічного дослідження виявив у 21 (70,0 %) пацієнта полісенсибілізацію до пилкових та/або побутових алергенів.
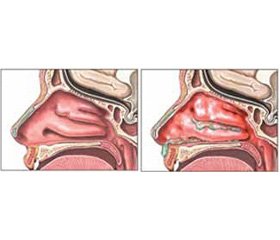
При риноскопічному дослідженні під час першого огляду в усіх дітей (100 %) були виявлені специфічні зміни у вигляді набряку носових раковин, потовщення слизової оболонки перегородки носа, блідості або ціанозу слизової оболонки носових раковин, значної кількості слизового секрету.
Включення препарату L-Цет до терапії дітей, хворих на алергічний риніт, мало позитивний терапевтичний ефект.
Аналіз клінічних симптомів на фоні застосованої терапії встановив поліпшення загального стану в більшості дітей на 3-тю — 4-ту добу: знизилася інтенсивність свербежу, зменшилося чхання, поліпшився сон.
На 14-ту добу терапії загострення алергічного риніту в усіх хворих було відзначено значну позитивну динаміку, що в першу чергу відображалося на поліпшенні носового дихання (табл. 2).
У всіх пацієнтів відзначене помірне зменшення ознак закладеності носа (2,50 ± 0,17 бала до початку лікування та 2,00 ± 0,14 бала на 14-й день терапії; р < 0,05). Це супроводжувалося зниженням інтенсивності свербежу носа на 43,5 %, чхання — на 46,8 %, ознак ринореї — на 36,4 % (р < 0,05). При цьому загальна бальна оцінка за шкалою RTSS4 становила 6,43 ± 0,13 бала.
Через 4 тижні лікування повне відновлення носового дихання спостерігалося в 16 (53,3 %) хворих. У інших 14 (46,7 %) дітей протягом дня відзначали легку закладеність носа, що за шкалою RTSS4 була оцінена в 1 бал. Легкий свербіж носа та чхання, оцінка яких також відповідала 1 балу, зберігалися в 10 (30,3 %) пацієнтів. Неінтенсивна ринорея, яка спостерігалася при контакті з причинно-значущим алергеном, зберігалася у 8 (26,7 %) дітей. Загальна бальна оцінка симптомів алергічного риніту за шкалою RTSS4 через 30 днів застосування левоцетиризину зменшилася в 6,9 раза й становила 1,43 ± 0,16 бала.
Позитивну динаміку було відзначено й при риноскопічному дослідженні. Спостерігалося зниження набряку носових раковин, зменшення або повна відсутність слизового секрету, нормалізація кольору слизової оболонки носових раковин.
Препарат добре переносився всіма пацієнтами. Завдяки його одно- чи двократному прийому досягався високий комплаєнс-контроль.
Тривале застосування левоцетиризину не викликало в жодної дитини побічних реакцій, у тому числі й з боку центральної нервової системи.
Змін біохімічних показників, що характеризують стан нирок та печінки, виявлено не було. Порушень функції серцево-судинної системи також не було зареєстровано, що підтверджували результати ЕКГ.
Висновки
1. Препарат L-Цет (левоцетиризин) проявляє хороший клінічний ефект у дітей, хворих на алергічний риніт, що підтверджується позитивною динамікою бальної оцінки за шкалою RTSS4 та рино–скопічної картини.
2. Препарат добре переноситься, має високу безпеку та може бути рекомендований для застосування в комплексній терапії алергічного риніту в дітей.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Brożek JL, Bousquet J, Baena-Cagnani CE, Bonini S, Canonica GW, Casale TB, Schünemann HJ. Allergic rhinitis and its impact on asthma (ARIA) guidelines: 2010 revision. J Allergy Clin Immunol. 2010 Sep;126(3):466-76. doi: 10.1016/j.jaci.2010.06.047.
2. Antypkin YuG, Lapshyn VF, Umanets TR, Kondratenkova TV. [Efficacy of L-cet use in children with seasonal allergic rhinitis. Zdorov’ye Rebenka. 2013;8(51):21-3. (In Ukrainian). doi: 10.22141/2224-0551.8.51.2013.84951.
3. Fang SY, Perng DW, Lee JY, Lin DY, Huangs CY. An open-label, multicentre study of levocetirizine for the treatment of allergic rhinitis and urticaria in Taiwanese patients. Chin J Physiol. 2010 Aug;53(4):199-207. doi: 10.4077/CJP.2010.AMK007.
4. Melamed I, Heffron M. Attention Deficit Disorder and Allergic Rhinitis: Are They Related? Journal of Immunology Research. 2016;2016:6. doi: 10.1155/2016/1596828.
5. Sidorovich OI, Luss LV. Modern approaches to the treatment of allergic rhinitis. Astma i allergija 2015;4:27-32. (In Russian).
6. Kurbacheva OM, Gushchin IS. Kestine in treatment of perennial rhinitis in adults and child. Rossijskij Allergologicheskij Zhurnal. 2004;4:75-8. (In Russian).
7. Davis S. Summer "sniffles": ear, nose and throat. SA Pharmacist's Assistant. 2015;15(4): 8-10.
8. Phan H, Moeller ML, Nahata MC. Treatment of allergic rhinitis in infants and children: efficacy and safety of second-generation antihistamines and the leukotriene receptor antagonist montelukast. Drugs. 2009;69(18):2541-76. doi: 10.2165/9884960-000000000-00000.
9. Sur DK, Scandale S. Treatment of allergic rhinitis. Am Fam Physician. 2010;81:1440-6. PMID: 20540482.
10. Bialiayeva LM, Mikulchik NV, Panulina NI. Allergic rhinitis in children: current diagnostic, treatment and prophilactic. Mezhdunarodnye Obzory: Klinicheskaja Praktika i Zdorov'ye. 2013;2(221): 34-9. (In Russian).
11. Olasińska-Wiśniewska A, Olasiński J, Grajek S. Cardiovascular safety of antihistamines. Advances in Dermatology and Allergology. 2014;31(3):182-6. doi: 10.5114/pdia.2014.43191.
12. Carnovale C, Russo S, Biondelli G, Gentili M, Pozzi M, Antoniazzi S, Clementi E. Levocetirizine-induced psychiatric disorders in a pediatric patient: A case report and a pharmacovigilance database analysis. Journal of Pharmacology and Pharmacotherapeutics. 2017;8(2):74-6. doi: 10.4103/jpp.JPP_14_17.
13. Trusova OV, Korostovtsev DS. Levotsetirizin (Ksizal). Harakteristika preparata i opyit klinicheskogo primeneniya [Levocetirizine (Xyzal). The characteristics of the drug and clinical experience]. Allergologiya. 2006;2:25-31. (In Russian).
14. Gillard M, Christophe B, Wels B, Peck M, Massingham R, Chatelain P. H1 antagonists: receptor affinity versus selectivity. Inflammation Research. 2003;52:49-50. doi: 10.1007/s000110300050.
15. Astafieva NG, Gamova IV, Udovichenko EN, Perfilova IA. Levocetirizine: modern aspects of the use in allergic diseases in terms of evidence-based medicine. Lechaschiy vrach. 2010;5(5):62. (In Russian).
16. Kondyurina EG, Zelenskaya VV. The antihistamines in the control of allergic diseases in children. Rossiyskiy Meditsinskiy Zhurnal. 2012;2:56-8. (In Russian).
17. De Blic J, Wahn U, Billard E, Alt R, Pujazon MC. Levocetirizine in children: evidenced efficacy and safety in a 6-week randomized seasonal allergic rhinitis trial. Pediatr Allergy Immunol. 2005;16(3):267-75. doi: 10.1111/j.1399-3038.2005.00216.x.
18. Potter PC; Paediatric Levocetirizine Study Group. Efficacy and safety of levocetirizine on symptoms and health-related quality of life of children with perennial allergic rhinitis: a double-blind, placebo-controlled randomized clinical trial. Ann Allergy Asthma Immunol. 2005;95(2):175-80. doi: 10.1016/S1081-1206(10)61208-2.
19. Dubuske LM. Levocetirizine: The latest treatment option for allergic rhinitis and chronic idiopathic urticaria. Allergy Asthma Proc. 2007;28(6):724-34. doi: 10.2500/aap.2007.28.3051.
20. Simons FE; Early Prevention of Asthma in Atopic Children Study Group. H1-antihistamine treatment in young atopic children: effect on urticaria. Ann Allergy Asthma Immunol. 2007;99(3):261-6. doi: 10.1016/S1081-1206(10)60662-X.
21. McDonald K, Trick L, Boyle J. Sedation and antihistamines: an update. Review of inter-drug differences using proportional impairment ratios. Hum. Psychopharmacol. 2008;23(7):555-70. doi: 10.1002/hup.962.
22. Snidvongs K, Seresirikachorn K, Khattiyawittayakun L, Chitsuthipakorn W. Sedative Effects of Levocetirizine: A Systematic Review and Meta-Analysis of Randomized Controlled Studies. Drugs. 2017;77(2):175-86. doi: 10.1007/s40265-016-0682-0.
23. Ten Eick AP, Blumer JL, Reed MD. Safety of antihistamines in children. Drug safety. 2001;24(2):119-47. doi: 10.2165/00002018-200124020-00003.
24. Hulhoven R, Rosillon D, Letiexhe M, Meeus MA, Daoust A, Stockis A. Levocetirizine does not prolong the QT/QTc interval in healthy subjects: results from a thorough QT study. European journal of clinical pharmacology. 2007;63(11):1011-7. doi: 10.1007/s00228-007-0366-5.
25. Pasquali M, Baiardini I, Rogkakou A, Riccio AM, Gamalero C, Descalzi D, Canonica GW. Levocetirizine in persistent allergic rhinitis and asthma: effects on symptoms, quality of life and inflammatory parameters. Clinical & Experimental Allergy, 2006;36(9):1161-7. doi: 10.1111/j.1365-2222.2006.02548.x.
26. Van Bever HP, Samuel ST, Lee BW. Halting the allergic march. World Allergy Organization Journal. 2008;1(4):57-62. doi: 10.1097/WOX.0b013e31816ddbc1.
27. Bousquet PJ, Combescure C, Klossek JM, Daurès JP, Bousquet J. Change in visual analog scale score in a pragmatic randomized cluster trial of allergic rhinitis. Journal of Allergy and Clinical Immunology. 2009;123(6):1349-54. doi: 10.1016/j.jaci.
2009.02.033.

/26-1.jpg )
/27-1.jpg )