Резюме
Актуальність. Одним із побічних ефектів дії цефалоспоринів ІІІ покоління є формування цефалоспориніндукованого біліарного псевдолітіазу (ЦІБПЛ). Мета. Вивчити особливості формування біліарного сладжа при застосуванні цефалоспоринів ІІІ покоління в терапії гострих респіраторних інфекційних захворювань у дітей. Матеріали та методи. Обстежено 46 дітей віком від 2 до 15 років з гострими респіраторними інфекційними захворюваннями, які отримували в терапії цефалоспорини ІІІ покоління парентеральним шляхом введення у вікових дозах. У всіх дітей до початку лікування і після закінчення антибіотикотерапії оцінювали показники біохімічного дослідження крові і дані ехосонографії (ультразвукове дослідження) біліарного тракту. Результати. За даними УЗД у 10 пацієнтів (21,7 %) з гострими респіраторними інфекційними захворюваннями після проведеного курсу терапії цефалоспоринами ІІІ покоління виявлено неоднорідний вміст у просвіті жовчного міхура у вигляді гіперехогенного субстрату, що свідчило про формування ЦІБПЛ. Середній вік пацієнтів із ЦІБПЛ становив 9,05 ± 1,44 року і перебував у межах від 4 до 15 років. Встановлено, що у 60 % обстежених дітей формування ЦІБПЛ протікало субклінічно. Результати біохімічного дослідження сироватки крові показали, що у дітей із ЦІБПЛ спостерігалося підвищення активності аланінамінотрансферази, аспартатамінотрансферази і лужної фосфатази. Було встановлено, що ЦІБПЛ відзначається у 22,9 % дітей на тлі терапії цефтріаксоном, у 9 % пацієнтів — цефтазидимом. Біліарний сладж формувався у 54,5 % хворих, які отримували цефтріаксон у високих дозах (100 мг/кг/добу), і в 75 % випадків — після 10-денного застосування даного антибіотика. Висновки. Отримані результати показали, що на тлі застосування цефалоспоринів ІІІ покоління при терапії гострих респіраторних інфекційних захворювань у 21,7 % хворих дітей відбувається формування ЦІБПЛ. Особливо високий ризик розвитку ЦІБПЛ відзначається при використанні високих доз цефтріаксону і пролонгованої терапії цефалоспоринами.
Актуальность. Одним из побочных эффектов действия цефалоспоринов ІІІ поколения является формирование цефалоспорининдуцированного билиарного псевдолитиаза (ЦИБПЛ). Цель. Изучить особенности формирования билиарного сладжа при применении цефалоспоринов ІІІ поколения в терапии острых респираторных инфекционных заболеваний у детей. Материалы и методы. Обследовано 46 детей возрастом от 2 до 15 лет с острыми респираторными инфекционными заболеваниями, которые получали в терапии цефалоспорины ІІІ поколения парентеральным путем введения в возрастных дозировках. У всех детей до начала лечения и после окончания антибиотикотерапии оценивали показатели биохимического исследования крови и данные эхосонографии (ультразвуковое исследование) билиарного тракта. Результаты. По данным УЗИ у 10 пациентов (21,7 %) с острыми респираторными инфекционными заболеваниями после проведенного курса терапии цефалоспоринами ІІІ поколения выявлено неоднородное содержимое в просвете желчного пузыря в виде гиперэхогенной взвеси, что свидетельствовало о формировании ЦИБПЛ. Средний возраст пациентов с ЦИБПЛ составлял 9,05 ± 1,44 года и находился в границах от 4 до 15 лет. Установлено, что у 60 % обследуемых детей формирование ЦИБПЛ протекало субклинически. Результаты биохимического исследования сыворотки крови показали, что у детей с ЦИБПЛ наблюдалось повышение активности аланинаминотрансферазы, аспартатаминотрансферазы и щелочной фосфатазы. Было установлено, что ЦИБПЛ отмечается у 22,9 % детей на фоне терапии цефтриаксоном, у 9 % пациентов — цефтазидимом. Билиарный сладж формировался у 54,5 % больных, получавших цефтриаксон в высоких дозах (100 мг/кг/сут), и в 75 % случаев — после 10-дневного применения данного антибиотика. Выводы. Полученные результаты показали, что на фоне применения цефалоспоринов ІІІ поколения при терапии острых респираторных инфекционных заболеваний у 21,7 % больных детей происходит формирование ЦИБПЛ. Особенно высокий риск развития ЦИБПЛ отмечается при использовании высоких доз цефтриаксона и пролонгированной терапии цефалоспоринами.
Background. One of the side effects of the third generation cephalosporins is the formation of cephalosporin-induced biliary pseudolithiasis (CIBPL). The purpose of the study was to establish the peculiarities of the formation of biliary sludge during the application of the third generation cephalosporins in the treatment of acute respiratory infections in children. Materials and methods. We examined 46 children aged 2 to 15 years with acute respiratory infections. Сephalosporins were administered intravenously in age doses. We evaluated the biochemical blood test and the echosonography (ultrasound) of the biliary tract before the treatment and after the end of antibiotic therapy of all children. Results. According to ultrasound data, in 10 patients (21.7 %) with acute respiratory infections, after a course of therapy with the third generation cephalosporins, heterogeneous contents were detected in the gallbladder lumen in the form of a hyperechoic suspension, which indicated the formation of CIBPL. The average age of patients with CIBPL was 9.05 ± 1.44 years and was within the range of 4 to 15 years. We found that in 60 % of the examined children, the formation of CIBPL proceeded subclinically. The results of a biochemical study of blood serum showed that in children with CIBPL, an increase in the activity of alanine aminotransferase, aspartate aminotransferase, and alkaline phosphatase was observed. It was found that CIBPL is detected in 22.9 % of children against the background of ceftriaxone therapy, in 9 % of patients — ceftazidime. Biliary sludge was formed in 54.5 % of patients receiving ceftriaxone in high doses (100 mg/kg/day), and in 75 % of cases after 10 days of using this antibiotic. Conclusions. The obtained results showed that against the background of using third generation cephalosporins in the treatment of acute respiratory infections, 21.7 % of children had CIBPL. A particularly high risk of developing CIBPL is observed when using high doses of ceftriaxone and prolonged therapy with cephalosporins.
Введение
Одними из основных и широко применяемых в педиатрической практике классов антибактериальных препаратов являются цефалоспорины ІІІ поколения. Выбор врача в пользу данных антибиотиков обусловлен их высокой терапевтической эффективностью за счет широкого спектра антимикробной активности в отношении грамотрицательных и грамположительных бактерий при различных инфекционных заболеваниях, длительным периодом полувыведения, а также высоким профилем безопасности [1–5].
Результаты современных исследований показывают, что одним из побочных эффектов действия цефалоспоринов ІІІ поколения является нарушение однородности желчи [1, 6–9]. Данный феномен получил название «цефалоспорининдуцированный билиарный псевдолитиаз» (ЦИБПЛ). Билиарный сладж чаще развивается на фоне применения цефтриаксона (15–57 %) [6, 7, 9], но встречается и при использовании цефотаксима (5,9 %) [10] и цефтазидима (2 %) [11]. Считалось, что формирование преципитатов в полости желчного пузыря на фоне применения цефтриаксона носит исключительно транзиторный характер [6, 7], однако результаты исследований последних лет опровергают абсолютную обратимость ЦИБПЛ. Установлено, что в 2–20 % случаев у детей возможно развитие самостоятельно обратимого ЦИБПЛ [12–14]. Цефалоспорининдуцированный билиарный сладж в большинстве случаев протекает субклинически, только у некоторых пациентов наблюдается возникновение типичных жалоб и симптоматики, свидетельствующих о поражении билиарной системы [11, 15]. В связи с этим основным методом диагностики ЦИБПЛ является эхографическое исследование билиарной системы: его чувствительность составляет 55–65 %, а специфичность — более 90 %.
Группой ученых под руководством Han Z. Park [16] впервые был проведен анализ химической структуры преципитатов в полости желчного пузыря у больных с ЦИБПЛ с использованием тонкослойной хроматографии, высокоразрешающей жидкостной хроматографии и электронного микрозондирования. Установлено, что при билиарном сладже, индуцированном цефтриаксоном, основным компонентом осадка желчи является кальциевая соль цефтриаксона, а также в преципитате содержится небольшое количество гранул билирубина и кристаллов моногидрата холестерина [16]. В последние годы проведен ряд исследований, определяющих дозы и длительность применения цефалоспоринов ІІІ поколения, при которых становится возможным формирование билиарного сладжа [6–9, 11].
Цель исследования: изучить особенности формирования билиарного сладжа при применении цефалоспоринов ІІІ поколения в терапии острых респираторных инфекционных заболеваний у детей.
Материалы и методы
Проведено комплексное обследование 46 детей в возрасте от 2 до 15 лет, которые находились на стационарном лечении в КУ «Днепропетровская городская детская клиническая больница № 1» ДОР с острыми бактериальными респираторными инфекционными заболеваниями. Верификацию диагноза и оказание медицинской помощи проводили в соответствии с приказами МЗ Украины от 13.01.2005 № 18 и от 16.07.2014 № 499. Все пациенты с момента поступления в стационар получали цефалоспорины ІІІ поколения парентерально в возрастных дозировках.
До начала лечения и после окончания антибиотикотерапии всем детям проводилось биохимическое исследование крови и эхосонография (ультразвуковое исследование (УЗИ)) билиарного тракта. Биохимические показатели сыворотки крови определяли по стандартным методикам: содержание общего белка, общего билирубина и его фракций, общего холестерина, щелочной фосфатазы (ЩФ), аспартатаминотрансферазы (АсАТ), аланинаминотрансферазы (АлАТ), тимоловая проба.
Статистическую обработку результатов проводили с использованием общепринятых математических методов вариационной статистики.
Результаты и обсуждение
Средний возраст обследованных детей составил 6,21 ± 0,56 года и варьировал от 2 до 15 лет. Соотношение мальчиков и девочек практически не отличалось (52,2 и 47,8 % соответственно). На основании клинико-анамнестических данных и лабораторно-инструментальных исследований всем детям был установлен клинический диагноз. В соответствии с приказами МЗ Украины от 13.01.2005 № 18 и от 16.07.2014 № 499 в зависимости от установленного клинического диагноза и степени тяжести заболевания всем детям была назначена терапия цефалоспоринами ІІІ поколения в соответствующих дозах парентеральным путем введения. Длительность применения антибиотиков определялась выраженностью клинических проявлений с учетом положительного эффекта от проводимой терапии. По результатам эхосонографии билиарной системы у всех обследованных детей до назначения антибиотикотерапии не наблюдалось патологических изменений. После проведенного курса терапии цефалоспоринами ІІІ поколения у 10 пациентов (21,7 %) с острыми респираторными инфекционными заболеваниями по данным ультразвукового исследования билиарного тракта выявлено неоднородное содержимое в просвете желчного пузыря в виде гиперэхогенной взвеси, что свидетельствовало о формировании ЦИБПЛ.
Средний возраст пациентов с ЦИБПЛ составлял 9,05 ± 1,44 года и находился в границах от 4 до 15 лет. Данный факт соответствует исследованию, проведенному Lokman Ustoyl и соавт. [10], в результате которого авторы установили, что у детей старше 4,5 года значительно возрастает риск развития ЦИБПЛ. По гендерному признаку отличий не наблюдалось (мальчиков — 50 %, девочек — 50 %).
В ходе исследования установлено, что у 60 % обследуемых детей формирование ЦИБПЛ протекало бессимптомно. Однако у 40 % пациентов основные клинические симптомы ЦИБПЛ проявлялись в виде жалоб на чувство тяжести и ноющие боли в правом подреберье, возникающие после погрешности в диете (20 %), жалоб на пониженный аппетит (10 %), тошноту (20 %), нарушение стула (20 %). При этом наблюдалось и сочетание этих симптомов у одних и тех же детей. При объективном исследовании: болезненность при пальпации в правом подреберье (30 %), положительные симптомы Кера, Мерфи (30 %), болезненность в панкреатических точках Дежардена, Мейо — Робсона, зоне Шоффара (10 %).
Результаты биохимического исследования сыворотки крови после проведенной антибиотикотерапии у обследованных детей представлены в табл. 1.
Установлено, что у пациентов с билиарным сладжем практически не изменилось содержание общего белка, холестерина в сыворотке крови. У детей с ЦИБПЛ определялось повышение активности АлАТ, АсАТ и щелочной фосфатазы, что указывало на наличие цитолитического и холестатического синдромов.
При обследовании наблюдаемых нами детей с острыми респираторными инфекционными заболеваниями было выявлено, что частота формирования ЦИБПЛ обусловлена назначенным антибиотиком, его дозой и длительностью применения. Так, при использовании цефтриаксона ЦИБПЛ наблюдался у 22,9 % детей, цефтазидима — у 9 % пациентов.
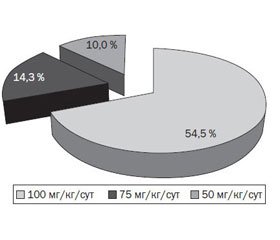
В ходе исследования установлено, что билиарный сладж формировался в большинстве случаев у больных, получавших цефтриаксон в высоких дозах (рис. 1).
При проведении анализа длительности курса антибактериальной терапии выявили, что ЦИБПЛ чаще (75 %) определялся у пациентов после 10-дневного применения цефтриаксона. Формирование билиарного сладжа при использовании цефтриаксона в течение 7 дней происходило у 18,8 % детей, 5 дней — у 8,3 % больных.
Несмотря на то, что применение высоких доз и пролонгированной терапии цефтриаксоном ассоциировано с риском развития ЦИБПЛ, назначение низких доз цефтриаксона не исключает возможности формирования псевдолитиаза.
Выводы
1. Применение цефалоспоринов ІІІ поколения при лечении острых респираторных инфекционных заболеваний у 21,7 % детей приводит к формированию билиарного сладжа.
2. Развитие цефалоспорининдуцированного билиарного псевдолитиаза у детей высоко ассоциировано с использованием высоких доз цефтриаксона и пролонгированной цефалоспориновой терапии.
3. У большинства детей формирование цефалоспорининдуцированного билиарного псевдолитиаза носит бессимптомный характер. Для своевременной диагностики цефалоспорининдуцированного билиарного псевдолитиаза рекомендуется проведение ультразвукового исследования билиарного тракта после цефалоспориновой терапии.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Абатуров А.Е. Цефалоспоринассоциированный билиарный псевдолитиаз / А.Е. Абатуров, Н.Ю. Завгородняя // Здоровье ребенка. — 2017. — Т. 12, № 2. — С. 73-78.
2. Волосовец А.П. Рациональная антибиотикотерапия респираторных заболеваний у детей / Волосовец А.П., Юлиш Е.И. — Донецк: Регина, 2005. — 389 с.
3. Хайтович Н.В. Цефалоспорины при лечении респираторных заболеваний в амбулаторно-поликлинической практике педиатра / Н.В. Хайтович // Здоровье ребенка. — 2013. — № 1(44). — С. 141-145.
4. Леженко Г.А. Обоснование рациональной антибиотикотерапии бактериальных заболеваний респираторного тракта у детей / Г.А. Леженко, Е.Е. Пашкова // Здоровье ребенка. — 2016. — № 2(70). — С. 33-38.
5. Zaffiri L. History of antibiotics. From salvarsan to cephalosporins / L. Zaffiri, J. Gardner, L.H. Toledo-Pereyra // J. Invert. Surg. — 2012. — Vol. 25, № 2. — P. 67-77. — doi: 10.3109/08941939.2012.664099.
6. Biner B. Ceftriaxone-associated biliary pseudolithiasis in children / B. Biner, N. Oner, C. Celtik, M. Bostancioğlu, N. Tunçbilek, A. Güzel et al. // J. Clin. Ultrasound. — 2006. — Vol. 34. — P. 217-228. — DOI: 10.1002/jcu.20228.
7. Choi Y.Y. Gallbladder pseudolithiasis caused by ceftriaxone in young adult / Y.Y. Choi, Y.H. Jung, S.M. Choi, Ch.S. Lee, D. Kim, K.Y. Hur // J. Korean Surg. Soc. — 2011. — Vol. 1, № 6. — P. 423-426. — doi: 10.4174/jkss.2011.81.6.423.
8. Murata S. Fasting and bed rest, even for a relatively short period, are risk factors for ceftriaxone-associated pseudolitiasis / S. Murata, T. Aomatsu, A. Yoden, H. Tamai // Pediatr. Int. — 2015. — Vol. 5, № 5. — P. 942-946. — doi: 10.1111/ped.12625.
9. Rodríguez Rangel D.A. Gallstones in association with the use of ceftriaxone in children / D.A. Rodríguez Rangel, A.P. Pinilla Oreja–rena, M. Bustacara Diaz et al. // Ann. Pediatr. (Barc). — 2014. — Vol. 80, № 2. — P. 77-80. — doi: 10.1016/j.anpedi.2013.04.001.
10. Ustyol L. Comparative evaluation of ceftriaxone- and cefota–xime-induced biliary pseudolithiasis or nephrolithiasis: A prospective study in 154 children / L. Ustyol, M.D. Bulut, K. Agengin et al. // Hum. Exp. Toxicol. — 2016. — Vol. 10. — Рii: 0960327116658108. — doi: 10.1177/0960327116658108.
11. Meng D. Sonographic assessment of ceftriaxone-associated pseudolithiasis in Chinese children / D. Meng, Y. Cao, J. Fu et al. // J. Int. Med. Res. — 2010. — Vol. 38, № 6. — P. 2004-2010. — doi: 10.1177/147323001003800614.
12. Nayak A. Ceftriaxone-Induced Gallstones: Case Report and Li–terature Review / A. Nayak, A. Slivka // ACG Case Rep. J. — 2014. — Vol. 1, № 3. — P. 170-172. — doi: 10.14309/crj.2014.40.
13. Serdaroglu F. Gallstones in childhood: etiology, clinical features, and prognosis / F. Serdaroglu, Y.S. Koca, F. Saltik et al. // Eur. J. Gastroenterol. Hepatol. — 2016. — Vol. 28, № 12. — P. 1468-1472. — doi: 10.1097/MEG.0000000000000726.
14. Tuna Kirsaclioglu C. Risk factors, complications and outcome of cholelithiasis in children: A retrospective, single-centre review / C. Tuna Kirsaclioglu, B. Çuhaci Çakir, G. Bayram et al. // J. Paediatr. Child. Health. — 2016. — Vol. 52, № 10. — P. 944-949. — doi: 10.1111/jpc.13235.
15. Oh T.H. Ceftriaxone-Induced Gallstone / T.H. Oh, Y.C. Lee, H.K. Yang // Clinical Ultrasound. — 2016. — Vol. 1, № 2. — P. 111-114. — doi: 10.18525/cu.2016.1.2.111.
16. Park H.Z. Ceftriaxone-associated gallbladder sludge. Identification of calcium-ceftriaxone salt as a major component of gallbladder precipitate / H.Z. Park, S.P. Lee, A.L. Schy // Gastroentero–logy. — 1991. — Vol. 100, № 6. — P. 1665-1670. — PMID: 2019372.

/31-1.jpg )
/31-2.jpg )