Резюме
Актуальність. Галактоземія І типу, або класична галактоземія (КГ), — найбільш тяжка форма спадкових порушень обміну вуглеводів, зокрема галактози. Галактоземія не включена до програми масового неонатального скринінгу в Україні. КГ характеризується неспецифічністю дебютних симптомів, супроводжується високими показниками смертності у неонатальному періоді. Актуальними є питання ранньої діагностики та лікування КГ за відсутності програми масового неонатального скринінгу в Україні. Мета. Аналіз клініко-лабораторних, молекулярно-генетичних особливостей КГ; визначення комплексу клінічних симптомів щодо формування селективних груп пацієнтів для призначення дієтотерапії та проведення лабораторної діагностики; розробка поетапної схеми ефективної ранньої діагностики та лікування пацієнтів при КГ за відсутності масового неонатального скринінгу з метою запобігання інвалідизації хворих, зниження показника дитячої смертності. Матеріали та методи. Впродовж 2014–2017 рр. у Центрі орфанних захворювань обстежено 317 пацієнтів із діагнозом «гепатит невизначеного генезу». Вік хворих — від 3 днів до 16 років. Хлопчиків було 145 (45 %), дівчаток — 172 (55 %). У всіх пацієнтів відзначена полісиндромна клінічна картина з переважним ураженням печінки. В усіх пацієнтів визначали активність ферменту GАLT в еритроцитах периферичної крові, проводили ДНК-дослідження з метою виявлення мажорних мутацій у гені GАLT. Всі хворі були обстежені на наявність вірусних гепатитів. За результатами біохімічного дослідження визначали рівень печінкових трансаміназ, лужної фосфатази, білірубіну, показники згортання крові. Також проводили тандемну мас-спектрометрію з метою виявлення порушень обміну амінокислот, органічних кислот і мітохондріального бета-окислення жирних кислот. У 5 пацієнтів за наявності припущення про глікогеноз проведене кількісне визначення глікогену у біоптаті печінки. Результати. Діагноз КГ підтверджений у 15 (4,7 %) з 317 пацієнтів: у 9 хлопчиків і 6 дівчаток віком від 14 діб до 15 років. У 13 (86,7 %) дітей клінічний діагноз КГ встановлений у середньому через 47 ± 15 діб життя. У 2 пацієнтів КГ діагностована у віці 2 і 15 років. У всіх пацієнтів активність ферменту GALT в еритроцитах була знижена і становила 0,08–5,8 Од/г Hb, у середньому 3,3 ± 1,6 Од/г Hb (в нормі > 10 Од/г Hb). Молекулярно-генетичний аналіз проведений у 14 (93,3 %) пацієнтів. У 5 хворих виявлений гомозиготний генотип за Q188R, в одного — за K285N, у 6 — гетерозиготний генотип за двома мажорними мутаціями (Q188R/K285N), в одного пацієнта виявлений генотип був р.Y209S/р.K285N, ще в одного — виявлена мутація р.K285N тільки в одній алелі. Отже, у 14 пацієнтів досліджені 28 алелей у гені GALT, ідентифіковані 27 мутацій: Q188R — у 57 % спостережень, K285N — у 36 %, р.Y209S — у 3 % (виявлена в одного пацієнта в одній алелі). В цілому мутації Q188R і K285N виявляли з частотою 93 %, що свідчить про високий рівень їх мажорності в українській популяції. Жовтяниця виявлена у 93 % хворих, гепатомегалія — у 80 %, диспептичний синдром — у 87 %. Катаракта була діагностована у 6 (40 %) пацієнтів, в усіх спостереженнях поєднана з неврологічними симптомами. Ураження нервової системи (спастичний тетрапарез, дистонія, тремор, когнітивна недостатність, дизартрія, затримка мовленнєвого розвитку) відзначені у 7 (21,8 %) хворих при КГ. Померли 4 (26,7 %) з 15 пацієнтів віком від 20 днів до 2,5 місяця. За даними клініко-генеалогічного аналізу у родинах хворих на КГ виявлено часті випадки ранньої смерті дітей (віком до 14 тижнів) унаслідок печінкової недостатності. У неонатальному періоді померли 4 дітей із трьох родин з обтяженим анамнезом. У цілому в родинах наших пацієнтів померли 8 (42,1 %) із 19 дітей з аналогічними клінічними симптомами. Лікування всім пацієнтам призначали з суттєвим запізненням, у середньому на 44-й день. Запропоновано схему діагностично-лікувальних заходів у пацієнтів селективної групи. Висновки. КГ — загрозливе для життя захворювання, що характеризується ураженням клітин печінки, диспептичним синдромом, сепсисом і спричиняє високий рівень смертності немовлят у неонатальному періоді. В цілому мутації Q188R і K285N виявлені у 93 % спостережень, що свідчить про високий рівень їх мажорності в українській популяції. Всі немовлята з жовтяницею, зумовленою гіпербілірубінемією, за наявності гепатомегалії, диспепсії, порушень згортання крові, високого рівня трансаміназ мають бути обстежені щодо КГ і негайно переведені на безлактозну дієту до отримання остаточних результатів лабораторної діагностики.
Актуальность. Галактоземия I типа, или классическая галактоземия (КГ), — наиболее тяжелая форма наследственных нарушений обмена углеводов, в частности галактозы. Галактоземия не включена в программу массового неонатального скрининга в Украине. КГ характеризуется неспецифичностью дебютных симптомов, обусловливает высокий уровень смертности в неонатальном периоде. Актуальны вопросы ранней диагностики и лечения новорожденных при КГ при отсутствии в стране программы массового неонатального скрининга в Украине. Цель. Анализ клинико-лабораторных, молекулярно-генетических особенностей КГ, определение комплекса клинических симптомов, формирование селективных групп пациентов для назначения диетотерапии и лабораторной диагностики; разработка поэтапной схемы эффективной ранней диагностики и лечения пациентов при КГ при отсутствии массового неонатального скрининга с целью предотвращения инвалидизации больных и снижения детской смертности. Материалы и методы. В период с 2014 по 2017 г. в Центре орфанных заболеваний обследованы 317 пациентов с диагнозом «гепатит неясного генеза». Возраст больных — от 3 дней до 16 лет. Мальчиков было 145 (45 %), девочек — 172 (55 %). У всех пациентов выявлена полисиндромная клиническая картина с преимущественным поражением печени. У всех больных определяли активность фермента GАLT в эритроцитах периферической крови и ДНК-диагностику с целью выявления мажорных мутаций в гене GАLT. Все пациенты обследованы на предмет вирусных гепатитов; по данным биохимического исследования определяли уровень печеночных трансаминаз, билирубина, щелочной фосфатазы, нарушения свертываемости крови. Также проведена тандемная масс-спектрометрия с целью выявления нарушений обмена аминокислот, органических кислот и митохондриального бета-окисления жирных кислот. У 5 пациентов при подозрении на гликогеноз проведено количественное определение гликогена в биоптате печени. Результаты. КГ диагностирована у 15 (4,7 %) из 317 пациентов: 9 мальчиков и 6 девочек в возрасте от 14 дней до 15 лет. У 13 (86,7 %) из 15 детей клинический диагноз КГ установлен в среднем на 47-е ± 15-е сутки жизни. У 2 пациентов КГ диагностирована в возрасте 2 и 15 лет. У всех пациентов активность фермента GALT в эритроцитах была снижена и составляла 0,08–5,8 Ед/г Hb, в среднем 3,3 ± 1,6 Ед/г Hb (в норме > 10 Ед/г Hb). Молекулярно-генетический анализ проведен у 14 пациентов. У 5 больных выявлен гомозиготный генотип по Q188R, у 1 — по K285N, у 6 — гетерозиготный по двум мажорным мутациям (генотип Q188R/K285N), у 1 пациента выявлен генотип р.Y209S/р.K285N, еще у 1 — обнаружена мутация р.K285N только в одной аллели. Таким образом, у 14 пациентов изучены 28 аллелей в гене GALT, идентифицированы 27 мутаций: Q188R — в 57 % наблюдений, K285N — в 36 %, р.Y209S — в 3 % (у одного пациенте в одной аллели). В целом мутации Q188R и K285N выявлены у 93 % больных, что свидетельствует о высоком уровне их мажорности в украинской популяции. Желтуха выявлена у 93 % пациентов, гепатомегалия — у 80 %, диспепсия — у 87 %. Катаракта диагностирована у 6 (40 %) детей, причем в сочетании с неврологическими симптомами. Поражение нервной системы (спастический тетрапарез, дистония, тремор, когнитивная недостаточность, дизартрия, задержки становления речи) выявлено у 7 (46,7 %) пациентов при КГ. Умерли 4 (26,7 %) детей из 15 в возрасте от 20 дней до 2,5 месяца. По данным клинико-генеалогического анализа в семьях пациентов при КГ выявлены частые случаи ранней детской смерти (в возрасте до 14 недель) вследствие печеночной недостаточности. В неонатальном периоде умерли 4 больных из трех семей. В целом в семьях наших пациентов умерли 8 (42,1 %) из 19 детей с аналогичными клиническими симптомами. Всем пациентам лечение назначено с существенным опозданием, в среднем на 44-е сутки. Предложена этапная схема лечебно-диагностических мероприятий у пациентов селективной группы. Выводы. КГ — угрожающее жизни заболевание, характеризующееся поражением клеток печени, диспептическим синдромом, сепсисом, обусловливающее высокий уровень смертности детей в неонатальном периоде. В целом мутации Q188R и K285N выявлены в 93 % наблюдений, что свидетельствует о высоком уровне их мажорности в украинской популяции. Все младенцы с синдромом желтухи, обусловленной гипербилирубинемией, при наличии гепатомегалии, диспепсии, высокого уровня трансаминаз, нарушений свертываемости крови, должны быть обследованы на КГ и безотлагательно переведены на безлактозную диету до получения окончательных результатов лабораторной диагностики.
Background. Galactosemia type I, or classic galactosemia (CG), is the most severe form of hereditary disorders of carbohydrate metabolism, in particular, galactose. Galactosemia is not included in the program of massive neonatal screening in Ukraine. The CG is characterized by the non-specific onset symptoms and leads to high mortality among infants in the neonatal period. The problem of early diagnosis and treatment of infants with CG in the absence of a program for massive neonatal screening in Ukraine requires solution. The purpose was to analyse the clinical and laboratory, molecular genetic features of patients with CG; to define a set of clinical symptoms and to form selective groups of patients for administration of diet therapy and laboratory diagnosis; to develop schemes-stages of effective early diagnosis and treatment of patients with CG in the absence of mass neonatal screening in order to reduce infant mortality and prevent the disability of patients with this pathology. Materials and methods. In 2014–2017, 317 patients with a diagnosis of hepatitis of uncertain origin were examined. The age of patients ranged from 3 days to 16 years; 145 (45 %) of them were males, 172 (55 %) — females. In all patients, a polysyndromic clinical picture with predominant lesion in the liver function was observed. All patients were examined for the activity of galactose-1-phosphate uridylyltransferase (GALT) enzyme in the red blood cells and underwent DNA diagnosis for the detection of major mutations in the GALT gene. All patients were examined for viral hepatitis, underwent biochemical blood tests for hepatic transaminases, alkaline phosphatase, bilirubin levels, and coagulopathy. Tandem mass spectrometry was also performed to exclude or confirm the metabolic imbalance of amino acids, organic acids, and mitochondrial beta-oxidation of fatty acids. Five patients with suspected glycogenosis have been subjected to a quantitative glycogen test in the liver biopsy sample. Results. The diagnosis of CG was established in 15 (5 %) of 317 patients. Male/female ratio was 9 : 6, patient’s age ranged from 14 days to 15 years at the time of investigation in the Center. In 13 out of 15 children, the clinical diagnosis of CG was made on average of 47 days of life (47 ± 15 days). In two patients, the CG was diagnosed at the age of 2 and 15 years. In all patients, the activity of GALT enzyme in erythrocytes was reduced and ranged from 0.08 to 5.8 U/g Hb (mean value 3.3 ± 1.6 U/g Hb) at a normal value > 10 U/g Hb. Molecular genetic analysis was performed in 14 patients. Five patients had a homozygous genotype of Q188R, 1 patient — homozygous K285N genotype, 6 patients were heterozygotes in two major mutations, Q188R and K285N (genotype Q188R/K285N); one patient had р.Y209S/р.K285N genotype, another one — р.K285N mutation only in one allele. Thus, 28 alleles in the GALT gene were examined from 14 patients and 27 mutations were identified: Q188R —57 %, K285N — 36 %, Y209S — 3 % (detected in one patient in one allele). The mutations Q188R and K285N together amounted to 93 % indicating a high level among Ukrainian population. Cataract has been diagnosed in 6 patients (40 %). In our group of CG patients, in all of them it was combined with neurological symptoms. Defeats of the nervous system (cognitive deficiency, spastic tetraparesis, dystonia, tremor and disorders in the form of dysarthria and delayed speech development) were noted in 7 CG patients (47 %). The analysis of the mortality in this group showed that it was 27 % (4 of 15 patients dead at the age of 24 days to 2.5 months). Additionally, the analysis of families with CG patients showed frequent cases of early death from liver failure in the age up to 14 weeks. In three families, there were four deaths in the neonatal period. If we consider all dead children with similar symptoms in the families with CG patients, then the percentage of deceased patients would be 47 % (8 of 19 children born in families with CG). In all cases, treatment was started too late, on average on day 44. Jaundice was observed in 93 % of CG patients, hepatomegaly — in 80 %, dyspeptic manifestations — in 87 %. The scheme has been proposed of stages of diagnostic and therapeutic measures in the selective group with suspected CG. Conclusions. CG is a life-threatening disease characterized by severe hepatocellular lesions, dyspeptic syndrome, sepsis, and high mortality in the neonatal period. Mutations Q188R and K285N together make up 93 % that indicates a high level in Ukraine. All infants with jaundice due to hyperbilirubinemia, hepatomegaly, dyspeptic disorders, high levels of transaminases, and blood clotting disorders should be screened for the presence of CG and urgently change the diet to lactose-free one, until the results of the confirmatory laboratory diagnosis are obtained.
Робота виконана в рамках НДР «Визначення генетичних основ ризику розвитку патологічних станів на різних етапах онтогенезу», номер держреєстрації 0114U002215 (2014–2018 рр.).
Вступ
Спадкові порушення обміну речовин, за яких відзначають ураження печінки, представлені великою групою моногенних захворювань, спричинених мутацією структурних генів, які контролюють синтез різних функціональних білків організму. Одним із характерних захворювань цієї групи є галактоземія (E742 за МКХ-10), що належить до спадкових порушень обміну вуглеводів [1].
В основі захворювання лежать мутації генів ферментів, що беруть участь у метаболізмі галактози, яка відіграє важливу роль в організмі, особливо під час росту і розвитку дитини. Галактоза — важливе джерело енергії для клітин організму, крім того, є пластичним матеріалом для синтезу глікопротеїнів, гліколіпідів та інших комплексних сполук, які входять до складу клітинних мембран, мієліну структур центральної нервової системи (ЦНС). Основним джерелом галактози для людини є їжа: більшість продуктів харчування містять лактозу, що у кишечнику шляхом гідролізу перетворюється на галактозу; певні продукти харчування містять галактозу у чистому вигляді.
Під терміном «галактоземія» розуміють групу з трьох спадкових автосомно-рецесивних захворювань, при яких в організмі хворого накопичується надлишок галактози та її метаболітів [2] внаслідок мутацій у генах ферментів, які беруть участь у ланцюгу реакцій перетворення галактози на глюкозу (шлях Leloir) [1]. Вроджена недостатність одного з трьох ферментів [1]: галактозо-1-фосфатуридинтрансферази (ГАЛТ; GALT), галактокінази (ГАЛК; GALK) і уридиндифосфат-галактозо-4-епімерази (ГАЛЕ; GALE) призводить до накопичення галактозо-1-фосфату, галактози і галактитолу в еритроцитах, клітинах печінки та інших тканинах, що впливає на осмотичні процеси, спричиняє виникнення набряків, тяжкого ураження печінки, нервової системи, катаракти, сепсису [3]. Сучасна класифікація галактоземій побудована за етіологічним принципом [4] (табл. 1).
Дана робота присвячена класичній галактоземії (КГ) І типу.
Уперше КГ була описана у 1908 р. von Reuss як класична клінічна картина захворювання у немовляти (несподівана відмова дитини від годування, тяжке ураження печінки, галактозурія; стан покращився після виключення з раціону грудного молока) [5].
КГ — найбільш тяжка форма порушення метаболізму галактози. Захворювання зазвичай маніфестує в перші дні або тижні життя дитини, швидко прогресує, за відсутності лікування є фатальним. На тлі грудного вигодовування у новонародженого виникають блювання, діарея, гіпотонія м’язів, млявість, летаргія. Невдовзі виникає і прогресує ураження печінки, що супроводжується її збільшенням, жовтяницею, нерідко — кровоточивістю внаслідок гіпокоагуляції. Вже у перші дні після народження у таких дітей нерідко виявляють катаракту, крововиливи у склоподібне тіло [3]. За результатами лабораторних досліджень виявляють підвищення активності трансаміназ, фракцій білірубіну (некон’югована гіпербілірубінемія, що на пізніх стадіях захворювання може трансформуватися у кон’юговану), гіпоглікемію, гіпоальбумінемію, підвищення вмісту аміаку й амінокислот, зокрема за рахунок фенілаланіну, тирозину та метіоніну. Знижений синтез VIII фактора згортання крові. Нерідко виявляють гіперхлоремічний метаболічний ацидоз, гіпофосфатемію, генералізовану гіпераміноацидурію, що свідчить про вторинну дисфункцію канальців нирок. За даними ультразвукового дослідження відзначають збільшення розмірів печінки. Запальні зміни у периферичній крові на тлі підвищення рівня С-реактивного білка та позитивного прокальцитонінового тесту є критерієм приєднання сепсису. Якщо хворим на КГ своєчасно не призначена безлактозна/безгалактозна дієта, майже 75 % з них помирають у перші місяці життя через печінкову недостатність або сепсис, спричинений грампозитивними мікроорганізмами (у 90 % спостережень E.сoli) [4]. У дітей, які виживають, виникає хронічна печінкова недостатність, тяжке ураження нервової системи, виражена затримка психомоторного розвитку, що призводить до глибокої інвалідизації та зменшення тривалості життя [6].
Єдиний метод лікування КГ — негайне та цілковите виключення галактози та лактози з раціону харчування дитини. Цей простий захід запобігає виникненню небезпечних для життя станів у неонатальному періоді, запобігає смерті дитини, зменшує ймовірність виникнення віддалених наслідків у вигляді ураження нервової системи [7].
КГ — найбільш поширене захворювання, спричинене порушенням обміну галактози. Частота його виявлення у новонароджених у різних етнічних популяціях варіабельна: від 1 : 16 476 в Ірландії до 1 : 47 000 — у Східній Європі та 1 : 146 000 — у Швеції. В середньому частота виявлення галактоземій становить 1 : 40 000–60 000 новонароджених, проте в країнах Азії це захворювання зустрічається набагато рідше [8, 9]. За даними масового неонатального скринінгу, в Російській Федерації галактоземію виявляють в 1 з 20 149 новонароджених [10].
Ген, який кодує фермент GALT, розташований на хромосомі 9p13, включає близько 4,3 кБ ДНК, складається з 11 екзонів [11, 12].
В останньому оновленні бази даних Університету UTAH зазначені 336 мутацій у гені GALT [13]. При КГ існує виражена кореляція між гено- та фенотипом. Характер мутацій та їх поєднання в гені впливають на резидуальну активність ферменту GALT. Описані м’які (варіант Дуарте) або асимптомні (варіант Лос-Анджелес) клінічні форми КГ, за яких відзначають підвищений рівень галактози [14].
У 1964 р. Е. Вeutler запропонував метод, за допомогою якого можна визначити наявність галактози у сухих плямах крові, отриманих для скринінгу на фенілкетонурію. Галактоземія — друге орфанне метаболічне захворювання після фенілкетонурії, яке почали виявляти під час масового неонатального скринінгу у 60-ті роки ХХ ст. у США і багатьох країнах Європи [5, 15]. Золотий стандарт лабораторної діагностики при КГ — визначення активності ферменту GALT в еритроцитах крові хворого.
В Україні програма масового неонатального скринінгу охоплює лише 4 спадкових захворювання, галактоземія до неї не включена. Виражений генетичний і клінічний поліморфізм КГ, неспецифічні симптоми дебюту захворювання, його ранній початок, висока смертність немовлят за відсутності своєчасної дієтотерапії потребують вирішення цілої низки нагальних питань [16, 17].
Мета: аналіз клініко-лабораторних, генетичних особливостей пацієнтів при КГ; розробка схеми етапів ефективної діагностики та лікування, зниження дитячої смертності, запобігання інвалідизації таких хворих.
Матеріали та методи
2014 р. у практичну діяльність медико-генетичної лабораторії та Центру орфанних захворювань НДСЛ «ОХМАТДИТ» впроваджені протоколи визначення активності ферменту GАLT в еритроцитах периферичної крові та ДНК-діагностика з метою виявлення мажорних мутацій в гені GАLT. Ці дослідження включені до протоколу обстеження пацієнтів з порушенням функції печінки. Впродовж 2014–2017 рр. обстежено 317 пацієнтів, у яких діагностований гепатит невизначеного генезу. 222 (70 %) хворих лікували у педіатричному, хірургічному відділеннях або відділенні інтенсивної терапії, 95 (30 %) пацієнтів обстежені амбулаторно. Хлопчиків було 145 (45 %), дівчаток — 172 (55 %), вік хворих — від 3 днів до 10 років В усіх спостереженнях відзначали полісиндромну клінічну картину з переважним ураженням печінки. Найчастіше у хворих виявляли жовтяницю, синдром цитолізу, коагулопатію, диспепсію, катаракту. Поєднання цих синдромів стало критерієм для формування селективної групи пацієнтів, яким проводили додаткове дослідження з метою діагностики КГ.
Усім пацієнтам проведені дослідження на наявність вірусних гепатитів, коагулограма, визначення рівня печінкових трансаміназ, лужної фосфатази, білірубіну. Всім хворим проведена тандем-мас-спектрометрія з метою виявлення порушень обміну амінокислот, органічних кислот і їх мітохондріального бета-окислення. У 5 пацієнтів за припущення про наявність глікогенозу визначали вміст глікогену у біоптаті печінки.
Клінічні симптоми КГ у пацієнтів селективної групи (рис. 1). Найчастіше виявляли жовтяницю (89 %) і гепатомегалію (46 %). Спленомегалія діагностована у 29 % хворих, синдром холестазу — у 29 %, відмова дитини від годування — у 49 %. Неврологічні порушення (зокрема, судороги) відзначено у 26 % спостережень, блювання — у 16 %, кровотеча — у 16 %, сепсис, асцит і/або набряки, летаргія, когнітивна недостатність — по 10 % спостережень, затримка фізичного розвитку, діарея, розлади дихання, катаракта — по 1 % спостережень.
Лабораторні показники у пацієнтів селективної групи (рис. 2). Гіпербілірубінемія виявлена у 75 % хворих, анемія — 49 %, коагулопатія — 39 %, гіпопротеїнемія — у 26 %, тромбоцитопенія та гіпоглікемія — по 16 % спостережень; синдром цитолізу відзначений у 48 % пацієнтів, підвищення рівня α-фетопротеїну — 10 %, феритину — в 1 %.
Для виявлення КГ застосовували якісні та кількісні методи діагностики: в усіх пацієнтів визначали активність ферменту GALT в еритроцитах крові, галактози в крові та сечі за допомогою тонкошарової хроматографії (ТШХ). Молекулярно-генетичне дослідження, що дозволяє виявити мутації в гені GALT, проводили за суттєвого зниження активності ферменту GALT.
Для ТШХ використовували вранішню або добову сечу та гепаринізовану капілярну кров. Аналіз проводили на пластинах завдовжки 20 см із покриттям Silica gel 60 на алюмінієвій підложці (Merck), на які наносили 10–20 мкл досліджуваної біологічної рідини (еквівалент 20 мкг/л креатиніну). Система розчинників складалася з льодяної оцтової кислоти, бутанолу та деіонізованої води у співвідношенні 2 : 1 : 1. Як стандарт використовували 10 мкл суміші 10% розчину фукози, глюкози, галактози, сахарози, мальтози та лактози. Для візуалізації фракцій вуглеводів застосовували орциновий реагент (50 мг орцину, 9,5 мл етилового спирту, 0,5 мл сірчаної кислоти), яким поливали пластини з подальшим їх нагріванням при 100 °С до появи забарвлення [18].
Активність GALT в еритроцитах визначали у зразках цільної венозної гепаринізованої крові за допомогою флуорогенного методу за результатами уридилтрансферазної трансформації галактозо-1-фосфату на 6-фосфатглюконат за допомогою глюкозо-6-фосфатдегідрогенази, яка міститься в еритроцитах. Реакція супроводжується вивільненням нікотинамідаденіндинуклеотидфосфату, який флюоресціює в ультрафіолетовому світлі [19]. Флюо–ресценцію оцінювали за допомогою багатофункціонального аналізатора Victor (Wallac Oy, Фінляндія), довжина хвилі збудження — 365 нм, емісія — 448 нм.
Детекція мажорних мутацій Q188R і K285N [20] в гені GALT здійснена за допомогою алельспецифічної полімеразної ланцюгової реакції на термоциклері SimpliAmp (AB, США) з використанням праймерів [3] та комерційних наборів GenPak PCR Core (Neogen, Україна). Візуалізацію та реєстрацію результатів здійснено за допомогою капілярного електрофорезу MultiNA (Shimadzu Biotech, Японія).
Диференціальну діагностику проводили з галактоземією, гепатитом, вродженими вадами розвитку, зокрема атрезією жовчовивідних шляхів; внутрішньопечінковим холестазом, гемохроматозом новонароджених, тирозинемією I типу, лізосомними хворобами накопичення; глікогенозами, муковісцидозом, вродженими порушеннями мітохондріального бета-окислення жирних кислот.
Результати та обговорення
За сукупністю даних анамнезу, клінічного перебігу захворювання, лабораторних та інструментальних методів дослідження КГ діагностовано у 15 (5 %) із 317 пацієнтів (9 хлопчиків і 6 дівчаток, вік хворих від 14 днів до 15 років).
Найчастіше у хворих на КГ виявляли жовтяницю (93 %), гепатомегалію (87 %), синдром цитолізу (80 %), тобто такі самі симптоми, що й у пацієнтів групи селективного скринінгу. Проте ураження клітин печінки при КГ було тяжчим і проявлялося коагулопатією (виявлена у 66 % спостережень), асцитом (53 %) та диспептичним синдромом (відмовою від їжі, блюванням — у 53 %, діареєю — 40 %, затримкою збільшення маси тіла — 87 %). Сепсис діагностований у 33 % хворих на КГ, що також відрізняло цих пацієнтів від групи селективного скринінгу з діагнозом «гепатит невизначеної етіології».
За даними біохімічного дослідження, у хворих на КГ виявлена генералізована гіпераміноацидопатія, що значно утруднювало диференціальну діагностику галактоземії зі спадковими порушеннями обміну амінокислот. Крім того, у 35 % хворих на КГ виявлений гіпоглікемічний синдром.
У 13 (86,7 %) з 15 дітей КГ клінічно діагностована у середньому на 47-й ± 15-й день життя; у 2 хворих (пацієнти № 2 і 3) діагноз встановлений у віці 2 і 15 років (табл. 2). Отже, в усіх хворих КГ діагностована запізно. Тяжкий, фатальний перебіг захворювання потребує призначення відповідної дієтотерапії до 7-го дня життя дитини [6].
Ферментодіагностика проведена у 14 (93,3 %) хворих; в одного пацієнта (№ 11) проведення цього дослідження було недоцільним через раніше здійснене переливання дитині крові у відділення реанімації. Оскільки активність GALT визначають в еритроцитах, наявність у крові хворого донорських еритроцитів впливає на результат дослідження; тому забір крові для ферментодіагностики при КГ необхідно здійснити до переливання хворому крові та її препаратів, зокрема еритроцитарної маси.
В усіх пацієнтів відзначене зниження активності ферменту GALT в еритроцитах крові від 0,08–5,8 Од/г (середнє значення — 3,3 ± 1,6 Од/г Hb) при нормі > 10 Од/г Hb.
ТШХ застосована в 10 пацієнтів, у крові та сечі п’ятьох із них виявлено галактозу; п’ятеро хворих на момент проведення дослідження перебували на безлактозній дієті, у них проведення ТШХ було недоцільним.
Молекулярно-генетичний аналіз проведений у 14 пацієнтів: у 5 з них виявлений гомозиготний генотип за Q188R, в 1 — гомозиготний генотип за K285N, у 6 — гетерозиготний генотип за двома мажорними мутаціями Q188R і K285N (генотип Q188R/K285N), в 1 пацієнта виявлений генотип р.Y209S/р.K285N, ще в 1 — відзначали мутацію р.K285N тільки в одній з алелей. Отже, у 14 пацієнтів досліджені 28 алелей в гені GALT, ідентифіковано 27 мутацій: Q188R — у 57 % спостережень, K285N — у 36 %, р.Y209S — у 3 %. Загалом мутації Q188R і K285N виявлені у 93 % пацієнтів, що свідчить про високий рівень їх мажорності у населення України, лише в одного хворого виявлена рідкісна мутація, описана у 1998 р., яку було внесено до бази даних мутацій у гені GALT [13].
Катаракта виявлена у 6 (40 %) пацієнтів. Зазвичай при КГ катаракту виявляють на 2–3-й тиждень життя дитини, більшість дослідників відносять її до «віддалених» симптомів. Так, діагноз у пацієнта № 3 (К-ний, хлопчик) остаточно встановлений у віці 16 років і виявився спорадичною знахідкою. Саме катаракта стала критерієм відбору хворих для обстеження на наявність КГ. У пацієнта відзначали виражену затримку фізичного розвитку, спастичний тетрапарез, вроджену катаракту; хворого спостерігали з діагнозом «дитячий церебральний параліч».
На нашу думку, виявлення катаракти на першому тижні життя дитини не є специфічним симптомом, проте її виявлення у ранньому дитинстві та підлітковому віці в поєднанні з порушенням функцій ЦНС вимагає спростування діагнозу КГ. У наших спостереженнях в усіх хворих при КГ відзначали катаракту у поєднанні з неврологічними симптомами.
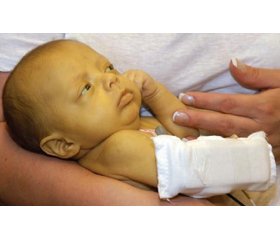
Ураження нервової системи: спастичний тетрапарез, тремор, дистонія когнітивні порушення, дизартрії відзначені нами у 7 (47 %) хворих (рис. 3, табл. 3). Варто зазначити, що ураження нервової системи відносять до віддалених ускладнень КГ. Галактоза відіграє важливу роль у побудові структурних компонентів ЦНС, проте патогенез ураження нервової системи при КГ до цього часу остаточно не визначений, зокрема, немає пояснення щодо виникнення симптомів ураження ЦНС за своєчасного встановлення діагнозу та призначення відповідної дієтотерапії. Деякі автори вважають КГ нейродегенеративним захворюванням, порушення, що при цьому виникають, на їх думку, зумовлені особливостями обміну ендогенної галактози [21]. Однак інші дослідники заперечують нейродегенеративний характер захворювання [22, 23].
/80-1.jpg)
Четверо з 15 (26,7 %) дітей, яких ми спостерігали, померли у віці від 20 днів до 2,5 міс. За даними клініко-генеалогічного аналізу у родинах хворих на КГ виявлені непоодинокі випадки ранньої смерті дітей (до 14 тижнів життя) внаслідок печінкової недостатності. У трьох родинах 4 дітей померли у неонатальному періоді. В цілому у родинах наших пацієнтів померли 8 з 19 (47 %) дітей, у яких відзначали характерні для КГ симптоми. Отже, КГ становить надзвичайно серйозну загрозу життю хворих дітей, несвоєчасна діагностика та лікування негативно позначаються на показниках ранньої дитячої смертності.
Оскільки в Україні не проводиться масовий скринінг новонароджених щодо КГ, вивчення епідеміологічних особливостей галактоземії та розробка ефективної профілактики ранньої дитячої смертності в родинах з обтяженим анамнезом практично неможливі. Проте ранній дебют захворювання вимагає організації масового неонатального скринінгу, оскільки лікування необхідно розпочинати до кінця першого тижня життя немовляти. Хоча в де–яких країнах неонатальний скринінг через пропущені випадки захворювання вважають неефективним [16], але в цілому відзначають доцільність його проведення [17].
В Україні КГ діагностують винятково клінічно, тому ймовірність збереження високого рівня смертності таких немовлят є досить високою, як і в інших країн із подібною ситуацією. Зокрема, у Мексиці КГ також діагностують клінічно, майже 80 % немовлят вчасно не призначають лікування, показники ранньої дитячої смертності досить високі, навіть за наявності типових дебютних симптомів захворювання [21]. Отже, обізнаність щодо КГ, правильна клінічна оцінка стану пацієнтів, формування селективної групи ризику сприятимуть вчасному проведенню діагностичних досліджень і призначенню немовлятам безлактозної дієти [4]. За результатами проведеного дослідження запропонована поетапна схема лікувально-діагностичних заходів при КГ (рис. 4).
Висновки
КГ — загрозливе для життя захворювання, що характеризується ураженням печінки, диспепсією, сепсисом і спричиняє смертність немовлят у неонатальному періоді.
В Україні впроваджений комплекс лабораторної діагностики КГ. У цілому мутації Q188R і K285N виявляють у 93 % спостережень, що свідчить про високий рівень їх мажорності в українській популяції.
Всі немовлята при жовтяниці, гепатомегалії, диспепсії, за високого рівня трансаміназ, порушення згортання крові мають бути обстежені на наявність КГ і негайно переведені на безлактозну дієту до отримання остаточних результатів лабораторної діагностики.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Sarafoglou K. Pediatric endocrinology and inborn errors of metabolism / K. Sarafoglou, G.F. Hoffmann, K.S. Roth. — McGraw-Hill Education, 2017. — 2nd ed. — P. 127-134. ISBN: 9780071773140.
2. Berry G.T. Introduction to the Maasticht workshop on galactosemia: lessons from the past and new directions in galactosemia / G.T. Berry, L.J. Elsas // J. Inherit. Metab. Dis. — 2011. — Vol. 34, N 2. — P. 249-255. doi: 10.1007/s10545-010-9232-1. PMID: 21116719.
3. International clinical guideline for the management of classical galactosemia: diagnosis, treatment, and follow-up / L. Welling, L.E. Bernstein, G.T. Berry [et al.] // J. Inherit. Metab. Dis. — 2017. — Vol. 40, N 2. — P. 171-176. doi: 10.1007/s10545-016-9990-5. PMID: 27858262. PMCID:PMC5306419.
4. Berry G.T. Classic galactosemia and clinical variant galactosemia. GeneReviews® [Internet] / G.T. Berry // Seattle (WA): University of Washington, Seattle, 1993–2017. Bookshelf ID: NBK1518. PMID: 20301691. Available online: https://www.ncbi.nlm.nih.gov/books/NBK1518.
5. Ridel K. An updated review of the long-term neurological effects of galactosemia / K. Ridel, N. Leslie, D. Gilbert // Pediatr. Neurol. — 2005. — Vol. 33. — P. 153-161. doi: 10.1016/j.pediatrneurol.2005.02.015. PMID: 16087312.
6. Movement disorders in adult patients with classical galactosemia / I. Rubio-Agusti, M. Carecchio, K.P. Bhatia [et al.] // Mov. Disord. — 2013. — Vol. 28, N 6. — P. 804-810. doi: 10.1002/mds.25348. PMID: 23400815.
7. Galactose content of legumes, caseinates, and some hard cheeses: implications for diet treatment of classic galactosemia/ S.C. van Calcar, L.E. Bernstein, F.J. Rohr [et al.] // J. Agric. Food Chem. — 2014. — Vol. 62, N 6. — P. 1397-1402. doi: 10.1021/jf404995a. PMID: 24456566.
8. Selective screening for metabolic disorders in the Slovenian pediatric population / B.R. Lampret, S. Murko, M.Ž. Tanšek [et al.] // J. Med. Biochem. — 2015. — Vol. 34, N 1. — P. 58-63. doi: 10.2478/jomb-2014-0056. PMID: 28356825. PMCID:PMC4922335.
9. Classical galactosemia in Ireland: incidence, complications and outcomes of treatment / K.P. Coss, P.P. Doran, C. Owoeye [et al.] // J. Inherit. Metab. Dis. — 2013. — Vol. 36, № 1. — P. 21-27. doi: 10.1007/s10545-012-9507-9. PMID: 22870861.
10. Федеральные клинические рекомендации по диагностике и лечению галактоземии // А.А. Баранов, Т.Э. Боровик, Т.В. Бушуева [и др.]. — М., 2016. — 33 с. [Internet] Available online: http://www.pediatr-russia.ru/sites/default/files/file/kr_gal.pdf.
11. Classical galactosemia and mutations at the galactose-1-phosphate uridyl transferase (GALT) gene / L. Tyfield, J. Reichardt, J. Fridovich-Keil [et al.] // Hum. Mutat. — 1999. — Vol. 13, № 6. — P. 417-430. doi: 10.1002/(SICI)1098-1004(1999)13:6<417::AID-HUMU1>3.0.CO;2-0. PMID: 10408771.
12. Frequency distribution of Q188R, N314D, Duarte 1, and Duarte 2 GALT variant alleles in an Indian galactosemia population / R. Singh, B.R. Thapa, G. Kaur [et al.] // Biochem. Genet. — 2012. — Vol. 50, N 11–12. — P. 871-880. doi: 10.1007/s10528-012-9527-z. PMID: 22798028.
13. База даних Університету UTAH. Available online: http://www.arup.utah.edu/database/GALT/GALT_display.php.
14. Berry G.T. Galactosemia: when is it a newborn screening emergency? / G.T. Berry // Mol. Genet. Metab. — 2012. — Vol. 106, N 1. — P. 7-11. doi: org/10.1016/j.ymgme.2012.03.007. PMID: 22483615.
15. Beutler E. A new method for the detection of galactosemia and its carrier state / E. Beutler, M. Baluda, G.N. Donnell // J. Lab. Clin. Med. — 1964. — Vol. 64. — P. 694-705. PMID: 14233158.
16. Appropriateness of newborn screening for classic galactosaemia: a systematic review / L. Varela-Lema, L. Paz-Valinas, G. Atienza-Merino [et al.] // J. Inherit. Metab. Dis. — 2016. — Vol. 39, N 5. — P. 633-649. doi: 10.1007/s10545-016-9936-y. PMID: 27116003.
17. Nine years of newborn screening for classical galactosemia in the Netherlands: Effectiveness of screening methods, and identification of patients with previously unreported phenotypes / L. Wel–ling, A. Boe–len, T.G. Derks [et al.] // Mol. Genet. Metab. 2017. — Vol. 120, N 3. — P. 223-228. doi: 10.1016/j.ymgme.2016.12.012. PMID: 28065439.
18. Рыбакова К.Д. Биохимические методы диагностики наследственных болезней / К.Д. Рыбакова, Н.А. Кузьмичева. — М., 1984. — С. 32-35.
19. Frank A. A screening procedure and a specific quantitative method for UDF glucose: a-D-galactose-1-phosphate uridylytransferase / A. Frank, D. Iboott, D. Shapcott [et al.] // Clin. Chem. — 1977. — Vol. 23, N 7. — P. 1348-1355.
20. Detection of common mutations in the GALT gene through ARMS / U. Mahmood, M. Imran, S.I. Naik [et al.] // Gene. — 2012. — Vol. 509, N 2. — P. 291-294. doi: 10.1016/j.gene.2012.08.010. PMID: 22963887.
21. Diversity of approaches to classic galactosemia around the world: a comparison of diagnosis, intervention, and outcomes / P.P. Jumbo-Lucioni, K. Garber, J. Kiel [et al.] // J. Inherit. Metab. Dis. — 2012. — Vol. 35, N 6. — P. 1037-1049. doi: 10.1007/s10545-012-9477-y. PMID: 22450714. PMCID:PMC3774053.
22. Cryptic residual GALT activity is a potential modifier of scholastic outcome in school age children with classic galactosemia / E.L. Ryan, M.E. Lynch, E. Taddeo [et al.] // J. Inherit. Metab. Dis. — 2013. — Vol. 36, N 6. — P. 1049-1061. doi: 10.1007/s10545-012-9575-x. PMID: 23319291. PMCID:PMC3657299.
23. Movement disorders in adult patients with classical galactosemia / I. Rubio-Agusti, M. Carecchio, K.P. Bhatia [et al.] // Mov. Di–sord. — 2013. — Vol. 28, N 6. — P. 804-810. doi: 10.1002/mds.25348. PMID: 23400815.

/75-1.jpg)
/77-1.jpg)
/78-1.jpg)
/79-1.jpg)
/80-1.jpg)
/81-1.jpg)